子宮內(nèi)膜異位組織中VEGF、c-fos表達(dá)及意義
潘虹,刁靜,湯蘊(yùn)琦,潘穎琳,李佳蕊,張萍(上海交通大學(xué)醫(yī)學(xué)院附屬新華醫(yī)院,上海200092)
?
子宮內(nèi)膜異位組織中VEGF、c-fos表達(dá)及意義
潘虹,刁靜,湯蘊(yùn)琦,潘穎琳,李佳蕊,張萍(上海交通大學(xué)醫(yī)學(xué)院附屬新華醫(yī)院,上海200092)
摘要:目的探討子宮內(nèi)膜異位組織中血管內(nèi)皮生長因子(VEGF)、c-fos表達(dá)及意義。方法選擇23例子宮內(nèi)膜異位癥(EMs)患者異位內(nèi)膜組織23例份(異位內(nèi)膜組)及在位內(nèi)膜組織20例份(在位內(nèi)膜組),正常子宮內(nèi)膜組織21例份(對照組)。采用免疫組化SP法檢測各組VEGF表達(dá),蛋白免疫印跡法檢測各組c-fos表達(dá),并分析內(nèi)膜組織VEGF與c-fos蛋白表達(dá)的關(guān)系。結(jié)果異位內(nèi)膜組和在位內(nèi)膜組VEGF、c-fos表達(dá)均高于對照組,P均<0.05;異位內(nèi)膜組和在位內(nèi)膜組VEGF、c-fos表達(dá)比較,P均>0.05。子宮內(nèi)膜組織中VEGF與c-fos表達(dá)呈正相關(guān)(r=0.425,P<0.05)。結(jié)論EMs患者在位及異位內(nèi)膜組織中VEGF與c-fos表達(dá)均升高;c-fos可能通過上調(diào)VEGF表達(dá),促進(jìn)子宮內(nèi)膜組織血管生成,繼而引起EMs的發(fā)生。
關(guān)鍵詞:子宮內(nèi)膜異位癥;血管內(nèi)皮生長因子;c-fos
子宮內(nèi)膜異位癥(EMs)是指具有生長功能的子宮內(nèi)膜組織,如腺體和間質(zhì),出現(xiàn)在子宮腔被覆內(nèi)膜及宮體肌層以外的其他部位。育齡期婦女EMs的發(fā)病率為10%~15%[1],不孕癥患者發(fā)病率高達(dá)40%[2]。EMs是一種良性疾病,但具有轉(zhuǎn)移、侵襲等惡性生物學(xué)行為。研究發(fā)現(xiàn),血管形成與EMs的發(fā)生密切相關(guān)[3,4]。c-fos、血管內(nèi)皮生長因子(VEGF)是調(diào)節(jié)血管形成的重要因子,但其與EMs發(fā)病的關(guān)系鮮見報道。為此,我們進(jìn)行了如下研究。
1資料與方法
1.1臨床資料選取2010年6月~2012年6月在我院行腹腔鏡和開腹手術(shù)的EMs患者23例,年齡24~47歲、平均35.6歲,均為卵巢子宮內(nèi)膜異位囊腫,無其他合并癥;既往月經(jīng)規(guī)律,術(shù)前6個月未服用任何激素類藥物,術(shù)后病理檢查確診為EMs;參照1985年美國生育學(xué)會修訂的EMs分期標(biāo)準(zhǔn)(r-AFS),均為Ⅱ、Ⅲ期。術(shù)后取其異位內(nèi)膜組織23例份(異位內(nèi)膜組),其中增生期12例份、分泌期11例份,HE染色后均可見子宮內(nèi)膜腺體;取其在位內(nèi)膜組織20例份(在位內(nèi)膜組),其中增生期11例份、分泌期9例份。選取正常子宮內(nèi)膜組織21例份(對照組),均由其他良性疾病行子宮切除或?qū)m腔鏡檢查刮宮所得,病理檢查證實(shí)均無子宮內(nèi)膜病變,其中增生期11例份、分泌期10例份。患者年齡26~48歲,平均36.3歲。
1.2VEGF表達(dá)檢測各組標(biāo)本分為兩份,一份立即浸泡在10%甲醛中固定,常規(guī)石蠟包埋,4 μm厚連續(xù)切片。采用免疫組化SP法檢測VEGF表達(dá),操作步驟嚴(yán)格按試劑盒說明書進(jìn)行。采用Image-Pro Plus6.0軟件分析顯微鏡下放大400倍的VEGF免疫組化圖像。分析前先對陽性目標(biāo)彩色分割、編輯,獲得滿意圖形、圖像,選取相應(yīng)區(qū)域,測量其積分光密度(IOD)及面積,以IOD值除以測量面積得到平均光密度。每張切片在高倍鏡下選取10個視野,計算10次平均光密度,取平均值。
1.3c-fos表達(dá)檢測將另一份標(biāo)本立即放入液氮中,置于-80 ℃超低溫冰箱保存,采用蛋白免疫印跡法檢測c-fos表達(dá)。加入組織裂解液后提取蛋白,測定蛋白濃度,裂解組織以每孔30 μg上樣,行聚丙烯酰胺凝膠電泳。電轉(zhuǎn)移至硝酸纖維素膜,封閉后依次加入兔抗人c-fos多克隆抗體、兔抗人actin多克隆抗體和辣根過氧化物酶標(biāo)記的羊抗兔IgG,最后經(jīng)化學(xué)熒光發(fā)光法顯影試劑盒顯影,操作過程按說明書進(jìn)行。采用數(shù)字凝膠成像系統(tǒng)對結(jié)果進(jìn)行灰度掃描分析,相對表達(dá)量以c-fos灰度面積積分與內(nèi)參照肌動蛋白actin的比值表示。

2結(jié)果
異位內(nèi)膜組和在位內(nèi)膜組VEGF、c-fos表達(dá)均高于對照組,P均<0.05;異位內(nèi)膜組和在位內(nèi)膜組VEGF、c-fos表達(dá)比較,P均>0.05。見表1。直線相關(guān)分析顯示,子宮內(nèi)膜組織VEGF與c-fos表達(dá)呈正相關(guān)(r=0.425,P<0.05)。
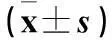
表1 各組VEGF、c-fos表達(dá)比較
注:與對照組比較,*P<0.05。
3討論
EMs是雌激素依賴性良性病變,但具有一些類似惡性腫瘤的生物學(xué)行為,特別是組織侵襲和血管形成能力。目前EMs發(fā)病機(jī)制尚未明確,以Sampson的經(jīng)血逆流種植學(xué)說為主。但經(jīng)血逆流至盆腔是普遍的生理現(xiàn)象,其中發(fā)生EMs者只占10%~15%[5],提示經(jīng)血逆流可能只是誘因。因此,探討子宮內(nèi)膜在腹腔內(nèi)種植生長的機(jī)制才是闡明EMs發(fā)病的關(guān)鍵。目前認(rèn)為,黏附、侵襲、血管形成是內(nèi)膜異位種植的病理生理過程[6],其中黏附和侵襲的過程很短暫,而異位種植病灶的發(fā)生和發(fā)展依賴于充足的血液供應(yīng),故認(rèn)為血管異常增生是EMs發(fā)病的重要原因[7]。
VEGF具有多種生物學(xué)效應(yīng),被認(rèn)為是調(diào)節(jié)血管生長作用最強(qiáng)的因子[8,9]。原癌基因c-fos是受雌激素作用的靶基因之一,人類和小鼠c-fos基因啟動子區(qū)域存在功能性雌激素反應(yīng)元件,雌激素作用后c-fos表達(dá)顯著上升,并與Jun蛋白形成轉(zhuǎn)錄因子AP-1,調(diào)節(jié)細(xì)胞侵襲、生長及血管形成等相關(guān)靶基因的表達(dá)。因此,c-fos被認(rèn)為是雌激素早期應(yīng)答基因,可作為雌激素作用的早期感受分子[10,11]。“在位內(nèi)膜決定論”認(rèn)為, EMs患者在位內(nèi)膜組織VEGF表達(dá)明顯高于非EMs[6]。本研究異位內(nèi)膜組和在位內(nèi)膜組VEGF、c-fos表達(dá)均顯著高于對照組,而異位內(nèi)膜組與在位內(nèi)膜組VEGF、c-fos表達(dá)比較無統(tǒng)計學(xué)差異,與史淑紅等[12]研究結(jié)論一致,均支持“在位內(nèi)膜決定論”,提示EMs患者在位內(nèi)膜組織血管生成能力較正常子宮內(nèi)膜組織增強(qiáng),一旦逆流進(jìn)入腹腔,很容易產(chǎn)生新生血管,并進(jìn)一步侵襲、發(fā)展,促使異位內(nèi)膜的成功種植和發(fā)展。Rein等[13]研究顯示,異位內(nèi)膜組織VEGF表達(dá)高于在位內(nèi)膜組織,本研究結(jié)果與其不同。可能與本研究采集異位內(nèi)膜標(biāo)本不同有關(guān),新形成的異位內(nèi)膜組織VEGF表達(dá)可能偏高,而陳舊性異位內(nèi)膜組織VEGF表達(dá)可能下降。
研究顯示,雌二醇通過c-fos上調(diào)乳腺癌組織VEGF表達(dá),從而促進(jìn)乳腺癌組織的血管形成[14]。Catar等[15]研究發(fā)現(xiàn),TGF-β1可誘導(dǎo)腹膜間皮細(xì)胞表達(dá)VEGF,電泳遷移率試驗顯示TNF-α或IL-1β與TGF-β1共同作用后,通過c-fos激活VEGF基因啟動子區(qū)域,而小干擾RNA抑制c-fos表達(dá)或c-fos抑制劑則降低VEGF基因啟動子活性,并下調(diào)VEGF表達(dá)水平;提示c-fos是介導(dǎo)TNF-α、IL-1β與TGF-β1促進(jìn)腹膜間皮細(xì)胞表達(dá)VEGF的重要分子。本研究結(jié)果顯示,子宮內(nèi)膜組織中VEGF與c-fos表達(dá)呈正相關(guān),說明c-fos可能通過上調(diào)VEGF表達(dá)而促進(jìn)異位子宮內(nèi)膜組織血管生成,繼而導(dǎo)致EMs的發(fā)生。本研究為探討EMs的發(fā)病機(jī)制提供了新思路,有望為EMs臨床治療提供新靶點(diǎn)。
參考文獻(xiàn):
[1] Missmer AS, Hankinson SE, Spiegelman D, et al. Reproductive history and endometriosis among premenopausal women[J]. Obstet Gynecol, 2004,104(5):965-974.
[2] Bruner-Tran KL, Zhang Z, Eisenberg E, et al. Down-regulation of endometrial matrix metalloproteinase-3 and -7 expression in vitro and therapeutic regression of experimental endometriosis in vivo by a novel nonsteroidal progesterone receptor agonist, tanaproget[J]. J Clin Endocrinol Metab, 2006,91(4):1554-1560.
[3] May K, Becker CM. Endometriosis and angiogenesis[J]. Minerva Ginecol, 2008,60(3):245-254.
[4] Lockwood CJ. Mechanisms of normal and abnormal endometrial bleeding[J]. Menopause, 2011,18(4):408-411.
[5] 徐叢劍,程明軍,黃宇婷,等.子宮內(nèi)膜異位癥病因?qū)W研究進(jìn)展[J].中國實(shí)用婦科與產(chǎn)科雜志,2009,25(9):712-714.
[6] 仝佳麗,郎景和.子宮內(nèi)膜異位癥的在位內(nèi)膜病變研究進(jìn)展[J].現(xiàn)代婦產(chǎn)科進(jìn)展,2010,19(6):465-467.
[7] Xu H, Zhang T, Man GC, et al. Vascular endothelial growth factor C is increased in endometrium and promotes endothelial functions, vascular permeability and angiogenesis and growth of endometriosis[J]. Angiogenesis, 2013,16(3):541-551.
[8] 汪俊元,王安才,曹蘅,等.血管內(nèi)皮生長因子與血管重構(gòu)的關(guān)系及阿托伐他汀干預(yù)作用[J].中國現(xiàn)代醫(yī)學(xué)雜志,2009,19(9):1379.
[9] Wu Ming, Yih Ho, Hong Nerng. The role of cytokines in endometriosis[J]. Am J Reprod Immunol, 2003,49(5):285-296.
[10] Gilabert-Estellés J, Ramón LA, Espana F, et al. Expression of angiogenic factors in endometriosis: relationship to fibrinolytic and metalloproteinase systems[J]. Hum Reprod, 2007,22(8):2120-2127.
[11] John S, Nayvelt I, Hsu HC, et al. Regulation of estrogenic effects by beclin 1 in breast cancer cells[J]. Cancer Res, 2008,68(19):7855-7863.
[12] 史淑紅,高秀娟,李艷芳,等.sflt-1、VEGF在子宮內(nèi)膜異位組織中的表達(dá)及意義[J].山東醫(yī)藥,2014,54(36):30-32.
[13] Rein DT, Schmidt T, Bauerschmitz G, et al. Treatment of endometriosis with a VEGF-targeted conditionally replicative adenovirus[J]. Fertil Steril, 2010,93(8):2687-2694.
[14] De Francesco EM, Pellegrino M, Santolla MF, et al. GPER mediates activation of HIF1α/VEGF signaling by estrogens[J]. Cancer Res, 2014,74(15):4053-4064.
[15] Catar R, Witowski J, Wagner P, et al. The proto-oncogene c-Fos transcriptionally regulates VEGF production during peritoneal inflammation[J]. Kidney Int, 2013,84(6):1119-1128.
中圖分類號:R711.71
文獻(xiàn)標(biāo)志碼:B
文章編號:1002-266X(2016)08-0063-03
doi:10.3969/j.issn.1002-266X.2016.08.025
通信作者:張萍(E-mail: shxinhuazp@163.com)
基金項目:國家自然科學(xué)基金青年科學(xué)基金資助項目(81100410);上海市自然科學(xué)基金資助項目(10ZR1420200)。

