外用皮質類固醇預防放射性皮炎效果的meta分析*
任玉芳,向玉云,唐 清,羊 洋,王國蓉
(1.電子科技大學醫學院,成都 610051;2.四川省腫瘤醫院護理部,成都 610041)
放射性皮炎是放療中常見的不良反應之一,發生率可達95%[1-2],一般在放療開始后2~3周內出現,并在放療結束后持續4~5周[3]。輕度放射性皮炎的表現主要為瘙癢、灼熱、色素沉著,重度表現為潰瘍、壞死、感染等,嚴重的反應甚至會導致放療中斷,增加患者的身心負擔[4]。目前針對放射性皮炎的預防和治療已經存在較多的研究[4-7],但是多數的研究都缺乏有力的支持[8]。外用皮質類固醇(topical corticosteroids,TCS)是指任何含有皮質類固醇的乳膏、噴霧或者溶液等,也是被推薦用于預防和治療放射性皮炎的方法之一,其抗炎作用主要是通過收縮血管、降低毛細血管通透性、抑制白細胞增殖和遷移來實現的[9]。2017年HARUNA等[10]的一項納入919例乳腺癌放療患者的meta分析顯示,TCS使患者濕性脫皮的風險大約降低5倍,但是該研究包括了TCS與其他藥物一起使用的情況,這可能對皮質類固醇的作用產生一定的影響。雖然相關指南也推薦可以使用TCS來預防和治療放射性皮炎,但是該指南的證據總結是基于乳腺癌患者的研究[11],因此TCS在減少其他腫瘤患者放射性皮炎上的有效性不明。本研究系統評價TCS在預防放射性皮炎中的作用,旨在為臨床放射性皮炎的預防提供參考依據。
1 資料與方法
1.1 納入及排除標準
納入標準:(1)隨機對照試驗(RCT);(2)病理學診斷為腫瘤患者且需要接受放療,年齡>18歲;(3)試驗組只以TCS為干預措施,可以是乳膏、噴霧、溶液等,對照組可以采用其他藥物、安慰劑藥膏或空白對照等,干預時間從放療第1天開始使用;(4)主要結局指標為≥3級放射性皮炎或濕性脫皮的發生率,次要結局指標為放射性皮炎的主觀報告癥狀如瘙癢、疼痛等。排除標準:(1)無法獲取全文;(2)非中、英文文獻;(3)干預方法陳述不明確;(4)數據無法提取。
1.2 文獻檢索
采用主題詞加自由詞的方法,檢索中國知網、萬方、維普、PubMed、Cochrane Library、Web of Science、Embase、CINHAL數據庫中的所有相關文獻。英文檢索(“Radiodermatiti*” OR “Radiation Induced Dermatitis” OR “Dermatiti*,Radiation Induced” OR “Radiation-Induced Dermatiti*” OR “Radiation Recall Dermatitis” OR “Dermatiti*,Radiation Recall” OR “Radiation Recall Dermatiti*” OR “Radiation Recall Reaction*” OR “Reaction*,Radiation Recall” OR “Recall Reaction*,Radiation” OR “Acute radiation skin injury”) AND (“Steroid*” OR “corticosteroid” OR “Catatoxic Steroids” OR “Betamethasone” OR “Dexamethasone” OR “Hexadecadrol” OR “Dexasone” OR “Oradexon” OR “Hexadrol” OR “Flumethasone” OR “Fluocinolone Acetonide” OR “Paramethasone” OR “Triamcinolone”);中文檢索(“放射性皮炎”OR“放射性皮膚損傷”OR“急性放射性損傷”)AND(“類固醇”OR“糖皮質激素類”OR“激素類”OR“地塞米松”OR“倍他米松”),時間不限。
1.3 文獻篩選與數據提取
由2名研究者根據納入和排除標準獨立進行文獻閱讀,篩選出符合標準的文獻,再根據需要提取資料信息并核對,如有分歧則請第3位研究者進行裁定。提取的資料信息包括:作者、發表年份、國家、腫瘤類型、樣本量、干預方法、放療的劑量等。
1.4 文獻質量評價
對符合納入標準的文獻,由2名研究者根據系統評價的Cochrane 手冊-5.1.0 版對納入的研究進行獨立評價,評價內容包括:隨機方法、分配隱藏、盲法、結局指標數據的完整性、選擇性報告結果及其他偏倚,對于存在分歧的由第3名研究者進行裁定。
1.5 統計學處理
采用RevMan5.3軟件對數據進行統計分析。當P>0.05,I2<50%時,可認為各研究間具有同質性,選用固定效應模型;P<0.05,I2≥50%時,表示異質性較大,則采用隨機效應模型,亞組分析或敏感性分析判斷異質性來源。計量資料采用加權均數差(MD)及95%CI表示,計數資料采用相對危險度(OR)及95%CI表示。
2 結 果
2.1 文獻檢索結果
共檢索出文獻3 270篇,英文文獻3 167篇,中文文獻103篇,最終符合納入標準的文獻有12篇[12-23]。文獻篩選流程見圖1。
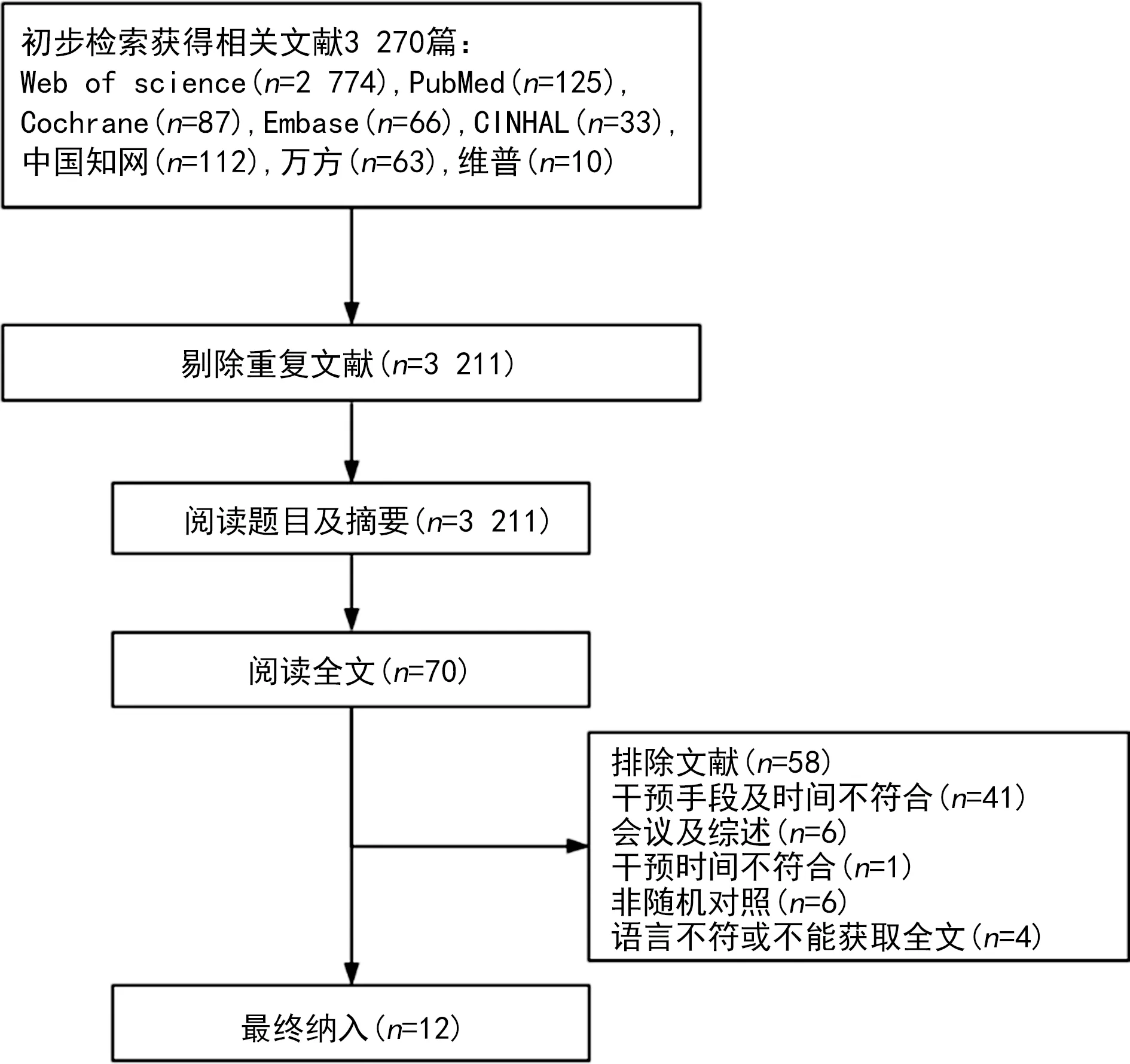
圖1 文獻篩選流程圖
2.2 納入文獻的基本特征及方法學質量評價
納入文獻的基本特征,見表1。納入的12項研究中8項研究[13-18,20,22]介紹了隨機分組的方法,9項研究[13-15,17-18,20-23]使用了分配隱藏,6項研究[13,17-18,20-22]使用了盲法。方法學質量評價見圖2和表2。
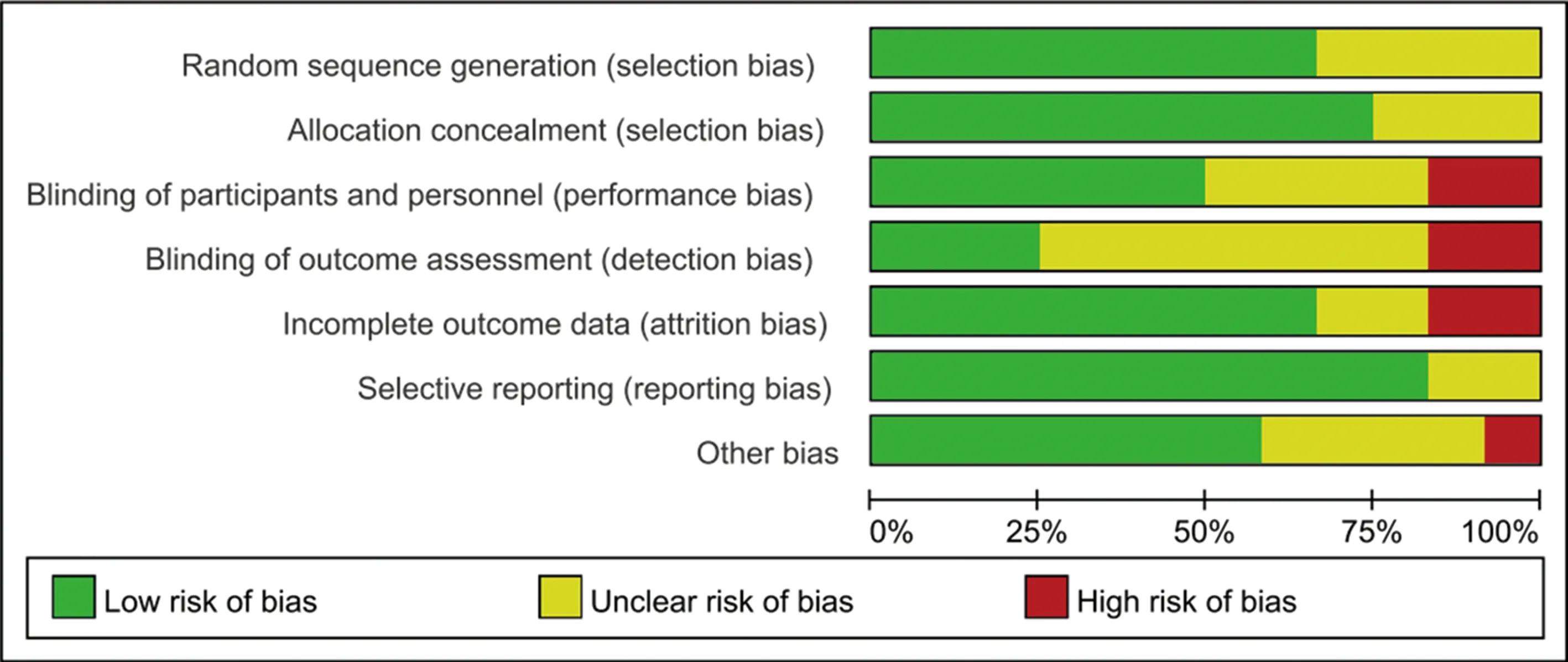
圖2 文獻質量評價結果
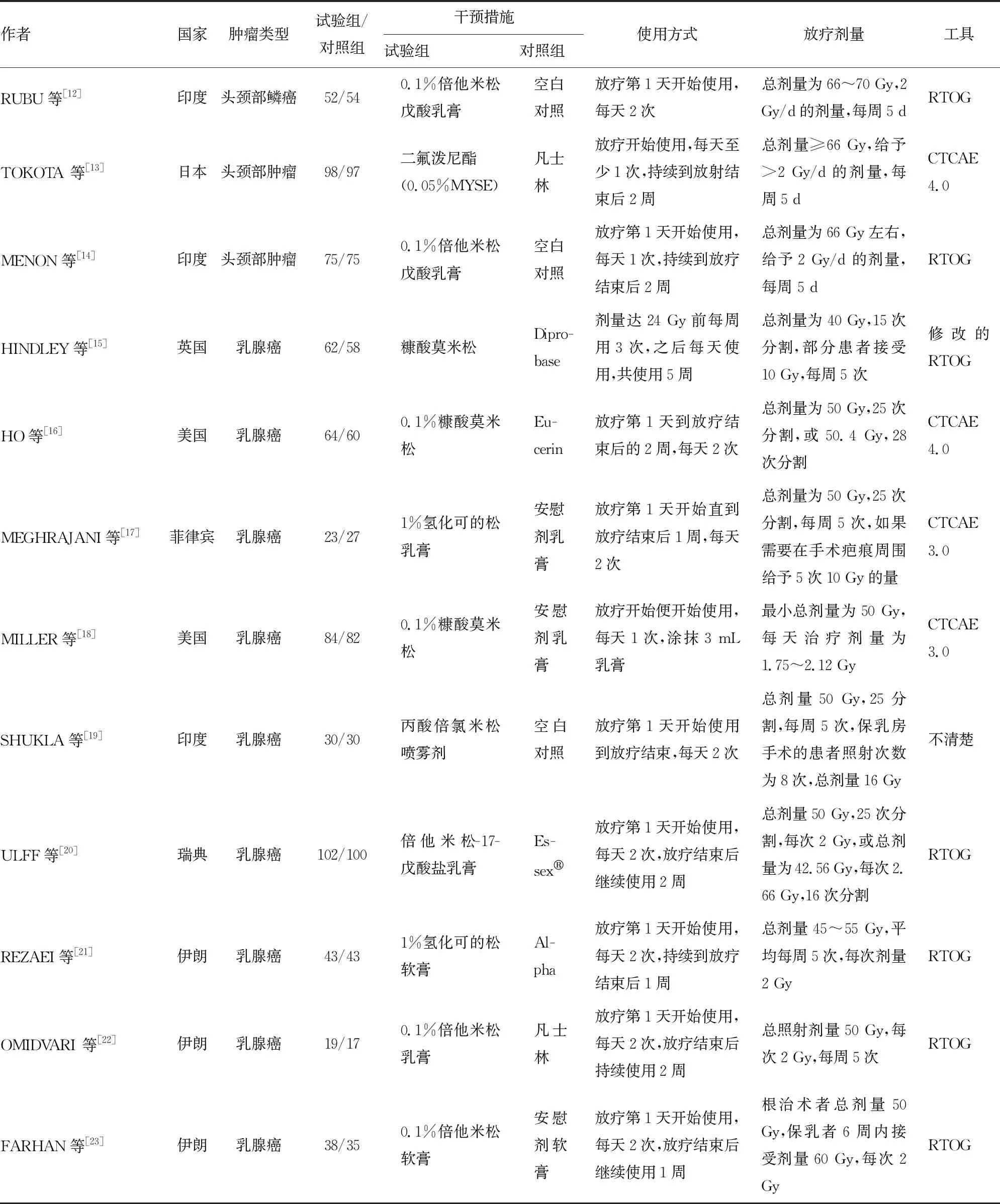
表1 納入研究的基本特征
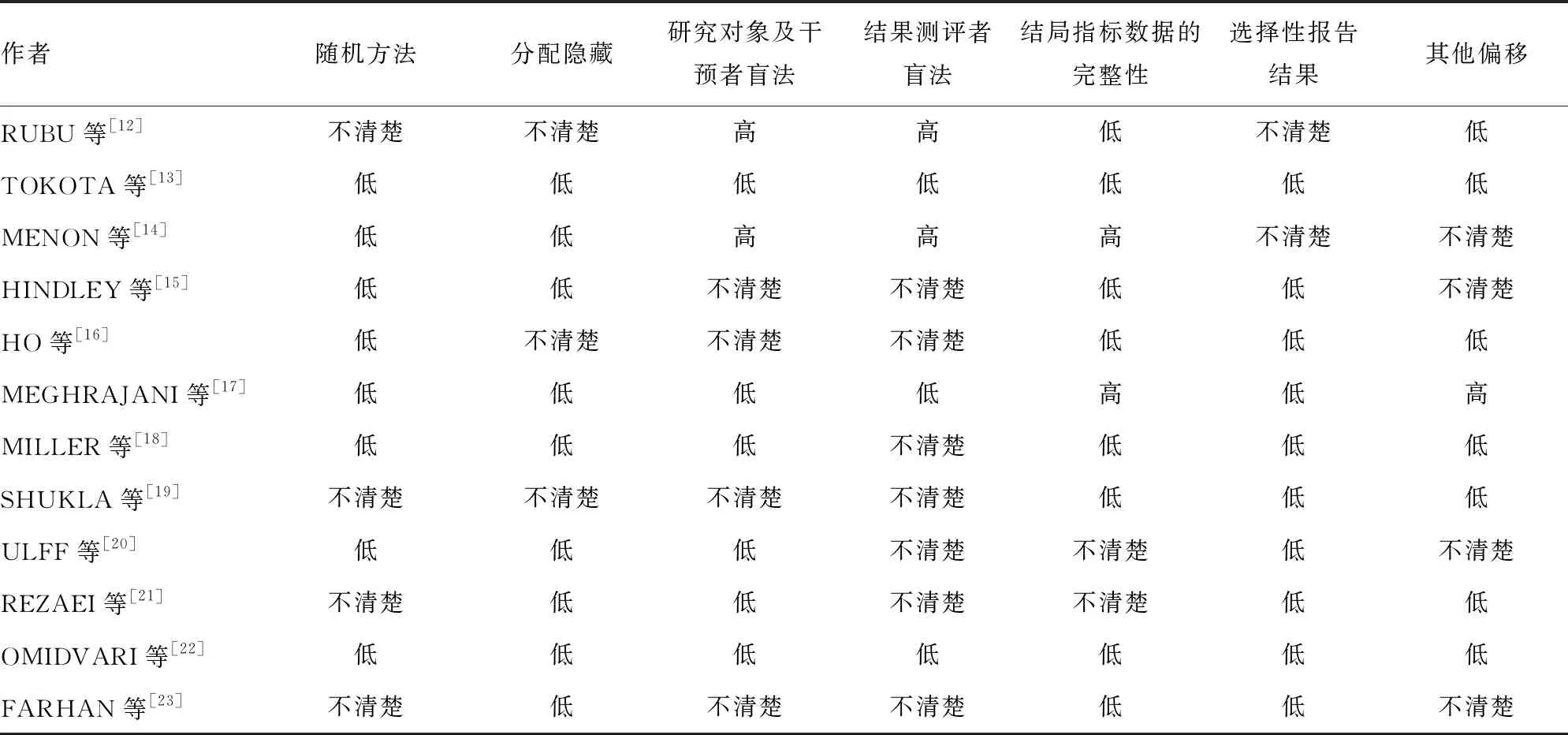
表2 納入文獻的質量評價
2.3 主要結局指標的meta分析
12項研究[12-23]報道了TCS對≥3級放射性皮炎或濕性脫皮的影響,最終共納入1 368例研究對象,試驗組690例,對照組678例。各研究間不存在異質性(P=0.29,I2=16%),選用固定效應模型。結果顯示,與對照組相比,試驗組TCS能改善放療患者≥3級放射性皮炎或濕性脫皮的發生(P<0.05),見表3。
考慮到不同的研究對象可能會對研究結果產生影響,因此進行亞組分析。結果顯示,乳腺癌亞組與對照組比較,≥3級放射性皮炎或濕性脫皮的發生率差異有統計學意義(P<0.05),而頭頸部腫瘤亞組與對照組比較差異無統計學意義(P>0.05),見表3。
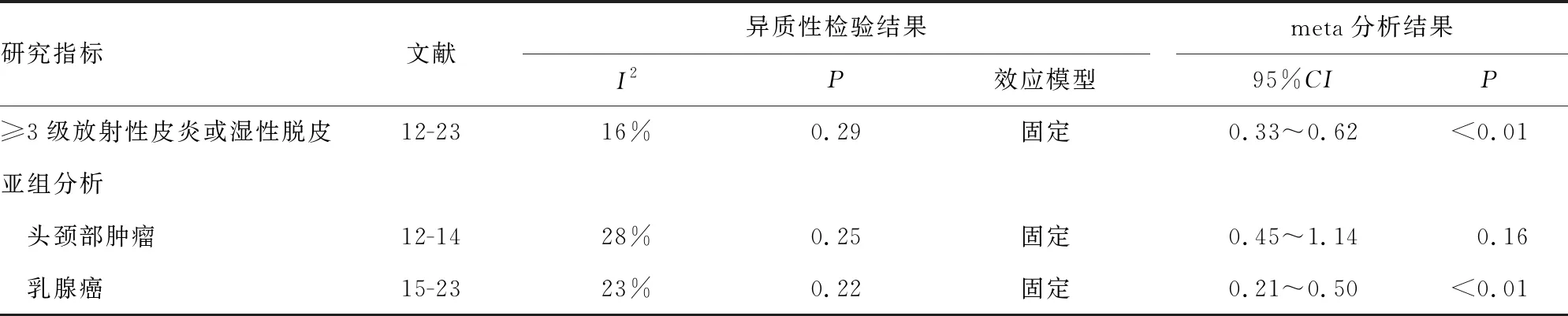
表3 TCS對≥3級放射性皮炎或濕性脫皮發生率的影響
2.4 次要結局指標的結果分析
8項研究[12-14,17-18,20-21,23]報告了患者的主觀癥狀即瘙癢、疼痛和燒灼感。5項研究[17-18,20-21,23]結果表示,與對照組相比,試驗組TCS的使用能減少乳腺癌患者的瘙癢癥狀,但是另外3項[12-14]關于頭頸部腫瘤的研究則表示,TCS并不能減少瘙癢癥狀。同時納入的6項研究[12,14,17-18,21,23]顯示,TCS的使用不能減少放療所引起的疼痛,見表4。

表4 患者主觀癥狀報告
2.5 敏感性分析
對主要觀察指標進行敏感性分析,采用逐一剔除法,重新估計合并效應量。結果顯示,異質性無明顯變化,上述研究結果有較好的穩健性。
2.6 發表偏移
采用漏斗圖對納入的12項研究[12-23]進行發表偏移分析,結果顯示漏斗圖較對稱,初步判斷偏移較小,研究結果較可靠,見圖3。
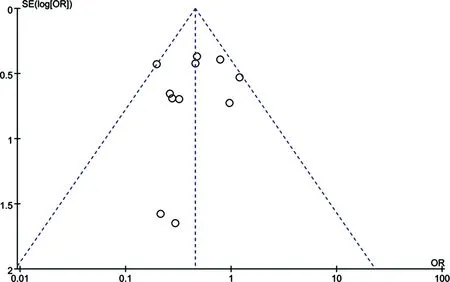
圖3 ≥3級放射性皮炎或濕性脫皮發生的漏斗圖
3 討 論
放射性皮炎的機制是由高能量射線直接損傷人體表皮細胞DNA分子單鏈或雙鏈引起細胞突變,進而引起的一系列皮膚反應和損傷[24-25],其發展過程一般從輕度紅斑到干性脫皮再到濕性脫皮,其中≥3級放射性皮炎是導致放療中斷最主要的原因[26]。本研究結果顯示,預防性使用TCS可以減少腫瘤患者≥3級放射性皮炎或濕性脫皮的發生,此結論與相關研究結果相一致[10,27]。
但是亞組分析結果顯示,TCS不能減少頭頸部腫瘤患者≥3級放射性皮炎或濕性脫皮的發生,此研究結果可能與頭頸部腫瘤患者發生≥3級放射性皮炎的概率較低(≤10%)[28],同時納入的研究對象只有451例有關。但是納入的3項研究中有1項[13]明確表示降低了頭頸部腫瘤患者≥3級放射性皮炎或濕性脫皮的發生(P=0.034),另外2項研究表示雖然沒有降低發生率,但是推遲了發生和進展。以上研究結果提示,TCS在預防頭頸部腫瘤放射性皮炎的發生上可能也有一定作用,但是未來尚需要較多的高質量研究以驗證。通常乳腺癌的照射劑量為50~60 Gy,而頭頸部腫瘤患者的照射劑量在60~70 Gy,且與鉑類化療藥物同步使用,因此這也可能是造成TCS在乳腺癌和頭頸部腫瘤患者中對放射性皮炎效果不同的原因。因此未來的研究需要關注TCS在其他腫瘤中的作用,如宮頸癌、外陰癌[29]等。同時在使用TCS的時候也要考慮長期使用會不會給患者帶來相關的不良反應,雖然納入的研究表示,頭頸部腫瘤放療患者TCS的使用并沒有延緩患者的傷口愈合和增加局部感染的風險,但是缺乏長期的隨訪研究。
放射性皮炎的患者主觀報告癥狀主要包括瘙癢、疼痛和燒灼感[30]。本研究結果顯示,與對照組比較,TCS的使用能減少乳腺癌患者的瘙癢癥狀,此結論與相關研究結果一致[10]。但是其中3項關于頭頸部腫瘤患者[12-14]的研究則顯示,TCS的使用并不能減少瘙癢癥狀,雖然TOMOYA等[13]表示TCS的使用瘙癢癥狀患者的比例從13%下降到8%,但是差異無統計學意義。同時有6項研究[12,14,17-18,21,23]結果表示,與對照組比較,TCS不能減少患者疼痛癥狀,此結論與相關研究一致[10]。但是目前關于患者主觀癥狀的評估工具,除了有視覺模擬量表、放射性皮膚反應評估量表外,還包括CTCAE的相關版本等,因此不能將研究結果納入meta進行量性分析,基于此情況未來尚需要較多的研究以驗證TCS在放射性皮炎主觀報告癥狀中的作用。
本研究最終只納入了頭頸部腫瘤和乳腺癌患者,因此未來需要更多的研究以驗證TCS在減少其他腫瘤患者放射性皮炎發生上的作用;同時,雖然研究表示頭頸部腫瘤患者在放療期間局部長期使用皮質類固醇并沒有增加感染的風險和帶來其他不良反應,但是目前缺乏長期的隨訪研究。

