慢性腎臟病患者腎功能分期、血清胱抑素C及生命質量與睡眠呼吸障礙的相關性研究
鄧祖撫
(雷州市人民醫院腎內科,雷州,524200)
慢性腎臟病(Chronic Kidney Disease,CKD)是全球重點關注的公共健康問題,近年來患病率逐年遞增,其疾病特點為病程長、遷延難愈及病情復雜等。睡眠呼吸障礙(Sleep Disordered Breathing,SDB)是導致CKD睡眠質量變差的常見誘因,其會導致全身炎癥、增加交感神經興奮性、誘導氧化應激反應,從而導致動脈硬化、血管內皮細胞功能障礙等[1]。相關文獻報道CKD因通氣控制不穩、腎小球濾過率降低及咽部水腫等原因極易增加SDB患病率。但目前臨床對于CKD與SDB二者關系的研究文章較少,因此本研究分析CKD患者腎功能分期、血清胱抑素C(Serum Cystatin C,CystC)及生命質量與SDB的相關性,現報道如下。
1 資料與方法
1.1 一般資料 選取2019年5月至2021年2月雷州市人民醫院收治的慢性腎臟病患者134例。其中男76例,女58例,男女比例1.31∶1,年齡26~77歲,平均年齡(51.46±4.32)歲,病程6個月至5年,平均病程(2.75±0.34)年;腎功能分期:CKD1-2期36例、CKD3-4期69例、CKD5期29例;原發疾病:高血壓腎病16例、慢性腎小球腎炎83例、糖尿病腎病17例、梗阻性腎病15例、乙肝相關腎病1例、狼瘡性腎病2例。
1.2 納入標準 1)原發性腎臟病的患者;2)符合美國改善全球腎臟病預后組織(Kidney Disease Improving Global Outcomes,KDIGO)制定的CKD診斷標準的患者[2];3)因自身疾病伴有不同程度疲乏與睡眠障礙的患者;4)未進行血液透析治療的患者;5)依據中華醫學會呼吸病學分會制定的指南,符合SDB診斷的患者。
1.3 排除標準 1)伴有精神類疾病或認知障礙的患者;2)急性腎功能不全的患者;3)合并水腫、胸腹腔積液、營養不良等并發癥的患者;4)長期使用抗失眠藥物的患者;5)臨床資料缺失的患者。
1.4 研究方法 1)腎功能分期標準。1期:伴輕度腎功能損害,且腎小球濾過率(Estimated Glomerular Filtration Rate,eGFR)>90 mL/min。2期:腎功能損害伴eGFR輕度下降,eGFR在60~90 mL/min范圍。3期:中度eGFR下降,eGFR在30~59 mL/min范圍。4期:重度eGFR下降,eGFR在15~29 mL/min范圍。5期:屬于腎衰竭期,eGFR<15 mL/min[3]。其中eGFR計算公式使用簡化腎臟病飲食改良公式(MDRD)。2)CystC檢測。抽取患者晨起空腹狀態下外周靜脈血2 mL,通過離心機離心后獲取上清液,采用免疫比濁法及試劑,通過全自動生化分析儀(型號:cobas e411)檢測。3)生命質量評價。采用中文版SF-36生命質量(Quality of Life,QOL)評分量表進行評估,量表由浙江大學翻譯編制而成,含4個維度,即軀體健康、心理疏導、角色功能、社會功能,36個條目,總分100分制。評分轉換公式:每維度評分=(實際得分-理論最低得分)/(理論最高得分-理論最低得分)×100,后采用Excel計算SF-36的QOL總分,總分越高表示生命質量越好[4]。4)睡眠評價與監測。采用Epworth嗜睡量表(Epworth Sleepiness Scale,ESS)評價嗜睡癥狀,總分為24分,當ESS評分≥10分時表示患者伴有日間嗜睡過多(Excessive Daytime Sleepiness,EDS)。通過便攜式睡眠監測儀(Res Med,澳大利亞,型號:Apnea-Link型)監測夜間>7 h的睡眠情況。監測前需在24 h內不可服用安眠類藥物或影響睡眠的食物。監測指標:呼吸暫停低通氣指數(Apnea Hypopnea Index,AHI)、氧減指數(Oxygen Desaturation Index,ODI)、低通氣指數、夜間低氧血癥發生次數。
1.5 觀察指標 1)CKD患者腎功能不同分期血清CystC水平、ESS評分、EDS發生率及睡眠呼吸相關指標分析。2)分析CKD患者腎功能分期、CystC及生命質量與SDB的相關性。
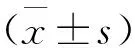
2 結果
2.1 CKD患者腎功能不同分期相關指標分析 CKD 5期患者血清CystC水平、ESS評分、EDS發生率及睡眠呼吸相關指標水平均高于CKD1~2期與CKD3~4期,而QOL評分低于CKD1~2期與CKD3~4期,差異均有統計學意義(均P<0.05)。見表1。

表1 CKD患者腎功能不同分期相關指標分析
2.2 CKD腎功能分期、CystC及QOL評分與SDB指標的相關性分析 CKD腎功能分期、血清CystC與SDB指標(ESS評分、AHI≥15次/h、低通氣指數、夜間低氧血癥發生率)正相關(均P<0.05);CKD患者QOL評分與SDB指標(ESS評分、AHI≥15次/h、低通氣指數、夜間低氧血癥發生率)負相關(均P<0.05)。見表2。

表2 CKD腎功能分期、CystC及QOL評分與SDB指標的相關性
3 討論
CKD患者因通氣控制不穩、咽部水腫等體征增加睡眠呼吸障礙的患病率。且調查發現CKD患者多數伴有睡眠呼吸暫停、夜間低氧血癥,但實際分析發現多數患者無典型癥狀,如EDS、夜間鼾聲及呼吸暫停、晨起頭痛等。
本研究首先分析CKD患者腎功能不同分期相關指標,結果顯示,CKD5期患者血清CystC水平、ESS評分、EDS發生率及睡眠呼吸相關指標水平均高于CKD1~2期與CKD3~4期,而QOL評分低于CKD1~2期與CKD3~4期(均P<0.05),證實CKD5期與CKD3~4期患者的SDB發病率與疾病嚴重程度均高于CKD1~2期患者,且CKD5期患者更易于發生嚴重的夜間低氧血癥與SDB,隨著CKD患者腎功能的不斷下降,其發生SDB的風險性增加。相關文獻報道CKD睡眠呼吸障礙癥狀越嚴重,會進一步惡化腎功能[4]。CKD主要發病機制是腎小球高濾過與腎小管慢性缺氧假說,其中以腎小管慢性缺氧假說更為重要。夜間低氧血癥會導致CKD患者腎髓質基礎偏低的供氧與高氧耗需求間出現失衡現象,致使腎臟對于缺氧情況異常敏感,因而夜間低氧血癥發生率升高有增加CKD疾病嚴重程度的風險。血清CystC可在幾乎所有有核細胞中以恒定速度持續轉錄與表達,無組織特性,因而CystC能在體內以恒定速度產生,且不受性別、年齡、體質量與炎癥狀態等的影響[5]。血清CystC是反映eGFR的重要內源性指標,其分子量低,可自由通過腎小球濾過膜,后由近端小管完全重吸收與分解,但腎小管不分泌CystC,其含量主要由eGFR決定,通過檢測血清CystC濃度可敏感、準確而又簡便可靠地評價腎小球濾過率,利于發現CKD患者的早期腎損害,評估腎損傷程度[6]。當CKD患者睡眠質量持續下降,且伴有日間嗜睡癥狀及夜間低氧血癥時,腎功能逐步惡化,殘余腎單位降低,減弱腎代償能力,導致腎小球濾過率、腎小管重吸收力減低,極有可能誘發心功能不全、高血壓與睡眠呼吸障,從而降低生命質量[7]。相關文獻報道,咽部橫截面積每縮小6%,患者AHI會增幅73%,進一步證實咽部狹窄或阻塞會增加睡眠呼吸障礙的發病率[8]。CKD患者的咽部水腫與患者全身體液的負荷過重密切相關,亦與尿毒癥患者咽部肌肉功能不全或神經功能密切相關,研究發現,阻塞型睡眠呼吸暫停患者的體位改變會引起下肢體液轉移,且在夜間平臥時體液會重新分布到患者頭頸部,集聚在上呼吸道的軟組織周圍,致使上呼吸道出現塌陷,增加睡眠呼吸暫停的風險性,而患者呼吸道肌肉的神經功能損傷則會進一步加重上述過程,因而體液從腿部轉移至頸部或肺部會導致體液負荷過重,增加阻塞型睡眠呼吸暫停、中樞型睡眠呼吸暫停的發病風險[9]。再者是CKD患者存在通氣控制不穩定的情況,分析發現,CKD5期患者機體中存在代謝性酸中毒或尿毒素排泄障礙,會增加其呼吸控制失衡風險性,化學反射效應增強,可能與“環路增益”理論密切相關。
綜上所述,多數CKD患者伴有SDB,且隨腎功能降低、血清CystC增加SDB患病風險增加,生命質量及睡眠質量下降,伴有日間嗜睡癥狀。

