基于網絡藥理學探析鬼箭羽治療2 型糖尿病潛在分子機制
劉 敏,邱現良,陳 秋
(成都中醫藥大學附屬醫院,四川成都 610075)
糖尿病(diabetes mellitus,DM)是一組以持續高血糖為特征的慢性代謝性疾病,可導致腎臟、眼底、心血管及神經等多個器官和組織的慢性損害及功能障礙。國際糖尿病聯盟公布的數據顯示,糖尿病已成為繼心血管疾病和癌癥之后威脅人類健康的第三大殺手[1]。據WHO 最新統計,2012 年DM直接造成150 萬人死亡,2014 年全球約有4.22 億(每11 人中就有1 人)糖尿病患者,是1980 年的14 倍,預計到2030 年糖尿病患者將達到6 億[2]。抗糖尿病藥物如雙胍類、磺酰脲類等在臨床被廣泛應用,但由于“一個靶點,一種藥物”的作用機制,它們可能具有相似的副作用,如體重增加、心血管疾病、低血糖和胃腸道反應等[3]。與合成藥物相比,中藥具有多成分、多靶點聯合或協同作用的特點,在DM 治療中發揮了重要作用[4]。
隨著生物信息學的快速發展,整合網絡生物學和藥理學的網絡藥理學被認為是一種有前景的更具成本效益的藥物開發方法[5]。與傳統的“一基因、一藥、一病”模式相比,網絡藥理學注重對疾病的“多靶點、多成分”治療。它可以揭示多組分和多靶標之間潛在的復雜關系,并提供了系統水平的方法來理解疾病的發病機制[6],而通過高通量篩選和生物信息學技術,還可建立可行的“藥物-靶點-疾病”網絡模型[7],其研究方法的整體性、系統性特點與中醫理論中的整體觀和辨證原則不謀而合。據報道網絡藥理學有多種應用,如中藥成分靶標/疾病基因預測、網絡平衡調控、協同成分對和活性成分組的解析[8-10]。因此,包括網絡藥理學和網絡醫學在內的基于網絡的方法得到了越來越多的發展和應用。
本研究主要基于數據挖掘分析國醫大師張發榮教授的用藥經驗,張老在臨證治療2 型糖尿病時常于辨治方中加用中藥鬼箭羽,每每取得良好的臨床療效。鬼箭羽始載于《神農本草經》,列為中品,其干有直羽如持箭予自衛之狀,故又名衛矛。鬼箭羽味苦,性寒,入足厥陰經,具破血通經、散瘀止痛、解毒殺蟲之功,主治經閉、癥瘕、產后瘀滯腹痛、蟲積腹痛等癥[11]。現代藥理學研究表明其具有降血糖、調血脂、抗動脈粥樣硬化、調節免疫等作用,近年來臨床多用于治療糖尿病、高脂血癥、動脈硬化及腎臟疾病等[12-15],效果顯著。因此,本研究應用網絡藥理學研究方法,對鬼箭羽活性成分及作用靶點進行篩選,研究其多成分-多靶點-多通路作用模式,以探索鬼箭羽治療2 型糖尿病的潛在分子機制。
1 資料與方法
1.1 鬼箭羽主要活性成分及靶點預測
通過檢索相關文獻和中藥系統藥理學數據庫與分析平臺(TCMSP)獲得鬼箭羽主要活性成分,根據外源化學物在人體內吸收、分布、代謝和排泄的動態變化規律,設置口服生物利用度(OB)≥30%、類藥性(DL)≥0.18 及小腸上皮細胞滲透率(Caco-2)≥-0.04 為篩選閾值。同時在TCMSP 數據庫提取鬼箭羽所有活性成分的潛在靶點數據,應用Perl(version 5.28.1)篩選出鬼箭羽主要活性成分的對應靶點,為方便后續分析,通過UniProt 數據庫在靶點全稱后注釋其基因名(Gene Symbol)。
1.2 “藥物-疾病”共同作用靶點預測
以“Diabetes Mellitus,Type 2”為關鍵詞分別檢索人類基因數據庫(GeneCards)和在線人類孟德爾遺傳數據庫(OMIM),建立與2 型糖尿病相關的靶點數據集。運用R(version 3.6.3)軟件中“VennDiagram”包,對鬼箭羽主要活性成分對應的靶點和2 型糖尿病的靶點數據集進行匹配重合,整合得到藥物和疾病的共同作用靶點進行后續分析。
1.3 “藥物-成分-靶點-疾病”網絡構建與分析
應用Perl project 將獲取的鬼箭羽主要活性成分的作用靶點和“藥物-疾病”的共同作用靶點進行相互映射,可獲得網絡中每個節點的屬性(type.txt),節點之間的連線關系(network.txt)以及藥物活性成分列表(molLists.txt)。將以上文件輸入Cytoscape(version 3.7.2),以 構 建“藥 物-成 分-靶 點-疾病”關系的可視化網絡圖,其中節點的屬性包括藥物、活性成分、共同作用靶點和疾病,若經預測成分與靶點之間存在對應關系,則在網絡中以邊連接。
1.4 “藥物-疾病”蛋白互作網絡的構建
將鬼箭羽和T2DM 的靶點基因交集上傳至STRING 數據庫(version 11.0),限定物種為人(Homo sapiens),設置最低要求的相互作用評分為highest confidence(0.900),隱去離散的節點,以獲得鬼箭羽治療T2DM 的蛋白質與蛋白質相互作用網絡圖(Protein-Protein Interaction,PPI),并 導 出string-interaction.tsv,基于PPI 網絡中每個基因連接節點的數目(count 值)篩選出鬼箭羽治療T2DM 的關鍵靶點。
1.5 GO 富集分析及KEGG 信號通路分析
應用R 中“org.Hs.eg.db(version 3.10.0)”包,將鬼箭羽與T2DM 共同作用靶點的基因Symbol 轉換為基因ID,再安裝“Bioconductor(version 3.10)”包對其進行GO(Gene Ontology)生物學過程富集分析和KEGG(Kyoto Encyclopedia of Genes and Genomes)信號通路分析,顯著性閾值設為P<0.05,得到鬼箭羽治療T2DM 靶點的主要生物過程和信號通路。GO 富集分析的結果將以柱狀圖和氣泡圖的形式展示,并提供KEGG 通路富集分析的柱狀圖及信號通路圖結果。
2 結果
2.1 藥物-疾病交集靶點預測結果
根據方法部分所述,以“鬼箭羽”為關鍵詞檢索相關文獻及TCMSP 數據庫,共獲得8 種滿足篩選條件的鬼箭羽活性成分和284 個作用靶點,其中作用靶點數目較多的活性成分為槲皮素(154 個)、山奈酚(63 個)和β-谷甾醇(38 個),見表1。以“Diabetes Mellitus,Type 2”分別檢索GeneCards 數據庫和OMIM 數據庫,共獲得與T2DM 相關的疾病靶點信息11 750 個,將上述鬼箭羽主要活性成分的作用靶點與T2DM 的疾病靶點數據庫取交集,最終得到154 個共同作用靶點。

表1 鬼箭羽主要活性成分數據信息Tab 1 Data information of main active ingredients of Euonymus alatus
2.2 “藥物-成分-靶點-疾病”網絡圖
基于方法部分所述,通過Cytoscape 軟件對“藥物-成分-靶點-疾病”關系進行可視化,可直觀得出鬼箭羽主要成分、T2DM 和作用靶點之間的網絡關系。其中紅色和藍色多邊形分別代表疾病和藥物名稱,紫色三角形代表鬼箭羽的主要活性成分,綠色圓形代表鬼箭羽和T2DM 的共同作用靶點,連線代表藥物、藥物活性成分、疾病及作用靶點之間的相互關系,見圖1。結果顯示,鬼箭羽的同一活性成分可調控多個靶點,同一靶點與多個活性成分相作用,充分體現了鬼箭羽在治療T2DM 多成分、多靶點的作用特點。
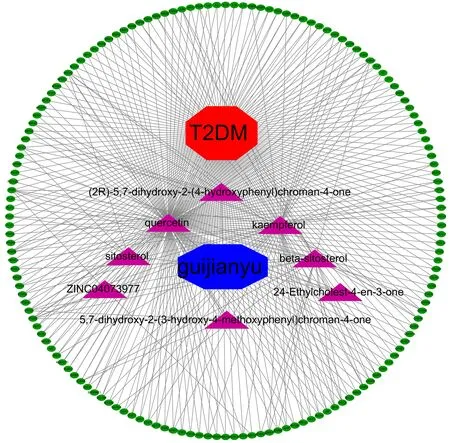
圖1 鬼箭羽的“藥物-成分-靶點-疾病”網絡Fig 1 Drug-ingredient-target-disease network of Euonymus alatus
2.3 PPI 網絡的構建與分析
將鬼箭羽主要活性成分和T2DM 的交集靶點上傳至STRING 數據庫,構建蛋白與蛋白相互作用關系網絡圖(PPI),見圖2。經計算,PPI 網絡中有154 個作用節點,490 條相互作用連線,圖中每個節點(Nodes)代表由單個蛋白編碼基因位點產生的多個蛋白,節點之間的連線(Edges)代表蛋白互作關系,連線的不同顏色則表示不同的互作證據。圖3為基于count 值選取排名Top30 的蛋白質節點,主要包括Jun 原癌基因(JUN)、絲裂原活化蛋白激酶(MAPK1、MAPK8)、絲 氨 酸/蘇 氨 酸 蛋 白 激 酶(AKT1)、V-Rel 網狀內皮增生病毒癌基因同源物A(RELA)、白細胞介素(IL6、CXCL8)、表皮生長因子受體(EGFR)、雌激素受體1(ESR1)等。蛋白連接節點的數目越多代表其在整個PPI 網絡中互作關系越頻繁,提示該蛋白可能是鬼箭羽治療T2DM 的核心調控靶點。

圖2 “鬼箭羽-疾病”靶點相互作用網絡Fig 2 Target interaction network of“Euonymus alatus-disease”

圖3 鬼箭羽治療T2DM 的核心調控靶點Fig 3 Key regulatory targets of Euonymus alatus in treating T2DM
2.4 GO 富集分析
對藥物-疾病的共同作用靶點進行GO 功能富集分析,共富集到153 條生物過程(P<0.05)。根據差異基因在GO term 富集的顯著性程度(P值),篩選得到前20 條主要生物過程,如圖4,其中顏色越紅表示富集的顯著性越高(P值越小)。這些生物過程主要包括核受體活性、轉錄因子活性直接配體調節序列特異性DNA 結合、類固醇激素受體活性、細胞因子受體結合、細胞因子活性、DNA 結合轉錄激活子活性、RNA 聚合酶Ⅱ特異性、血紅素結合等。圖5 所示氣泡圖可顯示富集基因數占上傳基因總數的比例(Gene Ratio),圓點越大表示占比越大,P值越小則顏色越紅,其中比例較大的為DNA 結合轉錄激活子活性、RNA 聚合酶Ⅱ特異性、細胞因子受體結合、受體配體活性。表明鬼箭羽治療T2DM 可能是通過參與以上的生物學調控過程發揮作用。
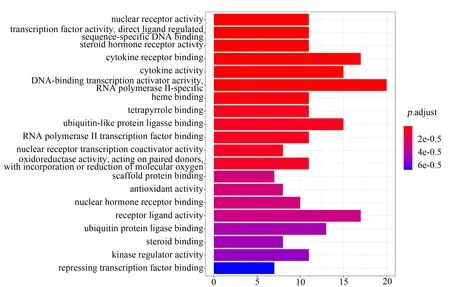
圖4 潛在靶點生物學過程的GO 分析Fig 4 GO analysis of potential targets in biological processes
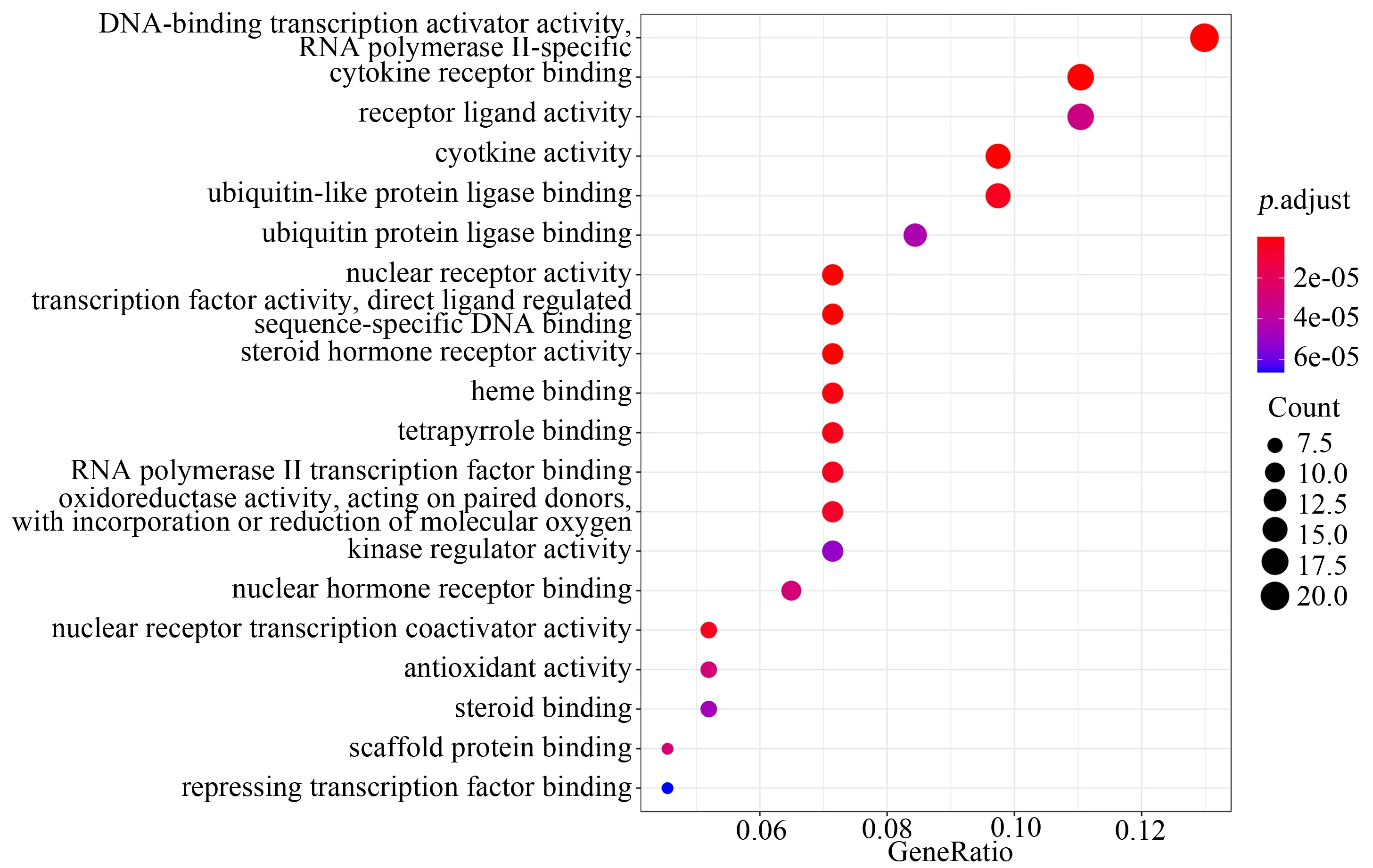
圖5 GO 生物功能富集分析的氣泡圖Fig 5 Bubble plot for GO biofunctional enrichment analysis
2.5 KEGG 信號通路富集分析
通過R 中“clusterProfiler”包對藥物-疾病交集靶點進行通路富集分析,共富集到156 條顯著通路(P<0.05),將P值由小到大排列篩選出前20 條主要信號通路,如圖6。通路主要富集在糖尿病并發癥中的AGE-RAGE 信號通路、流體剪切應力與動脈粥樣硬化、乙型肝炎、前列腺癌、卡波西肉瘤相關皰疹病毒感染、膀胱癌、TNF 信號通路、胰腺癌、IL-17 信號通路、丙型肝炎、人巨細胞病毒感染、肺癌、HIF-1 信號通路、甲型流感病毒、內分泌抵抗等,并與PI3K-Akt 信號通路、NF-κB 信號通路、胰島素抵抗、AMPK 信號通路、Ⅰ型糖尿病、Ⅱ型糖尿病、胰島素信號通路、脂肪細胞中脂肪分解的調節等有相關性,表明鬼箭羽活性成分可作用于不同的信號通路綜合發揮治療T2DM 的作用。圖7 標注了鬼箭羽主要活性成分在AGE-RAGE 信號通路中的作用靶點。

圖6 潛在靶點的KEGG 信號通路富集分析Fig 6 KEGG signaling pathway enrichment analysis of potential targets

圖7 鬼箭羽在AGE-RAGE 信號通路中的作用靶點Fig 7 Targets of Euonymus alatus in AGE-RAGE signaling pathway
3 討論
糖尿病可歸屬于中醫“消渴”或“消癉”范疇。《靈樞·五變》曰“怒則氣上逆,胸中蓄積,血氣逆留,髖皮充肌,血脈不行,轉而為熱,熱則消肌膚,故為消癉”,明確指出了消渴與瘀血之間的關系。《本草備要》載鬼箭羽“苦寒,破陳血,通經”,清楊時泰在《本草述鉤元》中謂本品“大抵其功精專于血分”。國醫大師張發榮教授認為消渴病“陰虛為本,燥熱為標,瘀血為患”,而鬼箭羽味苦善于堅陰,性寒能入血,又長于清解陰分之燥熱,對消渴病之陰虛燥熱者,每于辨治方中配伍本品15~30 g,能清熱止渴,降低血糖和尿糖,屢獲良效。且鬼箭羽具破血散瘀之功,對糖尿病并發心腦血管和腎臟、視網膜及神經系統等病變,可改善血液循環,促進新陳代謝,正所謂“通經隧、行瘀血、布津氣”,亦可使方中補益藥活潑暢榮而不壅膩,實為治療消渴病之上選藥品。
本研究中發現鬼箭羽作用于T2DM 的主要活性成分有8 個,其中作用靶點數目較多的成分為槲皮素、山奈酚和β-谷甾醇。在對糖尿病大鼠的試驗中顯示,研究劑量的槲皮素可顯著逆轉高血糖,降低糖化血紅蛋白和肝糖原水平,改善胰腺抗氧化狀態,還能預防和治療慢性高血糖時血紅蛋白糖基化相關的繼發性并發癥[16],槲皮素還可通過減少iNOS 表達、降低NO 水平及NF-κB 易位抑制等起到保護 胰 島β 細 胞 的 作 用[17-19]。山 奈 酚 可 激 活cAMP/PKA 通路介導產生促胰島素分泌作用,還可上調Akt、Bcl-2 蛋 白 的 表 達 和 降 低caspase-3 活 性,保 護胰島β 細胞不受高血糖誘導的凋亡和功能障礙的影響[20]。β-谷甾醇可增強糖酵解活性,刺激殘余β 細胞的胰島素分泌,增加糖尿病大鼠的肝葡萄糖利用,從而發揮降血糖作用[21]。此外,基于PPI 網絡分析得出鬼箭羽主要活性成分有JUN、MAPK1、AKT1、RELA、IL6、MAPK8、EGFR、ESR1、FOS、CXCL8 等多個作用靶點,表明鬼箭羽治療T2DM具有多成分、多靶點的特點。
GO 富集分析得到153 條生物過程,其中富集結果最顯著的是核受體活性(nuclear receptor activity)。核受體在包括發育和代謝穩態在內的關鍵過程中發揮重要的調節作用,也被稱為代謝性核受體。PPARs(亞 型α、β 和γ)是Ⅱ型 核 受 體,在 脂 質 代謝[22]和脂肪細胞分化[23]以及胰島素反應[24]中發揮重要作用,其中PPARα 活化可導致肝臟和肌肉中脂肪酸氧化增加[25,26],而PPARγ 活化主要在脂肪組織中增加胰島素敏感性[27],這兩種途徑使PPARs 在血脂異常和糖尿病的治療中成為重要靶點。研究最多的PPARs 合成配體是噻唑烷二酮類藥物(TZD),這類藥物甚至在了解其作用機制之前就用于增加胰島素敏感性,研究發現TZD 可通過活化PPARγ 降低胰島素抵抗、改變脂肪細胞分化并誘導脂蛋白脂酶(LPL)合成[28-30],十多年來被有效地用于2 型糖尿病的治療。貝特類藥物通過肝臟中PPARα 介 導 的LPL 活 化 增 加 甘 油 三 酯 脂 解[31],PPARα 的活化還可通過參與脂蛋白代謝中靶基因的轉錄變化增加高密度脂蛋白(HDL)水平[32],這些作用共同改善了致動脈粥樣硬化脂蛋白平衡,降低了心血管疾病的發病率。
KEGG 信號通路分析中富集結果最顯著的是AGE-RAGE 信號通路。研究表明,晚期糖基化終末產物(AGEs)與其受體(RAGE)結合后可啟動一系列受體后信號轉導通路,從多個途徑參與糖尿病慢性并發癥的發生和發展[33]。腎臟在持續高血糖環 境 中 產 生 大 量AGEs 上 調RAGE 表 達,RAGE 的過表達可導致活性氧(ROS)的產生并使炎癥加劇,從而促進腎臟慢性炎癥狀態的建立,最終導致腎臟結構和功能逐漸喪失[34]。Burke 等[35]對猝死于心血管并發癥的糖尿病患者的研究中發現,其冠狀動脈斑塊中RAGE 和EN-RAGE 的表達明顯高于非糖尿病患者,RAGE/EN-RAGE 的表達可能進一步損害細胞存活并促進斑塊的不穩定。AGEs-RAGE 相互作用還可引起外周神經中致炎基因的轉錄和氧化應激反應的發生,激活NF-κB,進而促使糖尿病周圍神經病變的發生[36],更有研究顯示,在糖耐量減低階段AGE/RAGE/NF-κB 即已活化[37]。因此,AGE-RAGE 通路可能是鬼箭羽治療2 型糖尿病及預防相關并發癥的重要機制之一。其次根據KEGG 富集分析結果,推測鬼箭羽還具有良好的抗病毒、抗腫瘤及免疫調節等作用,可進一步拓展其臨床應用及相關分子機制研究。
綜上所述,本研究首次應用網絡藥理學方法對鬼箭羽治療T2DM 的潛在分子機制進行了探索,篩選出鬼箭羽8 種主要活性成分及154 個藥物-疾病共同作用靶點,并構建了“藥物-成分-靶點-疾病”交互網絡圖,通過富集分析,發現了153 個生物過程和156 條信號通路直接或間接參與治療T2DM 及相關并發癥,體現了中藥多成分、多靶點、多途徑協同作用的特點。本研究的局限性在于,網絡藥理學是基于大量數據庫所做的預測,數據搜集的全面性及活性成分篩選標準的差異會對研究結果有一定影響,因此后續還需進一步過濾藥物活性成分,開展體內或體外實驗,并完善中藥復方成分的質量評價,為鬼箭羽的臨床應用提供科學實用的證據支持,本研究可為后續相關研究提供基礎。

