成人髓母細胞瘤診斷和治療研究進展☆
劉裕 肖爵賢 桂詩凱 程天祥 程祖玨
髓母細胞瘤(medulloblastoma,MB)是一種惡性原發性中樞神經系統腫瘤,好發于兒童,成人較為少見,成人MB每年發病率僅有6/1000萬[1]。臨床醫生常將其忽視,誤診為室管膜瘤、血管母細胞瘤和膠質瘤等其他疾病。成人MB的治療包括手術切除腫瘤,術后輔以全腦全脊髓放療(craniospinal irradiation,CSI)聯合后顱窩加強放療,同時予以化療,5年生存率為70%~80%[2]。目前對于成人MB放療、化療方案尚無統一的標準,預后影響因素也存在爭議。本文針對成人MB的診斷、治療以及預后影響因素的最新進展作一綜述。
1 分型與分期
1.1 MB分型2021年WHO第五版中樞神經系統腫瘤分類(WHO CNS5)更新了MB的組織學分型和分子分型,對MB的診斷提供了新的指導。MB的組織學類型分為:經典型(classi,CL)、促結締組織增生/結節型髓母細胞瘤(desmoplastic/nodular,DN)、廣泛的結節型髓母細胞瘤(medulloblastoma with extensive nodularity,MBEN)和大細胞/間變型髓母細胞瘤(large cell/anaplastic,LC/A)[3]。WHO CNS5將2016年版中的group3和group4歸為一組,將SHH活化型分裂為TP53野生型以及TP53突變型兩組。WHO CNS5更新的MB分子分型為:髓母細胞瘤,WNT活化型(medulloblastoma,WNT-activated);髓母細胞瘤,SHH活化和TP53野生型(medulloblastoma,SHH-activated and TP53-wildtype);髓母細胞瘤,SHH活化和TP53突變型(medulloblastoma,SHH-activated and TP53-mutant);髓母細胞瘤,非WNT/非SHH活化型(medulloblastoma,non-WNT and non-SHH)[3]。
1.2 MB分期1969年CHANG等根據腫瘤大小和轉移情況制訂MB的TM分期,并被廣泛的應用[4]。CHANG氏分期系統主要借鑒于其他腫瘤的TMN分期,其中T分期描述腫瘤侵犯情況,M分期描述腫瘤的播散轉移、腦脊液浸潤和遠處轉移情況,見表1。目前主要依據CHANG TM分期將MB分為標危組和高危組,其中標危組為T1~T3aM0,高危組為T3bM1~M4、T4M1~M4。
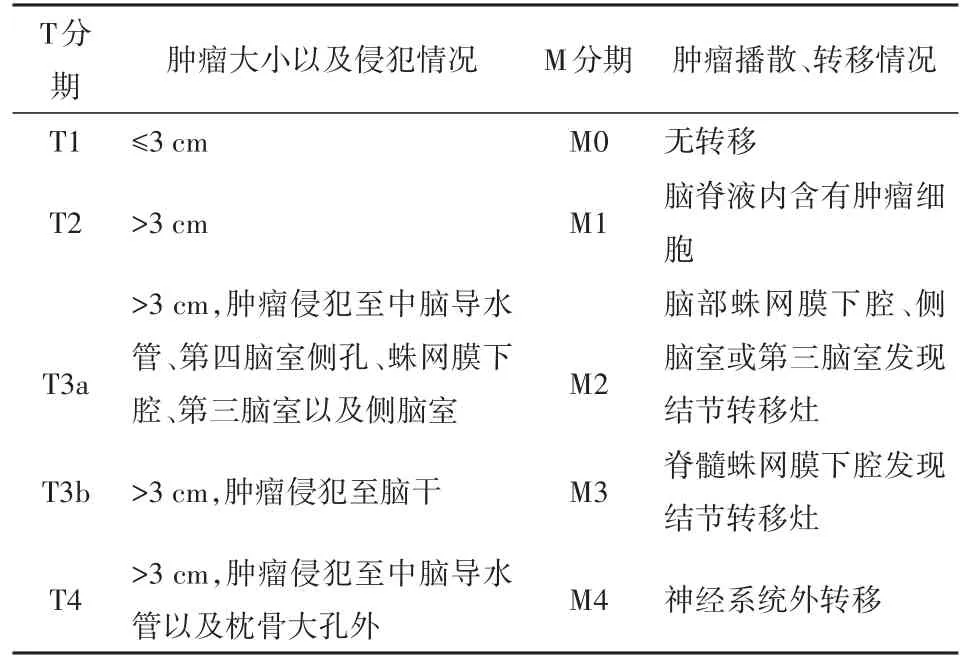
表1 CHANG氏分期
2 診斷
2.1 基因篩查MB發病與某些遺傳性癌癥易感基因存在著密切聯系。WASZAK等[5]發現APC、BRCA2、PALB2、PTCH1、SUFU和TP53等基因在MB發生發展中起重要作用,尤其在WNT活化型及SHH活化型表現更為明顯。相關研究表明TP53、PTCH1和SUFU基因突變患者更容易發生SHH活化型髓母細胞瘤[6]。
2.2 臨床癥狀成人MB好發于后顱窩,潛伏期1~18個月(平均7個月),常表現為小腦功能障礙、腦積水相應表現及顱高壓癥狀[7]。小腦功能障礙的臨床癥狀及體征可能因病變位置而不同[8]。中線區小腦MB多為串聯步態受損和閉目難立征陽性;小腦半球MB則多表現快速輪替運動障礙、指鼻試驗以及跟膝脛試驗陽性體征[8]。由于成人顱縫已經閉合,成人MB起病更加危急,顱高壓癥狀更加明顯。因此,大多數成人患者由于頭痛、惡心嘔吐或意識障礙等顱高壓相關癥狀而就診。腦神經受累的臨床癥狀也常出現,如外展神經受損導致復視,這可能是由于腦神經直接受累或者顱內壓升高所導致[8]。MB也可以通過蛛網膜下腔播散轉移,多數轉移至椎管內以及大腦表面,極少數轉移至淋巴結、骨、肺和肝臟,從而導致相應臨床癥狀[2,8-9]。
2.3 影像學表現顱腦CT和MRI是診斷MB常用影像學方法。成人MB多起源于小腦半球以及橋小腦角區,其顱腦CT多表現為小腦半球或橋小腦角區的高密度或混雜密度影,周圍環繞著低密度水腫帶,增強掃描腫瘤呈均勻強化[10]。顱腦MRI常表現為小腦半球處邊緣清晰的類圓形占位病變,多伴有囊性成分,T1加權像中腫瘤組織表現為等信號或低信號,T2加權像中腫瘤組織表現為等信號或者高信號,彌散加權成像(diffusion weighted imaging,DWI)中,腫瘤組織多提示彌散受限[10-11]。一項成人MB放療的多中心研究(NOA-07試驗)發現,腫瘤出血以及腦室內轉移多提示WNT活化型髓母細胞瘤[12]。PERREAUT等[13]發現MB分子亞型與腫瘤位置密切相關,WNT活化型多位于橋小腦角區,SHH活化型多位于小腦半球,非WNT/非SHH活化型多位于小腦蚓部或第四腦室。MORA等[14]發現,磁共振波譜成像(magnetic resonance spectrum,MRS)有利于區別MB與其他類型腫瘤:高膽堿提示MB,高肌醇提示室管膜瘤,高脂提示轉移瘤或血管母細胞瘤。羅楚涵等[15]在兒童MB鑒別診斷中應用動態對比增強磁共振(dynamic contrast-enhanced perfusion MRI,DCE-MRI)準確地顯示病變血流動力學變化,從而通過容量轉移常數(Ktrans)、速率常數(Kep)、血管外/細胞外間隙容積分數(Ve)、血漿容積分數(Vp)值等多種參數準確地對髓母細胞瘤與其他后顱窩腫瘤進行鑒別診斷,這也為成人MB與其他腫瘤的鑒別提供了一種新思路。
3 治療
3.1 外科治療成人MB首選手術切除。不同部位腫瘤可采取相應的手術入路。中線區MB可經膜髓帆入路或者蚓部入路,腦室內腫瘤可能還需要切除下蚓部進行腫瘤的暴露[6]。經膜髓帆入路更有利于切除延伸至外側隱窩的腫瘤[6]。成人MB常選擇俯臥位或側俯臥位,在神經導航下行旁正中入路幕下病變切除術。臨床醫生可根據腫瘤部位而選擇不同的手術體位,但是與體位相對應的并發癥需重視,比如坐位可能導致空氣栓塞以及氣顱等風險[16-17]。術中持續電生理監測(包括體感誘發電位及運動誘發電位的持續監測)在幕下病變切除術中起著重要的警示作用[18]。部分患者由于腫瘤壓迫導致腦脊液循環通路受阻,從而發展為梗阻性腦積水。對于此類患者優先選擇第三腦室造瘺術,需慎重選擇腦室-腹腔分流術,以防止增加腹膜轉移的風險[11,19]。
3.2 放療成人MB術后輔以CSI聯合后顱窩加強放療為標準治療。放療能夠控制局部腫瘤的生長以及延長患者的無進展生存期,然而對于成人MB放療的劑量選擇尚無統一標準[20]。成人MB患者放療劑量的選擇大多參考兒童患者臨床數據,其存在一些局限性。成人對放療的中樞神經系統毒性作用耐受強于兒童,然而骨髓以及其他器官對放療的耐受卻更差[6,21]。目前成人MB的標危組患者通常予以CSI(23.4 Gy)聯合后顱窩加強放療(54 Gy),輔以前期化療,或者CSI(36 Gy)聯合后顱窩加強放療(54.8 Gy);對于高危組患者予以CSI(36 Gy)聯合后顱窩加強放療(54 Gy),輔以前期化療[22]。ABACIOGLU等[23]發現,成人患者術后3周內、3~6周和6周后予以放療的5年無病生存率分別為0、85%和75%(P=0.002)。放療時機的選擇與成人MB的預后密切相關。西班牙醫學腫瘤學會(SEMO)關于成人MB的指南建議放療時機應在術后3~6周開始[7]。質子放療是一種新的放療方式,射線粒子的能量可直接進入腫瘤細胞內釋放,對正常組織以及臟器的毒害作用較小,效果優于普通的X射線以及電子線[22]。然而質子放療設備昂貴,限制了其在臨床的廣泛應用。
3.3 化療化療在兒童MB患者中取得較好效果。對于成人MB術后行放療的同時也予以化療。KOCAKAYA等[24]對227篇成人MB論文進行meta分析,表明一線化療患者的生存時間明顯長于單純放療患者或腫瘤復發時接受化療的患者。在一項根據兒科HIT-2000方案治療成人非轉移性MB的前瞻性多中心研究中,49例接受聯合放化療的非轉移性疾病成人患者的4年無病生存率為74%,總體生存率為94%[25]。目前SEMO以及EANO-EURACAN兩項關于成人MB的指南均建議,成人患者在接受手術切除以及放療的同時需行化療[6-7]。然而成人MB的化療方案無統一標準,大多借鑒兒童MB患者的方案。Packer方案是最為常見的一種化療方案,其包括放療期間予以長春新堿(1.5 mg/m2,不超過2 mg),隨后予以8個療程洛莫司汀(75 mg/m2),順鉑(70mg/m2)和長春新堿(1.5 mg/m2,不超過2 mg)治療[6-7]。成人MB患者對Packer化療方案的耐受性似乎比兒童患者更差,然而沒有其他對成人毒副作用小的藥物能夠替代順鉑、洛莫司汀或長春新堿等化療藥物,對于成人患者化療藥物的選擇待進一步研究[22]。
3.4 其他治療自體干細胞移植聯合高劑量化療在治療復發的成人MB是一種可行方案[22]。GILL等[26]一項關于復發的成人MB研究中,將自體干細胞移植聯合高劑量化療與接受常規化療的成人患者進行了比較,自體干細胞移植聯合高劑量化療組患者中位生存期高于常規化療組,表明接受自體干細胞移植聯合高劑量化療的復發成人MB患者具有更好預后。
隨著對MB分子亞型的認知加深,個體化靶向治療也成為了一種新的治療方案,SHH活化型是成人MB最為多見的分子亞型,其特征是Sonic-Hedgehog途徑的異常激活[27]。SMO抑制劑治療SHH亞型MB的早期臨床試驗結果欠佳。但是ROBINSON等[27]研究發現:SMO抑制劑對于成人患者效果較好,對于而兒童患者效果較差,原因是成人患者多為SHH通路的上游突變,而兒童患者多為下游突變,比如GLI基因的擴增以及SUFU基因的突變,這導致了對SMO抑制劑的耐藥性。Vismodegib(GDC-49)和sonidegib是兩種典型SMO抑制劑,通過與SMO結合,抑制SHH旁路并誘導腫瘤的退化,該藥物在MB的小樣本研究以及個案中具有良好療效[27-28]。關于Vismodegib(GDC-49)和sonidegib治療MB的一項meta分析也表明該藥物患者耐受性好、副作用小,并顯示了良好的抗腫瘤活性[29]。
4 預后影響因素
4.1 年齡與性別年齡是影響兒童MB預后的一個重要因素,然而是否影響成人MB的預后卻存在著爭議[30-32]。LAI等[31]通過分析454名成人MB的臨床數據,發現18~20歲的患者預后最好,21~40歲或40歲以上的患者預后最差。其他研究則認為年齡對于成人MB預后無意義。有研究表明女性MB患者比男性MB患者預后更好,然而更多研究則認為性別與成人患者的預后無相關性[32]。
4.2 組織學分型LC/A已被證明是兒童患者預后不良的因素,DN被認為兒童患者預后良好的因素[30]。成人患者中LC/A雖較為少見,但也提示預后不良[22]。張娜等[32]關于成人MB研究發現:DN 5年無進展生存期及總體生存率最好,CL和MBEN次之,LC/A預后最差。LAI等[31]一項關于成人MB的研究結果表明:LC/A及DN均預后較差。
4.3 分子分型WNT活化型約占成人MB的15%,對應的組織學類型多為經典型,預后最好,5年生存率約為90%,常與6號染色體、CTTNB1癌基因突變相關[33]。SHH活化型發病率表現為年齡的雙波峰分布,第一個峰值為出現在嬰兒組(0~3歲),第二個峰值在16歲以上青少年和成人,3~16歲患者少見[34]。SHH活化型約占成人MB 60%,WHO CNS5依據TP53基因有無突變分為TP53野生型以及TP53突變型,TP53突變型患者預后較差[3,33]。WHO CNS5將group3和group4合并為非WNT/非SHH活化型,其約占成人MB 25%,組織學類型多為經典型,5年生存率約為50%,常與MYCN和CDK6等基因的突變相關[23]。
4.4 轉移以及腫瘤切除程度診斷時出現腫瘤轉移已證實是成人MB預后不良的重要因素[2]。BRANDES等[34]一項評估成人MB預后的前瞻性研究結果表明:無轉移MB患者的預后明顯好于存在轉移MB患者,5年無進展生存期分別為75%和45%(P=0.01)。目前腫瘤全切除是兒童MB患者預后良好的重要因素,術后腫瘤殘留>1.5 cm2的兒童患者預后往往較差,然而腫瘤切除程度對于成人MB患者預后影響卻并不明確[29]。LAI等[31]多因素回歸分析表明腫瘤全切除是成人MB有利的預后因素。然而也有研究認為腫瘤切除程度并不是成人MB患者的預后影響因素[35]。雖然腫瘤切除程度對于成人MB的預后尚有爭議,但最大限度地安全切除腫瘤仍然是成人MB的手術目標。
5 總結與展望
從目前已有研究上看,成人MB發病率低,顱腦MRI是其首選的診斷方法,MRS以及DCE-MRI的應用可減少MB的誤診率。手術切除腫瘤是成人MB的首選治療方式,術后輔以放、化療能夠明顯改善患者的預后。分子分型為SHH活化和TP53突變型的成人MB預后差,個體化的靶向治療有望改善其預后。

