玻璃體腔注射貝伐單抗和雷珠單抗治療1型ROP療效的Meta分析
曹榮霞,李雁杰,劉為曬,白子超,楊柳森,李 鮮
0引言
早產兒視網膜病變(retinopathy of prematurity,ROP)是世界范圍內主要的兒童致盲性眼病之一[1]。嚴重的ROP可引起視網膜脫離,導致視力喪失。全球平均每年約有28300~45600例嬰幼兒被診斷為與ROP相關的不可逆性視力損害[2]。ROP 的發病機制包括兩個階段,第一階段發生在矯正胎齡約為22~30wk,這一階段早產兒處于相對高氧的環境,并且VEGF分泌減少;第二階段發生在矯正胎齡約為31~44wk,早產兒這一階段處于相對缺氧的環境,VEGF分泌增加。所以,對于ROP的抗VEGF治療需要掌握合適的時機,以達到預期治療目的[3-4]。
ROP作為一種新生血管性眼底病變,其治療方式也經歷了從冷凍治療到激光治療的變革。以上治療方法均通過破壞新生血管區視網膜來達到減少VEGF產生的目的,進而阻止疾病的進一步進展[5]。隨著抗VEGF治療眼底新生血管疾病的廣泛應用,抗VEGF藥物在ROP的治療中也逐步開展。2011年,BEATROP(Bevacizumab Eliminates the Angiogenic Threat of Retinopathy of Prematurity)研究首次提出玻璃體腔注射貝伐單抗(intravitreal bevacizumab,IVB)的治療方法可以消退ROP的新生血管,與傳統的激光治療相比,經過這種治療ROP有明顯更低的復發率[3]。盡管目前激光治療仍為ROP治療的金標準,但由于激光治療具有視野損害、術后高度近視發生率高及全身麻醉手術風險等副作用[6-7]。所以,抗VEGF藥物治療ROP也逐漸被廣泛應用于臨床中[8-9]。目前,臨床工作中廣泛應用的抗VEGF藥物主要包括:雷珠單抗、貝伐單抗、阿柏西普、康柏西普等。本文評價IVB和玻璃體腔注射雷珠單抗(intravitreal ranibizumab,IVR)治療1型ROP的療效。
1資料和方法
1.1資料由兩名研究員分別通過計算機檢索PubMed、Embase、Web of Science、the Cochrane Library、CQVIP、CBM、OVID、中國知網和萬方數據庫,檢索時間為建庫至2020-04-01。在PubMed數據庫中具體檢索策略為:(“retinopathy of prematurity”or“ROP”),and (“bevacizumab”or“avastin”or“intravitreal of bevacizumab”or“IVB”),and (“ranibizumab”or“lucentis”or“intravitreal of ranibizumab”or“IVR”)。中國知網的檢索關鍵詞包括:早產兒視網膜病變、貝伐單抗、雷珠單抗。使用EndNote X7對文獻進行管理。
1.1.1納入標準(1)早產兒出生體質量≤1500g,或孕期≤30wk[10];(2)ROP治療標準為ETROP[4]研究提出的1型ROP,具體為:Ⅰ區有附加病變的任何期ROP,Ⅰ區3期有或無附加病變,Ⅱ區2期或3期有附加病變的ROP;(3)比較IVB和IVR對1型ROP治療作用的隨機對照研究或者非隨機對照研究(病例對照研究);(4)研究至少包括一種以下結局指標:再治療率、完全血管化比例、等效球鏡度數(spherical equivalent,SE);(5)納入研究的貝伐單抗和雷珠單抗治療劑量具體為:貝伐單抗:0.625mg/0.025mL,雷珠單抗:0.25mg/0.025mL;(6)納入研究的ROP患者治療后屈光檢查年齡1~1.5歲。
1.1.2排除標準(1)未報道本次統計需要的結局指標,或者結局指標無法提取或推算;(2)研究分組信息不完善的研究。
1.2方法
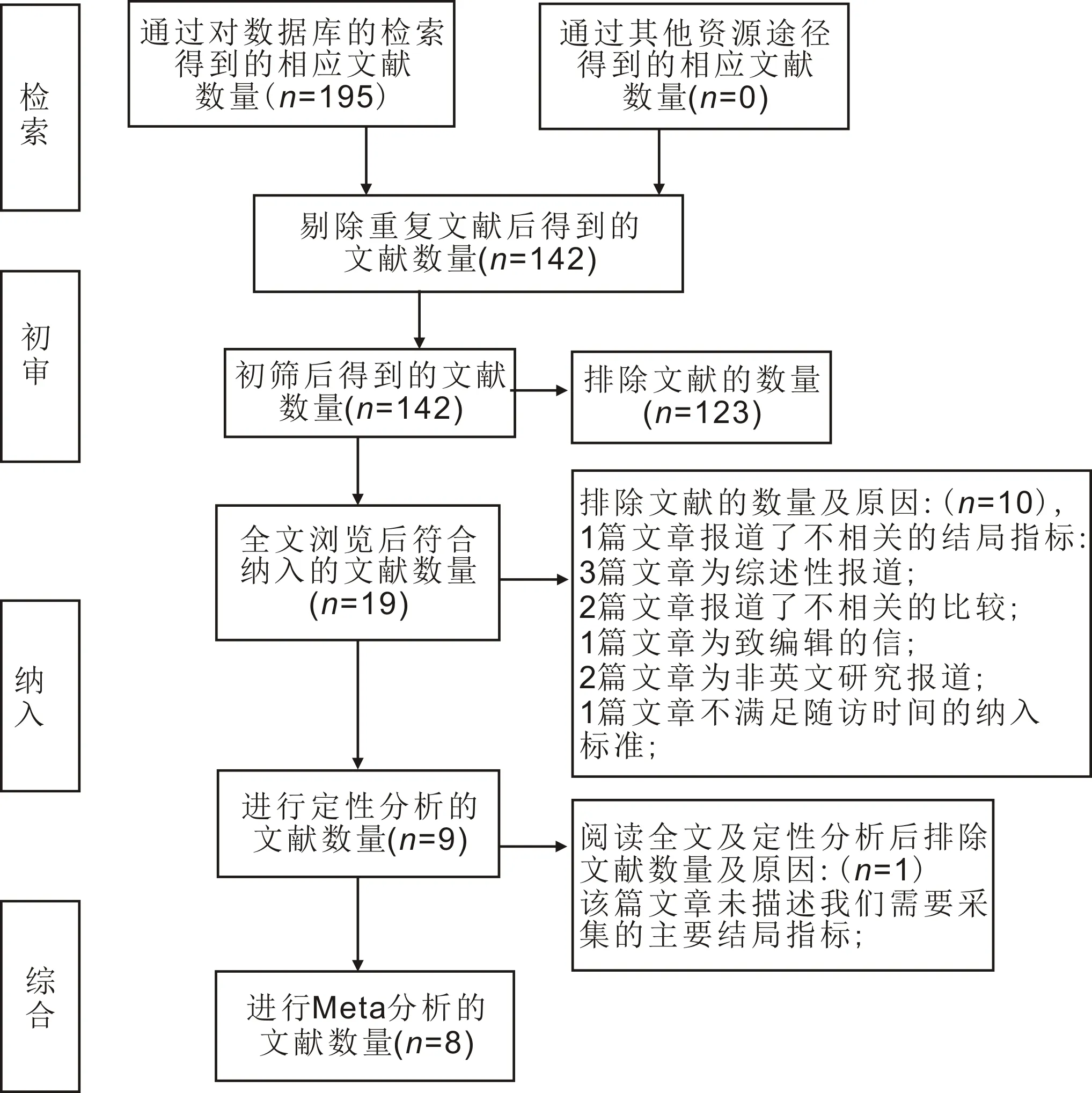
圖1 文獻篩選流程圖。
1.2.1數據提取由兩位研究員根據納入及排除標準進行文獻篩選和質量評估,當兩位研究員有疑義時,通過閱讀全文達成一致。在目標數據庫中一共檢索到195篇文章,其中53篇重復的文章被移除,通過閱讀標題和摘要,剔除123篇文章,通過閱讀全文,11篇文章被排除。最終,有8篇文章符合納入標準[11-18]。文章篩選流程見圖1。
從納入研究的文獻中提取的數據包括:基本研究信息:文章標題、作者、發表時間;樣本量、研究設計類型、治療計劃和隨訪時間,結果信息:再治療率、完全血管化比例和SE。納入研究的基本信息見表1。
1.2.2質量評價對納入的文獻(本研究納入的文獻均為病例對照研究)使用紐卡斯爾-渥太華量表(Newcastle-Ottawa Scale,NOS)[19]。NOS量表滿分為9顆星,0~3、4~6和7~9顆星分別代表低質量、中等質量和高質量,見表2。
統計學分析:使用Review Manager 5.3進行統計分析。連續性變量(等效球鏡度數)采用加權均數差(weighted mean difference,WMD)和95%置信區間為效應分析統計量,二分類變量(再治療率和完全血管化比例)采用比值比(odds ratio,OR)和95%置信區間為效應分析統計量。使用χ2檢驗來判斷納入研究之間的異質性。當P<0.1或者I2>50%時認為有明顯異質性,使用隨機效應模型,當P>0.1或I2<50%時使用固定效應模型。當存在明顯的異質性時,通過使用逐一排除某些研究的敏感性分析來進行異質性處理。采用Stata 16.0軟件進行偏倚檢驗,包括Begger檢驗和Egger檢驗。
2結果
2.1文獻質量評估對納入的8篇文獻進行質量評價,見表2。其中Kang等[18]研究得分為5星,為中等質量,其余研究得分7~8星,均為高質量。
2.2治療作用評價
2.2.1再治療率納入的8項文獻中均報道了再治療率,分析各研究結果間無明顯異質性(P=0.78,I2=0%),采用固定效應模型。結果顯示,IVR組比IVB組有明顯更高的再治療率,差異有統計學意義(OR=0.55,95%CI:0.34~0.88,P<0.05),見圖2。
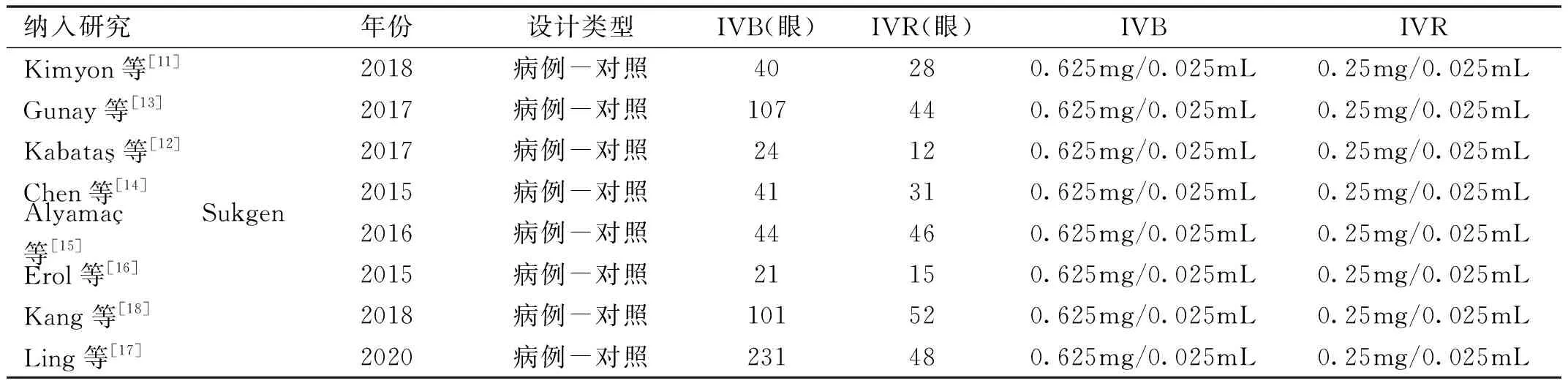
表1 納入研究的文獻基本信息
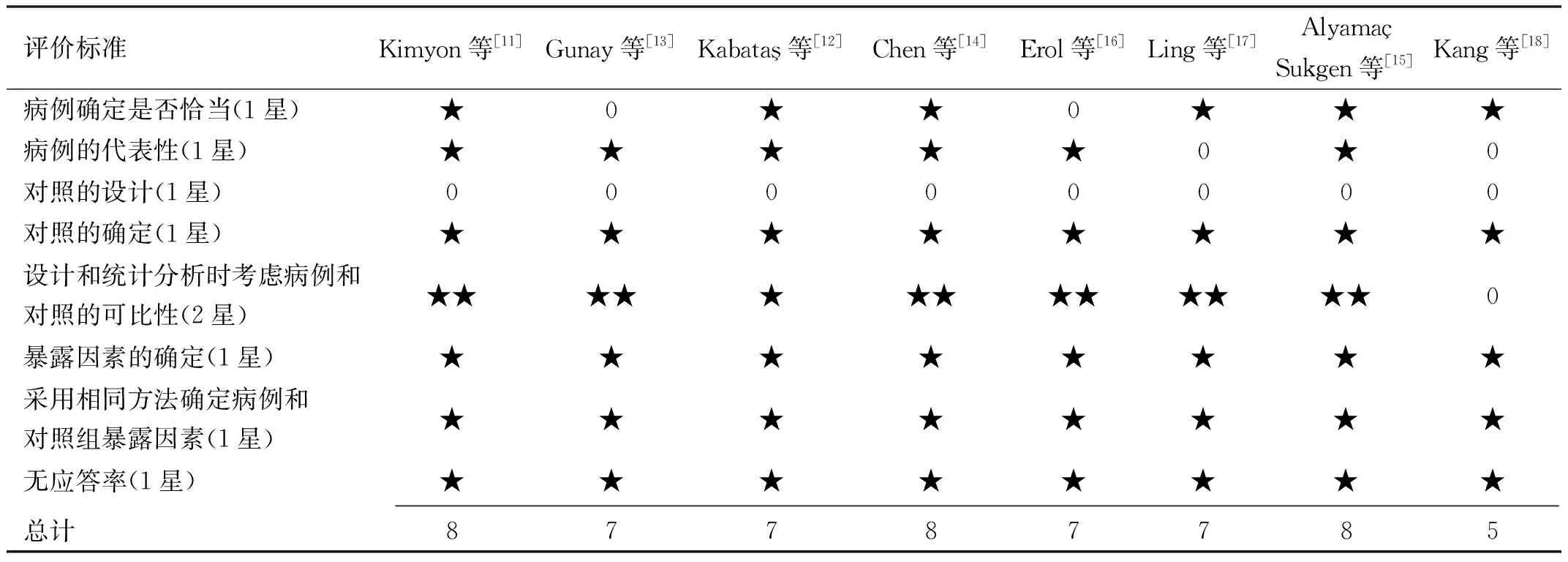
表2 納入研究的文獻NOS量表質量評價
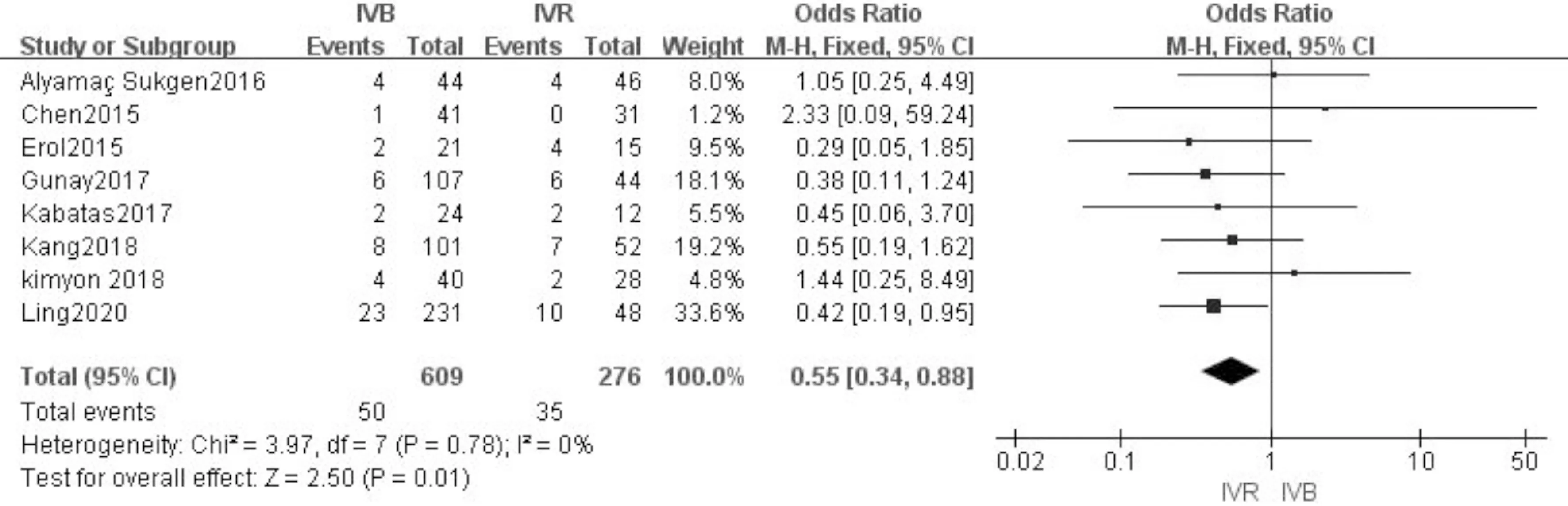
圖2 再治療率的森林圖。
2.2.2完全血管化比例納入的4項研究中(Gunay等[13],Kang等[18],Kimyon等[11],Alyama? Sukgen等[15])報告了完全血管化比例,數據分析各研究結果間存在異質性,且有統計學意義(I2=74%,P=0.01),使用隨機效應模型計算合并統計量,分析結果表明,在IVB和IVR組中完全血管化比例差異無統計學意義(OR=2.15,95%CI:0.80~5.76,P>0.05)(圖3)。分析其異質性來源,可能與 Kang等[18]中等質量的研究有關,通過剔除Kang等[18]研究進行敏感性分析,異質性從74%降低為0%,且總體效應量無變化(表3)。
2.2.3 SE在8項研究中,共有4項研究報道了等效球鏡度數(SE),對數據進行分析結果顯示,各研究間異質性較大(I2=63%,P=0.05),使用隨機效應模型計算合并統計量,結果表明IVR比IVB治療組有更低的SE,差異有統計學意義(WMD=-1.44,95%CI:-2.28~-0.00,P=0.05),見圖4。通過逐一剔除每篇文獻進行敏感性分析,剔除Kimyon等[11]的研究,結果表明兩組間差異無統計學意義(WMD=-0.71,95%CI:-1.59~0.17,P>0.05);通過剔除Gunay等[13]的研究,結果顯示兩組間差異無統計學意義(WMD=-0.98,95%CI:-2.69~0.73,P>0.05),見表4。分析其異質性來源可能與受檢者屈光檢測年齡、散瞳方法以及檢影驗光屈光檢查設備不同有關。Chen等[14]和Kimyon等[11]屈光檢測年齡為1.5歲,Gunay等[13]和Kabatas等[12]為1歲;Chen等[14]使用兩次間隔10min的2%環噴托酯以及1次1%托吡卡胺后1h行屈光檢查,Kabatas等[12]使用兩次間隔5min的1%環噴托酯50min后行屈光檢查,而Kimyon等[11]和Gunay等[13]使用2次間隔10min的1%環噴托酯滴眼液45min后行屈光檢查。
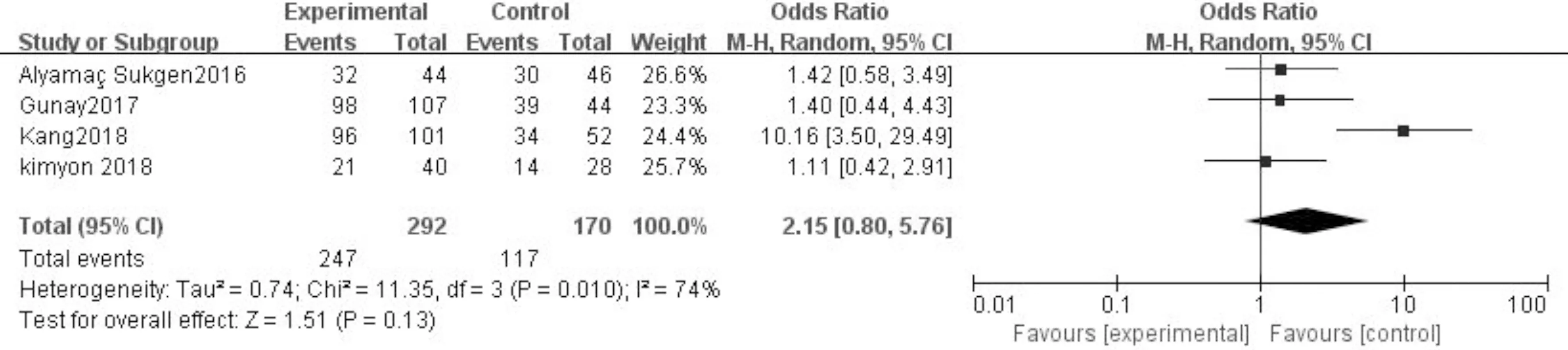
圖3 完全血管化比例的森林圖。
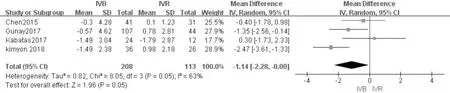
圖4 SE的森林圖。
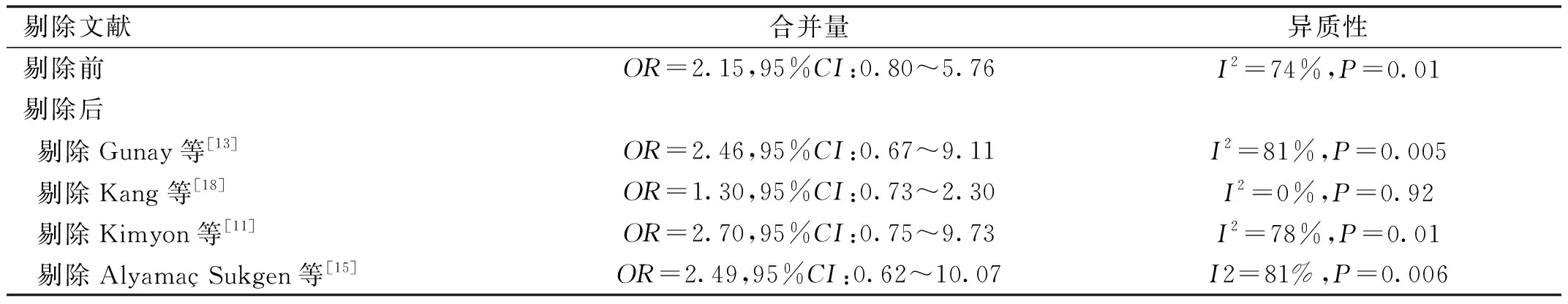
表3 完全血管化比例敏感性分析

表4 SE敏感性分析
Gunay等[13]未詳細闡述所用屈光檢查設備,Kabatas等[12]使用Welch Allyn Sure Sight檢影設備,而Kimyon等[11]以及Chen等[14]使用K-Plus 2 Nikon檢影設備。
2.3發表偏倚發表偏倚使用Begger檢驗和Egger檢驗,再治療率(P=0.386和P=0.194),完全血管化比例(P=0.734和P=0.643),SE(P=0.734和P=0.996),結果表明存在發表偏倚的可能性較小。
3討論
目前,ROP治療的金標準依然是激光治療。但是,隨著抗VEGF治療已經成功應用于糖尿病黃斑水腫(diabetic macular edema,DME)、視網膜靜脈阻塞(retinal vein occlusion,RVO)、年齡相關性黃斑變性(age-related macular degeneration,ARMD)等眼底新生血管性疾病,抗VEGF治療也在ROP的治療中逐步開展。由于成人與嬰幼兒的生理代謝特點等不同,抗VEGF應用于ROP治療仍有很大的爭議。由于受試者的特殊性,目前對于抗VEGF藥物治療ROP的臨床研究絕大部分均為病例對照研究,極少數為隨機對照研究。目前在臨床上關于ROP抗VEGF治療開展的研究包括:激光治療與抗VEGF治療的比較,不同類型抗VEGF藥物治療的比較,不同劑量抗VEGF藥物的比較等。
在ROP的臨床治療過程中,面臨的最大問題為ROP治療后復發。但是,目前世界范圍內仍缺乏對ROP復發的精確定義。所以,在不同的研究中,對ROP復發所使用的定義不同。Gunay等[13]認為ROP的復發為首次治療后視網膜血管化的停滯并伴隨視網膜分界線的出現,伴或者不伴附加病變。Ling等[17]認為復發是初始治療后視網膜狀況好轉,但是隨后附加病變或者新生血管的出現或惡化。而Kang等[18]認為ROP的復發為需要再治療,這與“RAINBOW(Ranibizumab versus laser therapy for the treatment of very low birthweight infants with retinopathy of prematurity)”[20]研究相似,所以在本次研究當中,我們使用再治療率來作為ROP治療后復發的評價指標。
在本次Meta分析中,發現與IVB治療組相比,IVR治療組有明顯更高的再治療率。我們推測這可能是與雷珠單抗有更小的分子量、更短的半衰期及更快的清除率有關。
雷珠單抗是一個分子質量為48kDa的人源化單克隆抗體片段,貝伐單抗是分子質量為149kDa的重組全長人源化單克隆抗體片段[21-22]。動物研究顯示,雷珠單抗的半衰期為2.88d,而貝伐單抗為4.32d。所以雷珠單抗比貝伐單抗有更小的分子質量,及更短的半衰期。換言之,即雷珠單抗對眼內VEGF因子的抑制時間較貝伐單抗更短[23-24]。
但是,由于雷珠單抗和貝伐單抗都是通過作用于VEGF-A發揮作用,所以其抗VEGF的機制基本類似。抗VEGF治療后,對于ROP患者完全血管化比例方面,兩種藥物無統計學差異。但有研究顯示,經兩種藥物治療后,嬰幼兒在完成血管化的時間方面,均晚于正常生理血管化時間,這可能是抗VEGF的治療作用[15]。
嬰幼兒正視化的發展是一個及其復雜的過程,它與眼內聚焦、視網膜光感受器發展、脈絡膜厚度及基因等因素相關[10]。本次Meta分析中,可以發現IVR治療組比IVB組有明顯更低的SE。我們推測這可能與多個因素相關:(1)有研究表明早產本身是近視發生的危險因素[25]。(2)與雷珠單抗相比,貝伐單抗有更長時間的視網膜VEGF 抑制,這可能導致周邊視網膜惡化加重,進而影響正視化過程。因為完整的周邊視網膜可能會促進正視化過程的正常發展[26]。
此外,還有研究表明,通過VEGF[27]、成纖維細胞生長因子[28]等在內的多種生長因子的共同作用,脈絡膜可能在鞏膜的重塑過程中發揮重要的作用。有研究發現,在DME、ARMD等的治療過程中,IVB和IVR治療可以明顯減少脈絡膜厚度和體積[29-31]。而與雷珠單抗相比,貝伐單抗有更長的半衰期,可以使脈絡膜厚度更大程度地降低,從而影響正視化過程,導致更大程度的近視發生。
本次Meta分析,所有納入的研究均為病例對照研究,無隨機對照研究的納入,并且納入研究的數量有限。在統計分析中,未分析抗VEGF治療后患者眼內及全身的并發癥。同時,由于本次研究納入的抗VEGF治療劑量均為成人的一半,沒有分析不同治療劑量對ROP的作用。并且沒有更長隨訪時間的SE改變的分析。
對于ROP治療,IVB和IVR均可以完成視網膜的完全血管化,并且這兩種治療在視網膜完全血管化比例方面無統計學差異。與IVB治療相比,IVR治療有更高的再治療率及更低的SE。由于本研究證據質量有限,故需要更多隨機對照研究來證明。

