右美托咪定抑制丙泊酚誘導原代培養皮層神經元凋亡
李建立,尹德云,王蘊欣,吳紅海,侯艷寧
(1.河北省人民醫院麻醉科,石家莊 050051;2.河北省人民醫院心內科,石家莊 050051;3.白求恩國際和平醫院藥劑科,石家莊 050082)
右美托咪定抑制丙泊酚誘導原代培養皮層神經元凋亡
李建立1,尹德云2,王蘊欣1,吳紅海3,侯艷寧3
(1.河北省人民醫院麻醉科,石家莊 050051;2.河北省人民醫院心內科,石家莊 050051;3.白求恩國際和平醫院藥劑科,石家莊 050082)
目的 探討右美托咪定抑制丙泊酚誘導原代培養皮層神經元凋亡的機制。方法 體外原代培養7d的大鼠皮層神經元,給予500μmol/L丙泊酚和(或)不同濃度右美托咪定處理12h后,分為丙泊酚組、右美托咪定+丙泊酚組,對照組給予同溶劑的20%脂肪乳,用四甲基噻唑藍(MTT)法檢測各組神經元存活率的變化,Hoechst33258核染色法檢測神經元調亡,蛋白質印跡法(Westernblotting)測定神經元磷酸化cAMP反應元件結合蛋白(pCREB)和細胞色素C(Cyt-C)蛋白水平。結果 與對照組比較,丙泊酚組神經元存活率明顯下降,神經元凋亡率明顯增加,pCREB蛋白水平明顯降低,Cyt-C蛋白水平明顯增加,差異均有統計學意義(P<0.01)。與丙泊酚組比較,右美托咪定+丙泊酚組神經元存活率明顯增加,神經元凋亡率明顯下降,pCREB蛋白水平明顯增加,Cyt-C蛋白水平明顯下降,差異均有統計學意義(P<0.01)。結論 右美托咪定可對抗丙泊酚引起的原代培養皮層神經元凋亡,其機制可能與增加pCREB蛋白水平,降低Cyt-C蛋白水平有關。
丙泊酚;右美托咪定;原代培養皮層神經元;凋亡;磷酸化cAMP反應元件結合蛋白;細胞色素C
丙泊酚通過激動γ氨基丁酸A型受體(gamma amino acid type A receptor,GABAR)和抑制N-甲基-D-天冬氨酸受體(N-methyl-D-aspartic acid receptor,NMDAR)發揮麻醉作用,被廣泛用于麻醉誘導和維持。藥典顯示3歲以下患兒慎用丙泊酚,但在臨床工作中丙泊酚被廣泛用于嬰幼兒麻醉。丙泊酚是否對發育期大腦產生神經損傷目前觀點不一。最近研究表明,丙泊酚可引起發育期動物大腦廣泛腦區神經細胞和原代培養神經元凋亡[1-4]。因此,尋找藥物抑制丙泊酚發育期神經毒性已成為嬰幼兒麻醉的重要研究內容。右美托咪定是高選擇性α2腎上腺素受體激動藥,具有鎮靜、鎮痛和拮抗交感神經活性的作用,可對抗丙泊酚引起的原代培養神經元凋亡和發育期大鼠大腦神經損傷,但具體機制還不清楚[5-6]。本文利用原代培養皮層神經元研究右美托咪定對抗丙泊酚誘導原代培養皮層神經元凋亡的機制。
1 材料與方法
1.1 藥物與試劑 丙泊酚(Diprivan,意大利AstraZeneca公司,批號:KW814),右美托咪定(江蘇恒瑞醫藥股份有限公司,批號14102132);20%脂肪乳購自廣州百特公司,DMEM培養液、胎牛血清、Neurobasal培養液、B27促生長劑購自美國Gibco公司,LY294002、二甲基亞砜(DMSO)、噻唑藍(MTT)購自美國Sigma公司,Hoechst33258熒光染料和胰蛋白酶購自北京索來寶公司,磷酸化cAMP反應元件結合蛋白(phosphorylated cAMP response-element binding protein,pCREB)和細胞色素C(cytochrome C,Cyt-C)抗體購自美國Cell Signal Technology公司。
1.2 方法
1.2.1 皮層神經元原代培養 按文獻[7]進行原代皮層神經元培養。體外培養7 d的神經元用于實驗。
1.2.2 實驗分組 觀察右美托咪定對神經元的保護作用時,分為對照組(給予同溶劑的20%脂肪乳)、丙泊酚組(丙泊酚終濃度為500 μmol/L)、右美托咪定+丙泊酚組(右美托咪定終濃度分別為0.001、0.010、0.100、1.000 μmol/L,丙泊酚終濃度為500 μmol/L)。檢測各種處理對神經元凋亡的影響時,分為對照組(給予同溶劑的20%脂肪乳)、丙泊酚組(終濃度為500 μmol/L)、右美托咪定+丙泊酚組(右美托咪定終濃度為0.1 μmol/L,丙泊酚終濃度為500 μmol/L)。
1.2.3 四甲基噻唑藍(MTT)法檢測神經元存活率 將細胞接種于96孔板,體外培養至第7天分別給予不同的藥物處理12 h后,按文獻[7]應用MTT法檢測神經元存活率。
1.2.4 Hoechst33258核染色法檢測神經元凋亡 將神經元接種于6孔培養板中,按上述方法培養,分別給予不同藥物處理后,按文獻[7]應用Hoechst33258核染色法檢測神經元凋亡。
1.2.5 蛋白質印跡法(Western blotting)測定pCREB和Cyt-C蛋白水平 細胞經不同藥物處理后,收集細胞,裂解細胞提取總蛋白,BCA法檢測樣品蛋白水平。取待測蛋白質50 μg加上樣緩沖液煮沸變性,于10%十二烷基硫酸鈉-聚丙烯酰胺凝膠中100 V電泳l.5 h,轉膜1 h,加入pCREB和Cyt-C抗體(1∶2 000),4 ℃過夜,常規洗滌,加羊抗鼠二抗(1∶5 000)37 ℃孵育60 min,洗滌,電化學法發光、顯影、掃描,用凝膠圖像處理系統分析目標條帶與內參條帶吸光度的比值。實驗重復3次,設β-actin蛋白為內參。

2 結 果
2.1 不同處理對原代培養皮層神經元存活率的影響 與對照組比較,丙泊酚組神經元存活率明顯下降,差異有統計學意義(P<0.01);與丙泊酚組比較,右美托咪定可濃度依賴性提高神經元存活率,差異有統計學意義(P<0.01),見圖1。
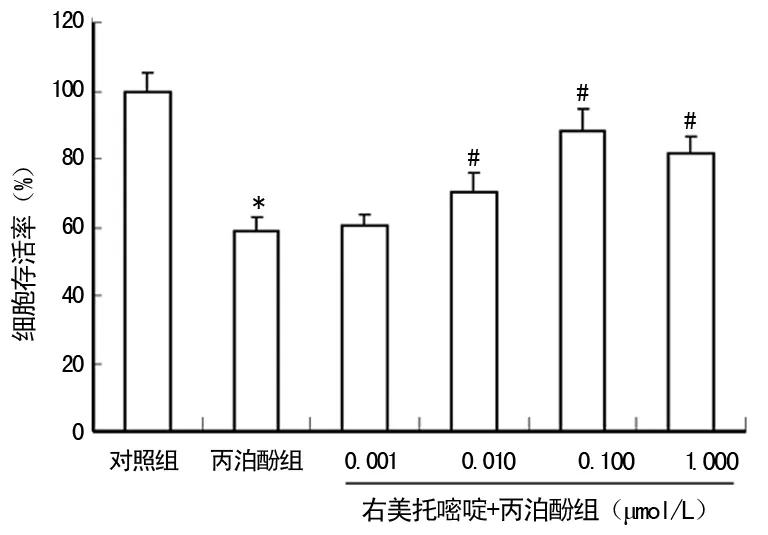
*:P<0.01,與對照組比較;#:P<0.01,與丙泊酚組比較。
圖1 不同處理對神經元存活率的影響
2.2 不同處理對原代培養皮層神經元凋亡的影響 與對照組比較,丙泊酚組神經元凋亡率明顯增加,差異有統計學意義(P<0.01);與丙泊酚組比較,右美托咪定+丙泊酚組皮層神經元凋亡率明顯下降,差異有統計學意義(P<0.01),見圖2。
2.3 不同處理對原代培養皮層神經元pCREB蛋白水平的影響 與對照組比較,丙泊酚組pCREB蛋白水平明顯降低,差異有統計學意義(P<0.01);與丙泊酚組比較,右美托咪定+丙泊酚組pCREB蛋白水平明顯增加,差異有統計學意義(P<0.01),見圖3。
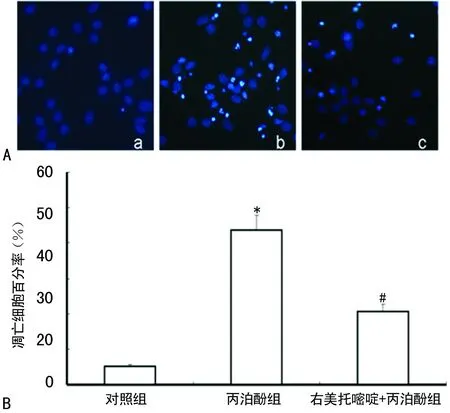
A:Hoechst33258核染色法(×200);a:對照組;b:丙泊酚組;c:右美托嘧喧+丙泊酚組;*:P<0.01,與對照組比較;#:P<0.01,與丙泊酚組比較。
圖2 不同處理對神經元凋亡的影響

*:P<0.01,與對照組比較;#:P<0.01,與丙泊酚組比較。
圖3 不同處理對神經元pCREB蛋白水平的影響
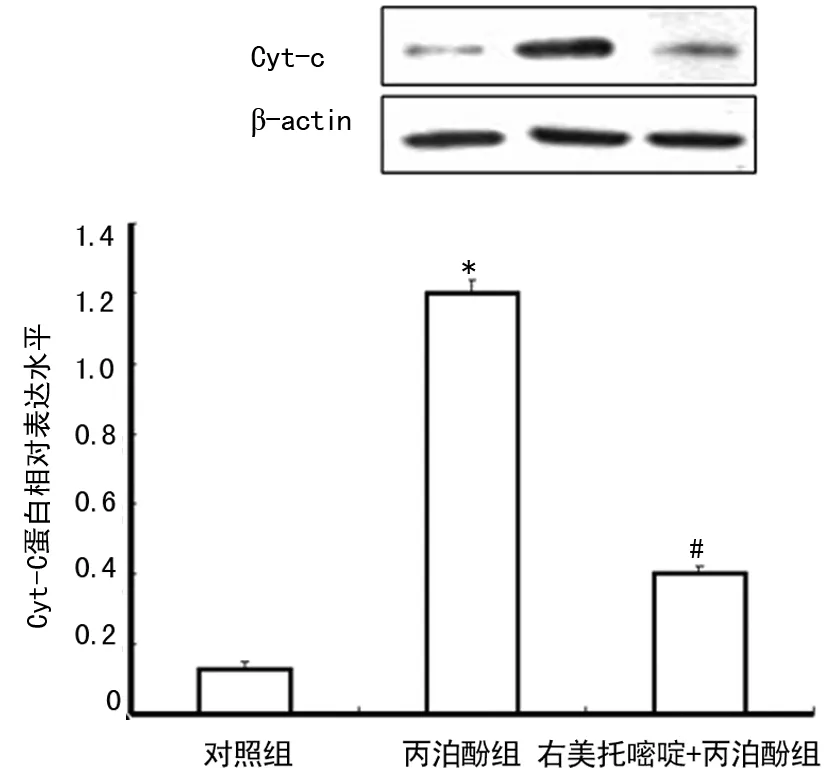
*:P<0.01,與對照組比較;#:P<0.01,與丙泊酚組比較。
圖4 不同處理對神經元Cyt-C蛋白水平的影響
2.4 不同處理對原代培養皮層神經元Cyt-C蛋白水平的影響 與對照組比較,丙泊酚組Cyt-C蛋白水平明顯增加,差異有統計學意義(P<0.01);與丙泊酚組比較,右美托咪定+丙泊酚組Cyt-C蛋白水平明顯降低,差異有統計學意義(P<0.01),見圖4。
3 討 論
全世界每年有眾多患兒因各種原因接受全身麻醉。近年來多項研究報道丙泊酚具有發育期神經毒性,可對發育期動物大腦和原代培養神經元產生損傷[1-4],因此,丙泊酚的發育期神經毒性引起了學者的廣泛關注,同時尋找安全有效防治丙泊酚發育期神經毒性的藥物具有十分重要的臨床意義。
右美托咪定是臨床上常用的高選擇性的α2腎上腺素受體激動藥,具有抑制交感神經,鎮靜鎮痛和減少麻醉藥用量等作用,作為麻醉輔助藥物被廣泛用于臨床麻醉中。目前研究發現,右美托咪定可對多種神經損傷模型產生保護作用,如對抗缺血再灌注損傷[8],高氧誘導的發育期大腦損傷[9]。另有研究發現,右美托咪定可抑制丙泊酚引起的原代培養海馬神經元存活率的下降,其機制尚不清楚[6]。另有研究表明,右美托咪定不會對發育期大腦產生神經損傷[10]。本文利用原代培養皮層神經元研究右美托咪定對抗丙泊酚引起原代培養皮層神經元損傷的機制。MTT結果顯示,與對照組比較,丙泊酚組神經元存活率明顯降低,右美托咪定可濃度依賴性地提高神經元的存活率。Hoechst33258核染色結果顯示,與對照組比較,丙泊酚組神經元凋亡率明顯增加,與丙泊酚組比較,右美托咪定+丙泊酚組神經元凋亡率明顯降低。
CREB為神經保護的中樞調節因子,參與細胞內多種信號通路的傳導,其磷酸化在調控轉錄起始過程中發揮著關鍵作用,另外磷酸化CREBser-133位點可介導神經元存活及突觸的形成,通過調控大量促神經元存活基因如Bcl-2和腦源性神經營養因子(BDNF)的表達,進而發揮神經保護作用[11]。研究發現,丙泊酚通過抑制CREB的磷酸化水平引起神經細胞損傷[12-13],右美托咪定可通過提高原代培養海馬神經元pCREB蛋白水平,進而抑制海馬神經元凋亡[14]。本文Westernblotting結果顯示,與對照組比較,丙泊酚組pCREB蛋白水平明顯降低,與丙泊酚組比較,右美托咪定+丙泊酚組pCREB蛋白水平明顯增加,提示丙泊酚通過降低皮層神經元pCREB蛋白水平引起皮層神經元凋亡,而右美托咪定可通過提高pCREB蛋白水平對抗丙泊酚誘導的原代培養皮層神經元凋亡。Cyt-C在線粒體凋亡信號轉導途徑中發揮著重要的作用,Cyt-C釋放入細胞質是細胞凋亡發生的關鍵步驟。Cyt-C是線粒體呼吸鏈上的重要組成成分,生理狀態下Cyt-C存在于線粒體內,當刺激因子作用于細胞后線粒體通過多種離子轉運機制,導致內膜兩側離子濃度差的變化,引起線粒體膜電位的下降,使線粒體膜電位通透性增加,Cyt-C釋放入細胞質,進而激活天冬氨酸特異性半胱氨酸蛋白酶-3(caspase-3),引起細胞凋亡。本文Westernblotting結果顯示,與對照組比較,丙泊酚組Cyt-C蛋白水平明顯增加,與丙泊酚組比較,右美托咪定+丙泊酚組Cyt-C蛋白水平明顯下降,提示丙泊酚通過增加皮層神經元Cyt-C蛋白水平引起皮層神經元凋亡,而右美托咪定可通過降低Cyt-C蛋白水平對抗丙泊酚誘導的原代培養皮層神經元凋亡。
綜上所述,右美托咪定通過抑制丙泊酚引起的神經元pCREB蛋白水平的下降,降低Cyt-C蛋白水平,抑制丙泊酚誘導的原代培養皮層神經元凋亡。本研究為圍術期應用右美托咪定預防丙泊酚引起的發育期大腦損傷提供了初步的實驗依據和理論依據。
[1]HuangJ,JingS,ChenX,etal.Propofoladministrationduringearlypostnatallifesuppresseshippocampalneurogenesis[J],MolNeurobiol,2016,53(2):1031-1044.
[2]KarenT,SchlagerGW,BendixI,etal.Effectofpropofolintheimmatureratbrainonshort-andlong-termneurodevelopmentaloutcome[J].PLoSOne,2013,8(5):e64480.
[3]ZhongY,LiangY,ChenJ,etal.PropofolinhibitsproliferationandinducesneuroapoptosisofhippocampalneuronsinvitroviadownregulationofNF-κBp65andBcl-2andupregulationofcaspase-3[J].CellBiochemFunct,2014,32 (8):720-729.
[4]BernsM,SeebergL,SchmidtM,etal.High-dosepropofoltriggersshort-termneuroprotectionandlong-termneurodegenerationinprimaryneuronalculturesfromratembryos[J].JIntMedRes,2009,37(3):680-688.
[5]LiJ,XiongM,NadavaluruPR,etal.Dexmedetomidineattenuatesneurotoxicityinducedbyprenatalpropofolexposure[J].JNeurosurgAnesthesiol,2016,28(1):51-64.
[6]扈俊華,,梁羽冰,覃怡,等.右美托咪定預處理對丙泊酚孵育的大鼠海馬神經元細胞活力的影響[J].臨床麻醉學雜志,2013,29(5):488-490.
[7]LiJ,WuH,XueG,etal.17β-oestradiolprotectsprimary-culturedratcorticalneuronsfromketamine-inducedapoptosisbyactivatingPI3K/Akt/Bcl-2signalling[J].BasicClinPharmacolToxicol,2013,113(6):411-418.
[8]張曉青,賈建麗,馮明靜,等.右美托咪定減輕大鼠全腦缺血再灌注損傷[J].基礎醫學與臨床,2013,33(1):117-118.
[9]SifringerM,vonHaefenC,KrainM,etal.Neuroprotectiveeffectofdexmedetomidineonhyperoxia-inducedtoxicityintheneonatalratbrain[J].OxidMedCellLongev,2015(2015):530371.
[10]KooE,OshodiT,MeschterC,etal.Neurotoxiceffectsofdexmedetomidineinfetalcynomolgusmonkeybrain[J].JToxicolSci,2014,39(2):251-262.
[11]FanM,JinW,ZhaoH,etal.Lithiumchlorideadministrationpreventsspatiallearningandmemoryimpairmentinrepeatedcerebralischemia-reperfusionmicebydepressingapoptosisandincreasingBDNFexpressioninhippocampus[J].BehavBrainRes,2015(291):399-406.
[12]張英,吳新海,鄭利民.丙泊酚對大鼠海馬cAMP效應元件結合蛋白磷酸化和cAMP效應元件結合蛋白mRNA表達水平的影響[J].國際麻醉學與復蘇雜志,2011,32(3):303-307.
[13]梁羽冰,利莉,陳靜,等.丙泊酚或依托咪酯對大鼠海馬膠質纖維酸性蛋白表達的影響[J].廣東醫學,2012,33(3):303-305.
[14]韋祎,扈俊華,梁羽冰,等.右美托嘧啶對胎鼠離體海馬神經元CREB磷酸化表達的影響[J].中華麻醉學雜志,2014,34(11):1309-1311.
Dexmedetomidine inhibits propofol-induced apoptosis in primary cultured cortical neurons*
LiJianli1,YinDeyun2,WangYunxin1,WuHonghai3,HouYanning3
(1.DepartmentofAnesthesiology,HebeiGeneralHospital,Shijiazhuang,Hebei050051,China; 2.DepartmentofCardiology,HebeiGeneralHospital,Shijiazhuang,Hebei050051,China; 3.DepartmentofPharmacy,BethuneInternationalPeaceHospitalofChinesePLA,Shijiazhuang,Hebei050082,China)
Objective To investigate the mechanisms of the protective effects of dexmedetomidine against the propofol-induced neuroapoptosis in primary cultured cortical neurons.Methods The neurons were cultured for 7 days and treated with 500 μmol/L propofol and(or) different concentrations of dexmedetomidine,then were divided into the propofol treatment group,propofol+dexmedetomidine treatment group.The neurons in the control group were treated with 20% fat emulsion dissolved in the same solvent.12 hours after different treatments,neuron viability was measured by using MTT assay,neuroapoptosis was detected by using Hoechst33258 staining,and the levels of pCREB and Cyt-C protein were detected by using Western blotting.Results Compared with the control group,propofol inhibited neuron viability greatly,the neuroapoptosis increased greatly,the level of pCREB decreased greatly and the level of Cyt-C increased greatly,there were statistically significant differences(P<0.01).Compared with propofol treatment group,dexmedetomidine increased neuron viability greatly,the neuroapoptosis decreased greatly,the level of pCREB increased greatly and the level of Cyt-C decreased greatly,there were statistically significant differences.Conclusion Dexmedetomidine exerts the neuroprotective effects against propofol-induced neuroapoptosis,which may be associated with the increase of pCREB level and the decrease of Cyt-C level.
propofol;dexmedetomidine;primary cultured cortical neurons;apoptosis;phosphorylated cAMP response-element binding protein;cytochrome C
河北省衛生廳指令性課題資助項目(ZL20140095);2015年政府資助臨床醫學優秀人才培養和基礎課題研究項目(361003-6)。 作者簡介:李建立(1976-),副教授,博士,主要從事麻醉藥理學研究。
??·基礎研究
10.3969/j.issn.1671-8348.2016.35.005
R
A
1671-8348(2016)35-4911-03
2016-05-19
2016-08-07)

