基于“三重表征”方式設計的《酸的化學性質(zhì)》的教學研究
郭超琪
【摘要】 ?酸堿鹽的知識是初中化學學習最大的分化點。如何對酸堿鹽的知識進行有效教學,是個值得探討的問題。而《酸的化學性質(zhì)》是學生學習酸堿鹽知識的起點。本文以《酸的化學性質(zhì)》為例,將“宏觀——微觀——符號”的三重表征的思維方式應用于酸的化學性質(zhì)的學習中。探討如何運用“三重表征”的思維方式進行酸堿鹽的教學,幫助學生更好地建構酸堿鹽的知識。
【關鍵詞】 ?初中化學 三重表征 酸的化學性質(zhì) 分階段教學
【中圖分類號】 ?G633.8 ? ? ? ? ? ? ? ?? ?【文獻標識碼】 ?A ? ? ? ?? ? ? ? ? ? ? ?【文章編號】 ?1992-7711(2015)07-079-03
一、問題的提出
化學用語、溶液和酸堿鹽經(jīng)常成為初中化學學習的三個分化點,特別是酸堿鹽部分知識因其知識點多,知識點之間的聯(lián)系緊密,且與此相關的習題綜合性強,因此,酸堿鹽成為初中化學學習最大的分化點。初中酸堿鹽的知識與高中“離子反應”等知識聯(lián)系緊密,初三學生對酸堿鹽知識的學習與掌握,特別是對酸堿鹽反應本質(zhì)的理解,有利于其高中的后續(xù)學習。
筆者在參加近5年的廣州市教研中,廣州市教研員李南萍老師、戴光宏老師和王季常老師都強調(diào)要做好初高中的銜接,將化學知識的學習一體化,初中化學知識的學習要為學生高中化學知識的后續(xù)學習服務。
“酸堿鹽”的教學屬于元素化合物的學習。對于“酸堿鹽”的教學策略,如果運用“三重表征”方式進行教學,可能會收到事半功倍的效果。《酸的化學性質(zhì)》是學生認識酸堿鹽化學性質(zhì)的開始,應用“三重表征”方式對酸的化學性質(zhì)進行學習,不僅可以幫助學生更好地記憶和理解酸的化學性質(zhì),還可以幫助學生形成“三重表征”的思維方式來學習堿和鹽的化學性質(zhì)。本文以《酸的化學性質(zhì)》為例,探討如何運用“三重表征”的思維方式進行酸堿鹽的教學,幫助學生更好地建構酸堿鹽的知識。
二、理論基礎
1.“三重表征”的含義
化學是一門研究物質(zhì)的組成、結(jié)構、性質(zhì)和變化規(guī)律的科學,由于化學學科的特點,要求學生從不同的角度去認識物質(zhì)。畢華林教授認為化學學習的基本領域包括:①可觀察現(xiàn)象的宏觀世界;②分子、原子、離子等微粒構成的微觀世界;③化學式、方程式、元素符號構成的符號與數(shù)字世界。因而,要從宏觀、微觀和符號三種水平上認識和理解物質(zhì),并建立三者之間的內(nèi)在聯(lián)系,從而形成化學學科特有的思維方式。這種思維方式稱之為“三重表征”思維方式。
2.元素化合物教學“宏觀——微觀——符號”三重表征的構建方式
“三重表征”是化學中元素化合物教學的重要方法,能幫助學生通過物質(zhì)的各種表征方式進行有意義的學習。運用“三重表征”進行元素化合物的教學的基本程序是,首先通過閱讀材料、觀看多媒體素材、觀察與分析實驗現(xiàn)象或科學探究等活動獲得宏觀反應事實的認識;接著通過書寫化學方程式或離子方程式獲得符號表征;最后運用理論模型從微觀角度分析反應獲得微觀認識。
三、基于“三重表征”方式設計的《酸的化學性質(zhì)》的教學案例
1.教學內(nèi)容
此教學課例選取人民教育出版社初中化學第十單元“酸和堿”課題1“常見的酸和堿”第3課時“酸的化學性質(zhì)”為教學內(nèi)容,包括鹽酸、硫酸的化學性質(zhì),即鹽酸、硫酸能與指示劑作用、能與活潑金屬反應和能與金屬氧化物反應,以及鹽酸、硫酸具有相似化學性質(zhì)的原因。
2.教學目標
①知道酸溶液中都存在H+,推測酸具有一些相似的化學性質(zhì);
②通過分組實驗完成鹽酸、硫酸與指示劑的實驗,能夠說出鹽酸、硫酸與指示劑反應的現(xiàn)象,理解不同酸溶液能使酸堿指示劑顯現(xiàn)相同顏色的原因,建立酸與指示劑反應的三重表征。
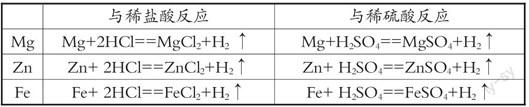
③通過回憶金屬與反應的條件,能夠說出Mg、Zn、Fe與鹽酸、硫酸的現(xiàn)象,寫出相應的化學方程式,理解不同酸溶液能與活潑金屬反應的原因,建立酸與金屬反應的三重表征。
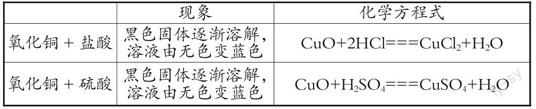
④觀察鐵銹、氧化銅與鹽酸、硫酸反應并說出反應的現(xiàn)象,寫出相應化學方程式,理解不同酸溶液能與金屬氧化物反應的原因,建立金屬氧化物與酸反應的三重表征。
⑤通過對酸化學性質(zhì)的學習,感受“組成(結(jié)構)決定性質(zhì)、性質(zhì)反映組成(結(jié)構)”的學科思想。
3.教學重難點
重點:酸的化學性質(zhì)
難點:利用微粒觀讓學生體會不同的酸具有相似的化學性質(zhì)的原因
4.教學過程
【引入】蝕刻工藝:酸吃掉金屬
環(huán)節(jié)1:酸在水溶液中都能電離出H+和酸根離子,推測酸具有一些共同的化學性質(zhì)
【提問】請同學們觀察實驗桌上所擺放的鹽酸和硫酸兩瓶無色溶液,你能說出它們的微觀組成嗎?
【討論】展示這兩種溶液的微觀示意圖,并討論以下問題:
(1)從物質(zhì)的類別看,它們是否屬于同類物質(zhì)?為什么?
(2)這兩種物質(zhì)是否會具有一些相似的化學性質(zhì)?
【微觀表征】陰離子分別是Cl-和SO42-.但陰離子都是H+,故它們都屬于酸。兩種溶液中都含有H+,所以推測它們可能會具有一些相似的化學性質(zhì)。
設計意圖:創(chuàng)設教學情境,引起學生學習的興趣。通過回憶鹽酸、硫酸的微觀組成,展示鹽酸、硫酸的微觀粒子圖,分析鹽酸、硫酸微觀組成的共同之處,使得學生在頭腦中形成鹽酸、硫酸這兩種物質(zhì)的“微觀表征”的表象。
環(huán)節(jié)2:通過學生分組實驗,引出酸化學性質(zhì)之一:能使酸堿指示劑顯示不同的顏色,建立酸與指示劑反應的三重表征
【分組實驗】鹽酸、硫酸分別與兩種指示劑的反應。
【宏觀表征】學生邊實驗邊記錄現(xiàn)象
【討論】兩種溶液都能使紫色石蕊溶液變紅色,無色酚酞溶液不變色,究竟是溶液中的哪種粒子引起的上述變化呢?
【微觀表征】鹽酸和硫酸兩種溶液中都含有的H+,應該是H+引起的變化。
設計意圖:學生通過分組實驗,獲得鹽酸、硫酸與石蕊、酚酞反應的“宏觀現(xiàn)象”,通過回憶鹽酸、硫酸的微觀組成,討論鹽酸、硫酸為什么能使紫色石蕊溶液變紅色,無色酚酞溶液不變色。實現(xiàn)由“宏觀表征”到“微觀表征”的轉(zhuǎn)換,學會從微觀的角度解釋宏觀現(xiàn)象。
環(huán)節(jié)3:通過游戲回憶金屬與酸反應的條件,引出酸化學性質(zhì)之一:酸能與活潑金屬反應,建立酸與活潑金屬反應的三重表征
【游戲】“尋找灰太狼”的游戲回憶金屬與酸反應的條件
【宏觀——符號表征】回憶鎂、鋅、鐵與鹽酸、硫酸反應的現(xiàn)象,并書寫鎂、鋅、鐵與鹽酸、硫酸反應的化學方程式
【討論】上述反應的反應物和生成物有什么共同之處?
【宏觀表征】反應物都是金屬和酸,生成物都有氫氣
【教師小結(jié)】鎂、鋅、鐵等活潑金屬能與鹽酸、硫酸反應生成氫氣,說明酸能與氫前的金屬發(fā)生置換反應。
【討論】鹽酸、硫酸都可以與活潑金屬反應產(chǎn)生氫氣。究竟是酸溶液中的哪種粒子引起的上述變化呢?
【微觀表征】鹽酸和硫酸兩種溶液中都含有的H+,應該是H+引起的變化。
設計意圖:通過“尋找灰太狼”的游戲回憶金屬與酸反應的條件,回憶鎂、鋅、鐵與鹽酸、硫酸反應的現(xiàn)象,書寫鎂、鋅、鐵與鹽酸、硫酸反應的化學方程式,實現(xiàn)由“宏觀表征”到“符號表征”的轉(zhuǎn)換,通過討論鹽酸、硫酸為什么都能與活潑金屬反應,實現(xiàn)由“宏觀表征”到“微觀表征”的轉(zhuǎn)換。
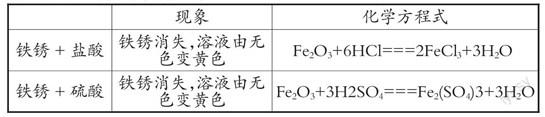
環(huán)節(jié)4:觀察鐵銹與鹽酸、硫酸的反應,建立堿與非金屬氧化物反應的三重表征
【學生回憶】鐵生銹會產(chǎn)生哪種物質(zhì)?化學式是什么?在物質(zhì)的分類中屬于什么?
【教師設問】當鐵銹遇到稀鹽酸,會發(fā)生反應嗎?
【學生可能的回答】可能會反應
【演示實驗】鐵銹與鹽酸、硫酸分別發(fā)生反應
【宏觀——符號表征】請同學們描述所觀察到的現(xiàn)象并試著寫出反應的化學方程式
【教師講述】鹽酸、硫酸不僅可以與鐵銹發(fā)生反應,還可以與氧化銅發(fā)生反應
【補充實驗】氧化銅與鹽酸、硫酸分別發(fā)生反應
【宏觀——符號表征】請同學們描述所觀察到的現(xiàn)象并試著寫出反應的化學方程式
【討論】上述反應的反應物和生成物有什么共同之處?
【學生可能的回答】反應物都是金屬氧化物和酸,生成物都有水。
【宏觀表征】金屬氧化物能與鹽酸、硫酸反應生成水。
【討論】鹽酸、硫酸都可以與金屬氧化物反應產(chǎn)生水。究竟是酸溶液中的哪種粒子引起的上述變化呢?
【微觀表征】鹽酸和硫酸兩種溶液中都含有的H+,應該是H+引起的變化。
【討論】利用上面的反應可以清除鐵制品表面的銹,除銹時能否長時間浸在酸中?為什么?
【學生可能回答】不能;當鐵釘表面的鐵銹被清除完,酸將與鐵發(fā)生反應。會腐蝕金屬。
設計意圖:學生通過觀察實驗現(xiàn)象獲得對鐵銹、氧化銅與酸反應的“宏觀表征”,通過書寫反應的化學方程式獲得鐵銹、氧化銅與酸反應“符號表征”,最后通過討論為什么鹽酸、硫酸都能與金屬氧化物反應,實現(xiàn)“宏觀表征”與“微觀表征”的切換。
環(huán)節(jié)5:總結(jié)酸的化學性質(zhì),知道酸具有相似化學性質(zhì)的原因:酸溶液中都有H+
【微觀——宏觀表征】由于不同的酸溶液中都含有相同的H+,因而具有一些相同的化學性質(zhì)
1. 酸溶液能使酸堿指示劑顯示不同的顏色
2. 酸溶液能與活潑金屬反應
3. 酸溶液與金屬氧化物反應
【練習】“蝕刻”福娃印刷模板
“蝕刻”是制作印刷模板的一種方法.現(xiàn)用“蝕刻”的方法制作“福娃”的印刷模板,制作過程如下:
①用稀鹽酸除去金屬板表面的“銹斑”,再進行打磨處理;
②在金屬板上鍍一層防酸材料——蜂蠟;
③在上面刻出“福娃”圖象;
④用稀鹽酸對其表面進行處理,稀鹽酸就能“吃掉”金屬;
⑤除去蜂蠟鍍層,金屬板上顯出“福娃”。
根據(jù)上述制作過程回答下列問題:
(1)制作印刷模板的金屬可選用 ? ? ? ? ? ? (選填“鐵”、“銀”或“銅”)。
(2)制作此模板依據(jù)的原理是 ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ?。
(3)寫出制作過程①中發(fā)生反應的化學方程式
。
設計意圖:通過總結(jié)酸的化學性質(zhì),使得學生在頭腦中建立起酸的化學性質(zhì)的認知圖式,建立起酸的化學性質(zhì)的三重表征。習題的設計呼應課前創(chuàng)設的情景,也是學生對酸的化學性質(zhì)的鞏固。
四、基于“三重表征”方式設計的《酸的化學性質(zhì)》的分階段教學
新課的教學是對酸的化學性質(zhì)學習的第一階段,學生學習了這節(jié)課之后在學生的腦中對酸的化學性質(zhì)會留有這樣的印象:鹽酸、硫酸之所以有共同的化學性質(zhì)是因為它們的水溶液中都有H+。例如,2012年廣州市中考題第25題就是對酸的共性的考查。題目中首先讓學生書寫三氧化二鐵與鹽酸反應的化學方程式和現(xiàn)象,再告訴學生白醋、檸檬酸溶液也能與三氧化二鐵發(fā)生類似反應,讓學生從微觀角度解釋反應的原因。
例1:實驗室有鹽酸、白醋、檸檬酸三種溶液,回答下列問題:
(1)向三氧化二鐵中放入足量鹽酸,充分反應后,觀察到的現(xiàn)象是 ? ? ? ,
反應的化學方程式是 ?? ? ?。
(2)白醋、檸檬酸溶液也能與三氧化二鐵發(fā)生類似反應,說明白醋、檸檬酸溶液和鹽酸中都含有的離子是 ? ?? ?。
大部分學生在學習新課之后,對酸的共性的理解并不存在障礙。但是對酸的個性的理解是存在障礙的。因此,酸的化學性質(zhì)第三階段的學習就是對酸的個性通過習題進行鞏固練習,適合在中考復習課中進行。教師可以設計幾道對酸共性和個性考查的題目,學生通過對比來學習酸的共性和個性。例如,2013年廣州市中考題第21題就是對酸的共性和個性的考查。題目中首先讓學生書寫稀硫酸與鐵粉、碳酸鈉和氯化鋇的化學方程式,再讓學生選出哪些反應屬于酸的共同的化學性質(zhì)。要正確地解答這道題,學生必須要思考一個問題:硫酸的化學性質(zhì)是否全部都是因為H+引起的。硫酸在水溶液中不僅可以電離出H+還可以電離出SO42-.其實硫酸與氯化鋇之所以能夠發(fā)生反應中,是因為生成了BaSO4白色沉淀。所以,“SO42-”才是正真的主角。
例2:硫酸、鹽酸是重要的化工原料。
(1)濃硫酸在實驗室常用作干燥劑,因為濃硫酸有 ? ? ?性。
(2)寫出稀硫酸與下列物質(zhì)反應的化學方程式:
①與鐵粉反應: ?? ? ?;
②與碳酸鈉溶液反應: ?? ? ;
③與氯化鋇溶液反應: ? ? ? ?;
上述反應中,屬于酸的共同性質(zhì)的是 ? ?? ?(填編號)
(3)鹽酸的下列用途中,不能用硫酸代替鹽酸的是 ? ? ? ?(填編號)
①金屬表面除銹②制造藥物氯化鋅③除去NaCl中的少量NaOH
無論是對酸的共性的分析,還是對酸的個性的分析,學生都可以運用“宏觀——微觀——符號”的三重表征方式進行。主要的分析過程為:先寫出反應的化學方程式(符號表征),再描述出反應的現(xiàn)象(宏觀表征),再根據(jù)方程式和現(xiàn)象,從微觀角度來分析產(chǎn)生宏觀現(xiàn)象的原因(微觀表征)。
五、基于“三重表征”方式設計的《酸的化學性質(zhì)》的教學思考
酸的化學性質(zhì)的教學采用“三重表征”的方式進行,讓學生通過不同角度對酸的化學性質(zhì)進行了意義建構,有利于他們對酸的化學性質(zhì)的整體理解和把握。“三重表征”教學同樣適用于“堿的化學性質(zhì)”、“中和反應“和“鹽的化學性質(zhì)”的教學。
通過第一階段《酸的化學性質(zhì)》的新課學習和第二階段酸的共性的習題鞏固,學生初步形成“宏觀——微觀——符號”的三重表征的思維方式,那么,在堿和鹽化學性質(zhì)的學習中,學生就可以遵循三重表征的思維方式去學習堿和鹽的共性。
《酸的化學性質(zhì)》應用“宏觀——微觀——符號”的三重表征的思維方式進行教學,堿和鹽的化學性質(zhì)的學習是對酸的化學性質(zhì)學習方式的延續(xù)和鞏固。相對固定的教學模式,有利于培養(yǎng)學生形成“宏觀——微觀——符號”的三重表征的思維方式,幫助學生從不同角度對酸堿鹽的知識進行建構,啟發(fā)學生形成酸堿鹽的學習思路,突破酸堿鹽的學習難點。
(此論文是廣東教育學會2014年度教育科研規(guī)劃小課題(課題編號:GDXKT2927)的研究成果)
[ 參 ?考 ?文 ?獻 ]
[1]畢華林,黃婕.國外關于化學學習水平的界定與研究進展[J].全球教育展望.2007.
[2]紀新慧.高中生化學三重表征思維方式的培養(yǎng)研究[D].山東師范大學.2009.
[3]葉靜怡.“酸堿鹽”的分階段模式支持下的有效教學[J].中學化學教學參考.2011.
[4]郭建虹.初中化學酸堿鹽教學策略有效性的研究[J].中學化學教學參考.2013.
[5]李友銀,蒲緒鳳.基于三重表征方式設計“鋁的重要化合物”教學[J].中學化學教學參考.2011.
[6]課程教材研究所.義務教育課程標準實驗教科書·化學九年級下冊[M].人民教育出版社:2012.
[7]廣州市教育局教學研究室.廣州市義務教育階段學科學業(yè)質(zhì)量評價標準.廣東省出版集團:2013.

