腦脊液引流治療主動脈夾層術后脊髓損傷8例*
楊小芳,劉瑞生,李元敏
(蘭州大學第一醫院心血管外科,甘肅 730000)
主動脈夾層(AD)是危重心血管疾病之一。主動脈內膜破裂引起血液大量流入撕裂處,導致中層和內層分離,最終形成AD。根據國際常用的Stanford分型將AD分為A型(TAAD)和B型(TBAD),分別累及升主動脈和降主動脈[1]。AD的主要治療方法為開胸手術和血管內主動脈修復(TEVAR)術。近年來,手術方法和術后診斷的發展提高了術后患者存活率。然而脊髓損傷(SCI)仍然是主動脈修復術后最常見和最嚴重并發癥之一。TAAD患者開胸手術后SCI發生率可高達20%[2]。在TEVAR術后發生SCI的風險尚未完全確定,據文獻報道,發生率為2%~12%[3-4]。SCI可表現為截癱、知覺喪失或尿便失禁,可顯著降低患者生活質量[5]。此外,術后發生SCI患者在術后病程中病死率顯著增加,除年齡和術后急性腎衰竭外,截癱也是死亡率的重要預測因素之一[6]。
既往研究表明,腦脊液(CSF)引流對SCI的預防和治療均具有顯著效果[7-9]。SCI早期治療中單用升高血壓治療或結合CSF引流對大多數患者有效,大多數患者實現了完全或長期的神經功能恢復[6、10]。然而現有的研究樣本量均很少,有效的循證醫學證據不足。本研究發現AD術后CSF引流具有有效的治療作用,現報道如下。
1 資料與方法
1.1 一般資料
選取2011年1月至2021年4月本院心血管外科收治的行AD手術(包括開放性手術440例和介入手術191例)患者631例,8例患者術后發生SCI,均行CSF引流,8例患者中男7例,女1例;年齡32~61歲;TAAD 6例,TBAD 2例;手術方式:開放7例,介入1例;SCI發生時間:即刻(麻醉蘇醒后即發現)5例,延遲(術后24 h以上才發現)3例;累及肋間動脈4例,術前平均動脈壓(MAP)<90 mm Hg(1 mm Hg=0.133 kPa)4例,伴高血壓6例,術前下肢運動及感覺異常1例,均為急性期。
1.2 方法
1.2.1治療方法
8例患者中行全胸腹主動脈置換術2例,行升主動脈置換、全主動脈弓置換聯合象鼻支架植入術3例,行升主動脈置換(Bentall術)、全主動脈弓置換聯合血管內主動脈修復(TEVAR)術2例,介入行單純TEVAR術1例。1例患者術前存在SCI,因此在術中行CSF引流,其他患者在術后麻醉清醒后常規評估肢體功能,每4小時1次,發現異常后立即行CSF引流術。操作方式:于 L3~4或L4~5 腰椎間隙進行穿刺,測量CSF壓力后留置引流管,持續引流CSF。CSF引流期間去枕平臥,禁止抬高床頭。集液器位于脊柱平面以上至少10 cm,通過調節其高度嚴格控制引流速度,不超過 10~15 mL/h,全天引流量小于300 mL。CSF引流術后7 d或患者肌力恢復后拔除引流管。發生SCI患者均維持MAP>90 mm Hg,并給予脫水、激素沖擊、營養神經、間斷高濃度吸氧等治療。輔以肢體功能康復訓練及針灸治療。
1.2.2隨訪
8例患者術后隨訪6~24個月。
2 結 果
AD術后SCI發生率為1.27%(8/631),開胸手術后SCI發生率為1.59%(7/440),TEVAR術后SCI發生率為0.52%(1/191)。隨訪期間6例患者于截癱后4~11 d肌力基本恢復,其中3例患者出院后繼續進行康復訓練,1年后下肢肌力及感覺恢復,生活可自理;2例患者雙下肢肌力及感覺未恢復,診斷為永久性截癱(其中1例為術中行CSF的患者)。8例患者均未出現CSF引流相關并發癥。1例永久性截癱患者于出院后6個月因肝癌死亡。手術方式及患者預后見表1。
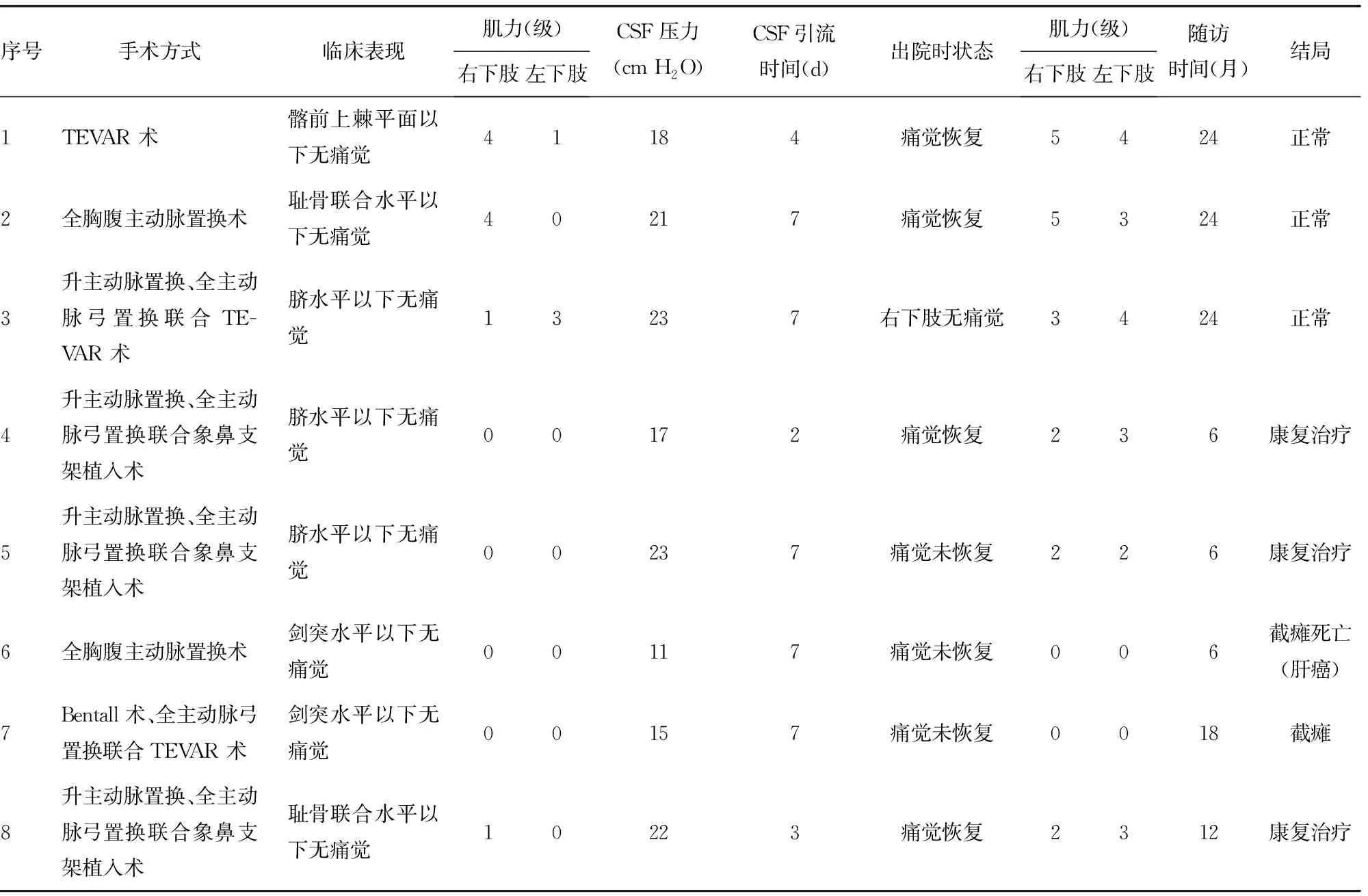
表1 手術方式及患者預后(n=8)
3 討 論
隨著診斷技術和手術方法的改進,AD術后并發癥發生率逐年降低,生存率提高。然而,SCI仍是影響患者生活質量的嚴重并發癥之一。TEVAR術后SCI發生率低于開胸手術[6-7,11],與本研究結果相同。目前,AD術后發生SCI的具體病理生理機制尚不清楚,可能是一個動態的、復雜的過程。此外,其致病因素多種多樣,可能發生在主動脈修復手術前、期間或術后[7,10,12-14]。有研究表明,SCI癥狀的緩解可顯著影響急性TAAD和急性TBAD患者的總體存活率[15]。SCI的預防和治療包括維持圍手術期高血壓、CSF引流、左鎖骨下動脈血運重建和藥物治療等[9]。
以往研究表明,CSF引流是治療SCI的有效方法,但是在術前、術中還是術后進行CSF引流仍存在爭議[10、16-20]。神經生理監測可用于早期發現和治療SCI,但其效用受醫護人員因素和少數術中SCI患者的限制[21]。而術前常規放置CSF引流管可避免CSF引流延遲安置而致患者術后的突然癱瘓[22]。 DESART等[23]進行了607例TEVAR患者的隊列研究,其中57例(9.4%)患者發生了某種程度的SCI,54例(94.7%)患者在護理過程中接受了CSF引流,其中術后行CSF引流患者為31例(54.4%)。但KITPANIT等[24]研究表明,常規預防性CSF引流可能不合理,因預防性CSF引流相關并發癥發生率超過了SCI發生率,并且CSF引流顯著增加了重癥監護病房和總住院時間。因此,CSF引流管放置時機對出院后功能損害或長期并發癥的影響尚不明確。2010年美國心臟病學會基金會/美國心臟協會指南建議CSF引流用于開放性TAAD修復術中的脊髓保護[25]。2015年歐洲心胸外科協會同樣建議將CSF引流用于SCI高危患者TAAD的修復[26]。根據指南建議,本研究在術后密切監測患者下肢肌力和感覺,一旦出現SCI臨床表現立即進行CSF引流,效果良好。
發生SCI患者的康復效果與損傷嚴重程度有關[27]。本研究中1例患者術前即出現SCI,在術中留置引流管,但未獲得良好效果,其原因可能與損傷時間較長、損傷程度較重有關。術中低血壓是SCI發生的獨立危險因素,長時間低灌注可能導致不可逆損傷。本研究中2例永久性截癱患者即考慮圍術期血壓持續偏低,引起脊髓低灌注造成長時間缺血所致。有研究提示,CSF引流對顱內壓低的患者效果不佳[28]。本研究中2例永久性截癱患者穿刺后測壓明顯低于其他6例患者。因此,發生SCI后監測顱內壓偏低則可能提示患者預后不良。
CSF引流是一種侵入性操作,可能會引起一些并發癥。HANNA等[29]報道了81例TEVAR患者CSF引流并發癥發生情況,9例(11.1%)患者發生輕微CSF引流并發癥,包括頭痛、穿刺部位出血、持續性CSF漏或硬膜下血腫等。但一項類似研究結果顯示,48例患者在放置CSF引流管期間沒有出現并發癥[30]。存在這種差別的原因可能是放置導管的時機(TEVAR術前24 h),以及在留置及取出引流管時嚴格的抗凝管理。另外有研究發現,進行預防性CSF引流的患者中7.6%發生了CSF引流相關的主要并發癥,包括2.6%的蛛網膜下腔出血、2.6%的脊髓血腫、1.3%的小腦出血和1.3%的需要椎板切除的脊髓引流骨折[23]。本研究中7例患者均在術后發生SCI即刻留置CSF引流管,并在留置引流管后進行嚴格抗凝管理,未出現CSF引流術后并發癥。
綜上所述,SCI在AD術后仍有較高的發生率。在術后初期減少鎮痛鎮靜藥物的使用并密切觀察患者病情變化,發現SCI后即刻行CSF引流,75%的患者獲得了良好效果,且8例患者均未出現CSF引流術后并發癥。因此,CSF引流聯合嚴格的抗凝管理、激素沖擊、營養神經及合理的康復治療,可對AD術后SCI患者起到良好效果,改善其生活質量。

