結直腸息肉切除術后復發的臨床特點及相關因素
蒯亞仙,李 楊,徐建華,王 旭,孫 斌
2021年全球結直腸癌新發病例占惡性腫瘤發病率10.0%,位列第3位;結直腸癌病死率例占惡性腫瘤病死率9.4%,位列第2位[1]。在我國,最新發布的全國癌癥統計數據顯示,結直腸癌的發病率位列第2位,病死率位列第4位,發病率逐年上升[2]。結直腸息肉是結直腸癌最重要的癌前病變,結腸鏡檢查中對息肉的切除可以減少結腸直腸癌(colo-rectal carcinoma,CRC)總病死率[3]。息肉最常見的類型是腺瘤,腺瘤的數量是結直腸癌的重要風險因素,因此患有多發息肉的人群是臨床工作中重點關注的對象。結腸息肉漏診是導致間期結腸癌的風險因素[4-5],對于已經行結腸鏡檢查及息肉切除治療的患者,第2次結腸鏡檢查中如何降低漏診概率、識別息肉復發的高風險因素尤為重要。該文旨在對結直腸息肉切除后復發的特點進行研究,為息肉復發的臨床風險評估工作提供依據。
1 材料與方法
1.1 病例資料選取2016年10月—2021年11月在安徽醫科大學第一附屬醫院消化內鏡中心接受結腸鏡檢查的患者370例。記錄患者性別、年齡、內窺鏡圖像特征及病理資料等數據,所有結腸鏡檢查及治療均由有經驗的內窺鏡醫師(具有5年以上工作經驗,結腸鏡檢查工作量>500次/年)進行。
1.1.1納入標準 ① 至少進行過2次結腸鏡檢查,2次檢查的時間間隔至少6個月,且第2次結腸鏡檢查發現至少一處息肉復發;② 結腸鏡檢查中發現的所有息肉都應通過內鏡治療完全切除,且患者病歷資料記錄完整;③ 首次結腸鏡檢查并行內鏡下切除術之前6月內患者至少在該院或者外院進行過1次結腸鏡檢查,確認存在結腸息肉;④ 每次檢查及治療均行完整結腸鏡檢查,完整的結腸鏡檢查指所有到達盲腸的結腸鏡檢查;⑤ 結腸鏡下息肉切除術應獲得所切息肉組織病理學的完整資料。
1.1.2排除標準 ① 有家族或個人有遺傳性息肉綜合征病史、炎癥性腸病、缺血性腸病或個人CRC病史;② 結腸外科手術史;③ 新發現CRC患者;④ 未完成完整的結腸鏡檢查。
1.2 研究內容將每次術前6個月內完成的結腸鏡檢查定義為初篩,作為高質量結腸鏡檢查的依據。將行內鏡下切除治療的兩次結腸鏡檢查定義為首次和第2次結腸鏡檢查。依據第2次結腸鏡復查復發息肉數量是否超過3枚,分為多發性復發組(復發息肉數量≥3枚)和非多發性復發組(復發息肉數量<3枚)[6],在本研究過程中,回顧所有的結腸鏡檢查資料和病理報告,并收集有關息肉的顏色、數量、大小、位置、形狀、切除方式和病理以及患者的年齡、性別和檢查時間、腸道準備情況的資料,并分別進行統計分析。
1.3研究方法① 用打開的活檢鉗(6 mm)估計息肉的大小,或在切除后測量,大小單位為cm;② 位置分為近端結腸(盲腸、升結腸、肝曲、橫結腸和脾曲),遠端結腸(降結腸、乙狀結腸和直腸);③ 根據Paris內鏡分類將息肉的形狀分為隆起型(Ⅰp、Ⅰs、Ⅰsp)和表淺型(0-Ⅱa、0-Ⅱb、0-Ⅱc);④根據世界衛生組織推薦的結腸直腸癌分級標準,將病理分類為腺瘤型(管狀腺瘤、絨毛狀腺瘤)和非腺瘤型(傳統鋸齒狀息肉、炎性或增生性息肉及其他類型),以及是否存在絨毛狀組織;⑤切除方式分為冷切除和熱切除,其中冷切除包括活檢鉗夾除和圈套器切除,熱切除包括電凝、內鏡下黏膜切除術(EMR)、內鏡下黏膜剝離術(ESD);⑥多發性息肉患者的大小、位置和組織學類型分別根據最大、最近端和最晚期病變進行分類;⑦色澤分為發紅與非發紅。

2 結果
2.1 基本資料篩選出15 627例完整結腸鏡檢查有結直腸息肉的患者資料,已行內鏡下結直腸息肉切除術的有6 176例患者,僅1 551例患者接受2次及以上的內鏡下結腸息肉切除術,其中31例患者結腸鏡檢查間隔不足半年,138例患者患有炎癥性腸病、家族性腺瘤性息肉病或Peutz-Jeghers綜合征,300例患者有結直腸癌病史,20例患者有結直腸外科手術史,110例患者在復查中新發現了癌性病變,582例患者病理資料不全,最終在370例符合條件的患者中,依據第2次結腸鏡結果,復發息肉數量是否超過3枚,分為多發性復發組(復發息肉數量≥3枚,)和非多發性復發組(復發息肉數量<3枚)。
2.2 兩組患者基本特征統計分析非多發性復發組314例,其中男性245例,女性69例,結腸鏡檢查時年齡為22~82(53.50±10.87)歲,兩次檢查時間間隔477(359,760)d,首次檢查和第2次檢查息肉個數分別是2(1,2)、1(1,2)個,波士頓腸道評分(the Boston bowel preparation scale,BBPS)分別為(6.28±1.54)分和(6.54±1.32)分;多發性復發組56例,其中男性47例,女性9例,結腸鏡檢查時的平均年齡為28~75(56.38±10.25)歲,兩次檢查時間間隔490(375,997)d,首次檢查和第2次檢查息肉個數分別是2(1,4)、3(3,4)個, BBPS分別為(6.43±1.49)、(6.46±1.32)分。對兩組總特征統計分析,其中非多發性復發組首檢息肉數2(1,2),多發性復發組首檢息肉數2(1,4),P=0.001,即多發性復發與首次結腸鏡檢查時息肉數量有關,首次檢查中發現并切除的息肉數量越多,越容易出現多發性復發。見表1。
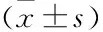
表1 非多發性復發組和多發性復發組基本特征的比較
2.3 首次結腸鏡檢查結果統計分析首次結腸鏡檢查中非多發性復發組與多發性復發組息肉數量分別為582、143個,兩組息肉大小分別為0.6(0.4,1.0)、0.6(0.5,1.0) cm,息肉部位分析中左半結腸占比分別為0.70、0.59,兩組腺瘤占比分別為0.68、0.71,存在絨毛狀成分的占比分別為0.06、0.06,熱切除占比分別為0.05、0.60,隆起型息肉占比分別為0.09、0.08,發紅息肉占比分別為0.81、0.89。在單因素統計分析中,息肉大小(P=0.033)、息肉部位(P=0.002)、息肉色澤(P=0.032)是息肉多發性復發的風險因素,在左半結腸、較大的息肉、顏色發紅的息肉更容易出現多發性復發。在多因素回歸分析中,息肉的部位是多發性復發的獨立風險因素,P=0.001,左半結腸更容易出現多發性復發,其中乙狀結腸發生多發性復發的比例最高。見表2。
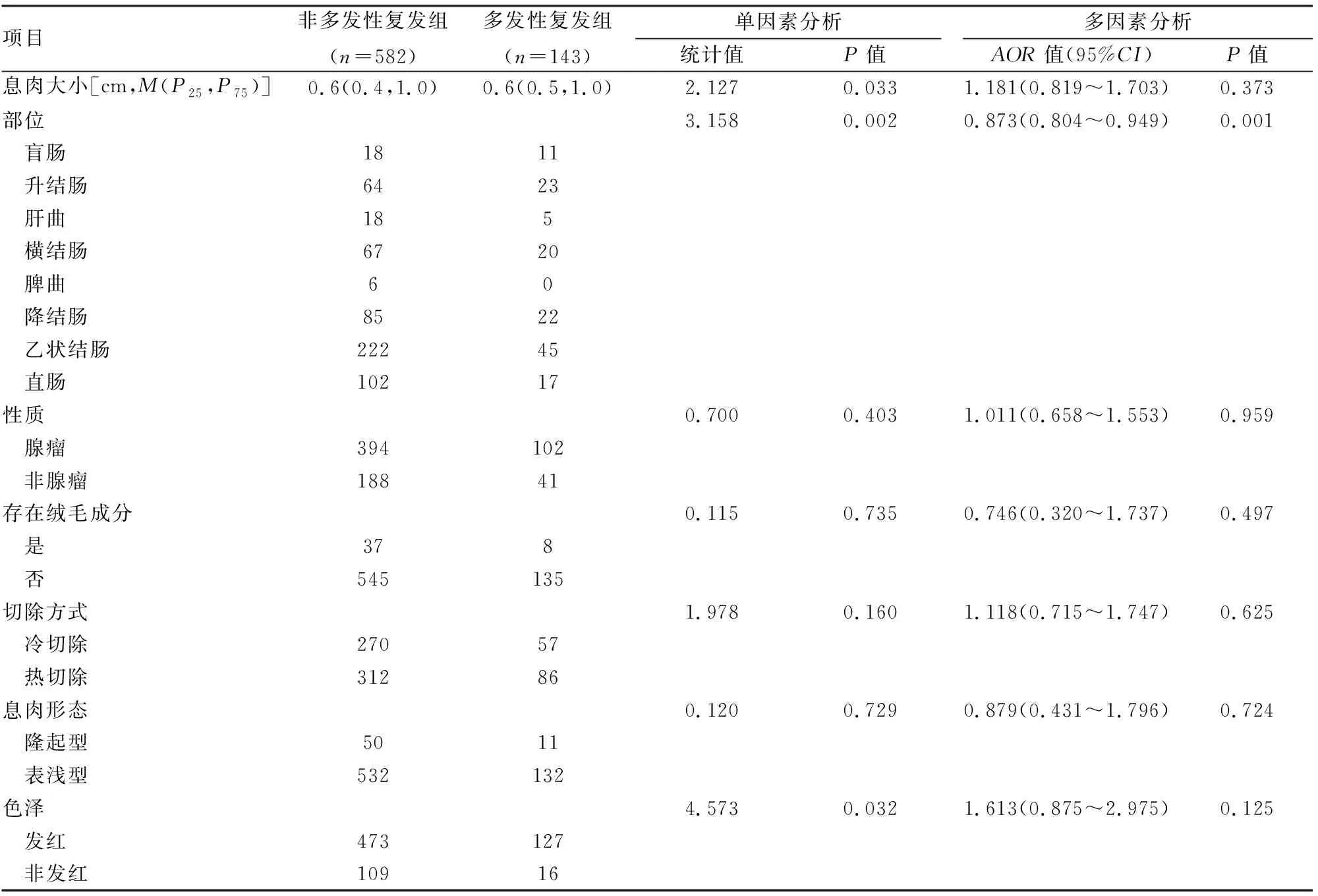
表2 非多發性復發組和多發性復發組首次結腸鏡檢查結果的比較(n)
2.4 第2次結腸鏡檢查結果統計分析第2次結腸鏡檢查中非多發性復發組的息肉數量為405個,多發性復發組的息肉數量為189個,息肉大小分別為0.5(0.4,0.6)、0.5(0.4,0.7) cm,息肉部位分析中左半結腸占比兩組分別為0.62、0.60,腺瘤占比分別為0.53、0.59,存在絨毛狀成分的占比分別為0.02、0.04,熱切除占比分別為0.21、0.36,隆起型息肉占比分別為0.16、0.15,發紅息肉占比分別為0.71、0.74。在單因素統計分析中,分別采用Mann-WhitneyU檢驗及皮爾森卡方檢驗統計結果顯示,息肉大小(P=0.008)、切除方式(P<0.001)是息肉多發性復發的相關因素;在多因素回歸分析中,切除方式是多發性復發的獨立相關因素(P=0.001),說明多發性復發組的息肉直徑較大,而治療息肉時更多地采用熱切除方法。見表3。
表3 非多發性復發組和多發性復發組第2次結腸鏡檢查結果的比較(n)
3 討論
定期檢查發現結直腸息肉復發是預防結直腸癌發生的關鍵,2020年發表的美國最新共識中提示,息肉切除后的監測和檢查要根據息肉患者所檢出息肉的組織學、數量、位置和大小進行風險分層,其中腺瘤數量≤2的小腺瘤為低危組,而根據不同的風險分層,結腸鏡檢查的監測間隔各不相同,其中最短的監測間隔為6個月,故本研究中以此作為納入和分組的標準[4]。比較兩組患者在兩次結腸鏡檢查中的腺瘤占比,雖然復查中都有所降低,但腺瘤性息肉依舊占據主導地位,近年來發表的研究表明,在隨訪中,多個腺瘤患者發生進展期腺瘤的風險增加,甚至發生結直腸癌的風險增加[7-8],這就使得對結直腸息肉切除后的多發性復發研究更具有意義。
通過統計分析,本研究得出首次結腸鏡檢查中息肉的數量是息肉切除后多發性復發的獨立風險因素。首次結腸鏡檢查中發現并切除的息肉數量越多,越容易發生多發性復發,這與Pommergaard et al[7]研究結果一致。Pommergaard指出息肉切除術后多發性復發除了與患者的個人體質、生活飲食習慣相關外,還與息肉的不完全切除率有關。近來高質量研究[9-10]也表明,隨著息肉切除數量的增加,由不完全切除導致的復發風險也在增加,成為多發性復發的風險因素之一。本研究在對首次結腸鏡檢查的單因素分析中提示,多發性復發與首次檢查中息肉的大小和色澤也具有相關性,Hao et al[6]研究指出越大的息肉不完全切除率越高,且可能含有的進展期腺瘤可能性越大,而發紅的息肉也更容易被發現,這與本研究結果相一致,但是在多因素回歸分析中,息肉大小和色澤的相關風險因素沒有統計學意義。本研究另一個結果是息肉切除后的多發性復發與息肉的位置有關,在第2次結腸鏡檢查中,兩組息肉部位分析中左半結腸占比都達半數以上,而多發性復發組的左半結腸息肉占比0.62以上,故左半結腸息肉更容易出現多發性復發,這與Alecu et al[11]研究結果一致。該結論與其他研究中右半結腸容易出現息肉復發的結論并不矛盾,右半結腸因其解剖位置及息肉類型的特殊,更容易發生漏診和息肉的復發,而本研究中兩次治療前均予以至少一次的結腸鏡檢查,因而減少了右半結腸的漏診,乙狀結腸、直腸更容易出現增生性息肉,故發生多發性復發的可能性更大。
本研究還對其他P>0.05的因素進行了統計分析,兩組中具有絨毛狀組織的息肉占比相當,但是在第2次結腸鏡復查中多發性復發組中絨毛狀組織的占比明顯高于非多發性復發組,雖然P=0.077,由于具有絨毛狀組織的腺瘤被認為是具有進展期腺瘤特征[4],因此在臨床工作中更應對其做出妥善處理,防止復發,甚至導致結直腸癌的發生。近年來研究[9、12-15]表明男性、≥60歲、基線結腸鏡檢查中進展期腺瘤、切除方式等與復發相關,但本研究的結果沒有發現這些相關性,除了研究主題有區別外,還可能因本研究是單中心的回顧性研究,存在選擇偏倚,數據量不夠大、時間間隔短等原因,后期應繼續擴大研究的數量和范圍,用大量的隊列研究來闡明息肉切除后復發的特點,得出更加科學的結論。
總之,首次結腸鏡檢查中息肉的數量和息肉的部位是息肉切除后多發性復發的獨立風險因素,結腸鏡下發現并切除的息肉數量越多,越容易發生息肉的多發性復發,左半結腸也更容易出現息肉的多發性復發。因此,對于多發性息肉患者,尤其是息肉數量≥3的患者,應當為其提供個體化的結腸鏡復查方案。

