地西他濱聯合CAG方案治療復發難治性AML的臨床效果及安全性分析
李 娜
〔太原鋼鐵(集團)有限公司總醫院血液科,山西 太原 030003 〕
復發難治性急性髓系白血病(acute myeloid leukemia,AML)屬于一類遺傳學高度異質性血液系統惡性疾病。該病的治療難度大、易復發。其原因主要為,白血病細胞的細胞膜上有一種特殊的糖蛋白,可降低白血病細胞內藥物的濃度,使藥物無法滅殺白血病細胞[1]。目前,臨床上尚無公認的治療復發難治性AML 的有效方案。由阿糖胞苷、阿克拉霉素及粒細胞集落刺激因子三種藥物組成的CAG 方案是一種將化療、誘導分化治療和誘導凋亡治療有機結合,并能產生明顯藥物協同效應的化療方案,多用于治療各種預后不良的AML。但由于該病患者存在個體差異,故用CAG 方案對其進行治療也無法達到預期的臨床效果[2]。地西他濱是天然2’-脫氧胞苷酸的腺苷類似物,有抑制腫瘤細胞增殖的作用,且較少引起腫瘤細胞耐藥[3]。本研究主要是探討用地西他濱聯合CAG 方案治療復發難治性AML對患者免疫功能的影響及安全性分析。
1 資料與方法
1.1 一般資料
選取2017 年4 月至2021 年2 月太原鋼鐵(集團)有限公司總醫院收治的40 例復發難治性AML 患者為研究對象。本次研究對象納入標準:1)其病情符合《復發難治性急性髓系白血病中國診療指南(2017 年版)》[4]中的相關診斷標準。2)其精神及感知功能正常。3)對其進行實驗室檢查的結果確診其患有AML。其排除標準:1)合并有其他的血液系統疾病。2)合并有免疫系統缺陷或內分泌系統病變。3)合并有重要器官的疾病或缺陷。4)合并有其他的惡性腫瘤。用隨機數表法將40 例患者均分為對照組和治療組。對照組20 例患者中有男11 例,女9 例;其年齡為49 ~77 歲,平均年齡(65.37±7.24)歲;用FAB 分類法〔由法國(French)、美國(American)、英國(British)在1976 年提出的關于急性白血病的分型診斷標準〕對其病情進行分型的結果顯示:有2 例M1 型患者,有1 例M2 型患者,有3 例M4 型患者,有12 例M5 型患者,有2 例M6 型患者。治療組20 例患者中有男13 例,女7 例;其年齡為51 ~75歲,平均年齡(64.24±6.17)歲;用FAB 分類法對其病情進行分型的結果顯示:有3 例M1 型患者,有2 例M2 型患者,有1 例M4 型患者,有9 例M5 型患者,有5 例M6 型患者。兩組患者的一般資料相比,P>0.05,存在可比性。
1.2 方法
采用由注射用阿糖胞苷〔生產企業:輝瑞制藥(無錫)有限公司,批準文號:國藥準字H20205028,規格:0.5 g/支〕、注射用鹽酸阿克拉霉素(生產企業:揚州奧賽康藥業有限公司,批準文號:國藥準字H20060196,規格:20 mg/ 支)和重組人粒細胞集落刺激因子注射液(生產企業:Kirin Brewery Company Limited,批準文號:國藥準字S20030071,規格:75 μg :0.3 mL/ 支)三種藥物組成的CAG 方案對對照組患者進行治療。注射用阿糖胞苷的用法:進行皮下注射,每次注射10 mg/m2,每12 h 用藥1 次。注射用鹽酸阿克拉霉素的用法:進行靜脈滴注,每次滴注20 mg,每日用藥1 次,在每個化療周期的第1 d、第3 d、第5 d、第7 d 使用。重組人粒細胞集落刺激因子注射液的用法:進行皮下注射,每次注射300 μg,每日用藥1 次。采用CAG 方案(用法與對照組患者相同)聯合注射用地西他濱(生產企業:山東新時代藥業有限公司,批準文號:國藥準字H20173052,規格:25 mg/ 支)對治療組患者進行治療。注射用地西他濱的用法:進行靜脈滴注,每次滴注20 mg/m2,每日用藥1 次,在每個化療周期的第1 至第5 d 使用。兩組患者均以14 d 為一個化療周期,連續治療2 個周期。
1.3 觀察指標
治療結束后,觀察對比兩組患者血生化指標的變化情況。血生化指標包括全血中性粒細胞計數(neutrophil,NEUT)、血紅蛋白(hemoglobin,Hb)的含量及血小板計數(blood platelets count,BPC)。治療前后,分別采集兩組患者5 mL 的靜脈血(在清晨空腹的狀態下采集),用血常規檢測儀檢測其全血NEUT、Hb 的含量及BPC。記錄兩組患者免疫功能相關指標的變化情況。治療前后,分別采集兩組患者5 mL 的靜脈血(在清晨空腹的狀態下采集),按照2500 r/min 的轉速對其血液標本進行15 min 的離心處理后,取得血清標本。使用免疫速率比濁法檢測兩組患者血清免疫球蛋白(immunoglobulin,Ig)M、IgA、IgG 的水平。統計治療期間兩組患者不良反應(包括肝功能損害、發熱、血小板減少、惡心嘔吐及肺部感染等)的發生情況。
1.4 統計學方法
應用SPSS 20.0 統計軟件對本次研究中的數據進行分析,計量資料用均數± 標準差(±s)表示,采用t檢驗,計數資料用百分比(%)表示,采用χ2檢驗,P<0.05為差異具有統計學意義
2 結果
2.1 治療前后兩組患者血生化指標的對比
治療前,兩組患者的全血NEUT、Hb 含量及BPC 相比,P>0.05。治療后,兩組患者的全血NEUT、Hb 含量及BPC 均低于治療前,P<0.05。治療后,兩組患者的全血NEUT、Hb 含量及BPC 相比,P>0.05。詳見表1。
表1 治療前后兩組患者血生化指標的對比(± s)
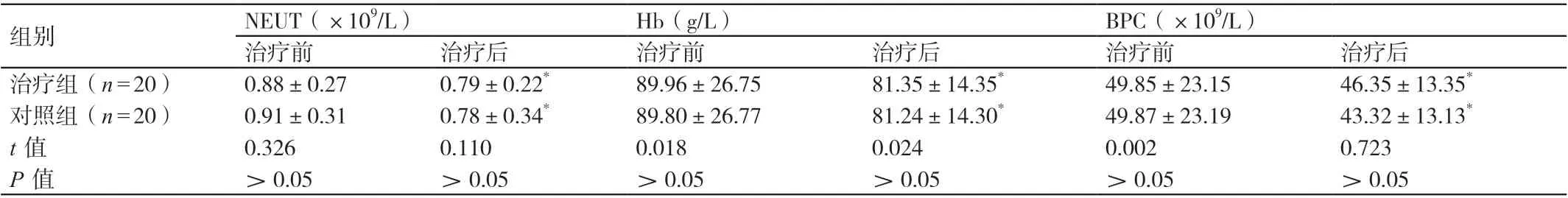
表1 治療前后兩組患者血生化指標的對比(± s)
注:* 與治療前相比,P <0.05。
組別 NEUT(×109/L) Hb(g/L) BPC(×109/L)治療前 治療后 治療前 治療后 治療前 治療后治療組(n=20) 0.88±0.27 0.79±0.22* 89.96±26.75 81.35±14.35* 49.85±23.15 46.35±13.35*對照組(n=20) 0.91±0.31 0.78±0.34* 89.80±26.77 81.24±14.30* 49.87±23.19 43.32±13.13*t 值 0.326 0.110 0.018 0.024 0.002 0.723 P 值 >0.05 >0.05 >0.05 >0.05 >0.05 >0.05
2.2 治療前后兩組患者免疫功能指標的對比
治療前,兩組患者血清IgM、IgA、IgG 的水平相比,P>0.05。治療后,兩組患者血清IgM、IgA、IgG 的水平均低于治療前,P<0.05。治療后,兩組患者血清IgM、IgA、IgG 的水平相比,P>0.05。詳見表2。
表2 治療前后兩組患者免疫功能指標的對比(g/L,± s)
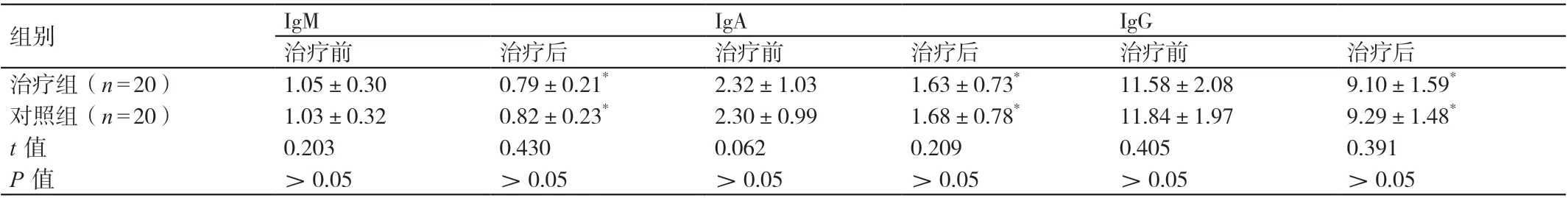
表2 治療前后兩組患者免疫功能指標的對比(g/L,± s)
注:* 與治療前相比,P <0.05。
組別 IgM IgA IgG治療前 治療后 治療前 治療后 治療前 治療后治療組(n=20) 1.05±0.30 0.79±0.21* 2.32±1.03 1.63±0.73* 11.58±2.08 9.10±1.59*對照組(n=20) 1.03±0.32 0.82±0.23* 2.30±0.99 1.68±0.78* 11.84±1.97 9.29±1.48*t 值 0.203 0.430 0.062 0.209 0.405 0.391 P 值 >0.05 >0.05 >0.05 >0.05 >0.05 >0.05
2.3 治療期間兩組患者不良反應發生情況的對比
治療期間,與對照組患者相比,治療組患者中發生惡心嘔吐、發熱患者的占比較高,發生血小板減少患者的占比較低,P<0.05。兩組患者中發生肝功能損害、肺部感染患者的占比相比,P>0.05。詳見表3。

表3 治療期間兩組患者不良反應發生情況的對比[例(%)]
3 討論
AML 患者的預后極差,其病情易復發或進展為難治性AML,若治療失敗可導致其死亡[5]。CAG 方案中的藥物均可作為白血病細胞的誘導分化劑,促進白血病細胞的分化和凋亡。但由于患者對化療藥物的耐受性不同,治療后其骨髓造血功能恢復的速度也存在差異,故其實際療效與臨床預期療效存在一定的差異[6]。而且,CAG 方案中的藥物均存在一定的細胞毒性。患者在應用這類藥物時易出現免疫功能下降的現象,并可出現發熱、惡心嘔吐及血小板減少等不良反應。地西他濱屬于胞嘧啶類似物。該藥可激活機體中沉默失活的抑癌基因,有效地抑制癌細胞的擴散和轉移[7]。該藥還可作為一種特殊的催化劑,提高阿糖胞苷對白血病細胞的敏感性,并可與重組人粒細胞集落刺激因子及阿糖胞苷發揮協同的作用[8]。
本次研究的結果證實,用地西他濱聯合CAG 方案對復發難治性AML 患者進行治療可影響其免疫功能及血生化指標,治療期間其發熱、惡心嘔吐等不良反應的發生率也較高,但其血小板減少的發生率較低。

