全腹腔鏡下遠端胃切除術聯合三角吻合術治療胃癌的臨床研究
張一帆
胃癌是胃腸道常見的惡性腫瘤,死亡率較高,嚴重威脅患者生命安全。目前手術是治療該疾病的首選方式,且隨著腹腔鏡技術的發展,全腹腔鏡下遠端胃切除術(TLDG)成為治療胃癌的主要方式,該手術可保留部分正常胃組織,可維持術后患者基本胃功能[1-2]。但遠端胃切除術還需Brillroth Ⅱ式吻合術式配合,進行消化道重建,方可完成手術,保證手術效果。目前該術式分為三角吻合(DA)與管狀吻合(TA)[3]。其中TA于術中作輔助性小切口完成吻合術操作。而DA則是腹腔鏡下完成吻合術操作,可有效降低手術創傷,更利于患者術后恢復[4]。基于此,本研究旨在探討TLDG聯合DA治療胃癌的臨床效果。現報告如下。
1 資料與方法
1.1 一般資料
本研究通過醫學倫理委員會審核同意,選擇我院2018年2月至2020年4月收治的75例胃癌患者,采用隨機數表法將其分為對照組(n=38)和觀察組(n=37)。對照組男性22例,女性16例;年齡47~74歲,平均(58.32±4.25)歲;腫瘤直徑2~8 cm,平均(5.16±1.04)cm。觀察組男性23例,女性14例;年齡45~76歲,平均(57.62±4.38)歲;腫瘤直徑2~9 cm,平均(5.52±1.14)cm。兩組一般資料比較(P>0.05),有可對比性。
1.2 入選標準
(1)納入標準:①經手術病理確診為胃癌;②腫瘤分期Ⅰ~Ⅲ期;③患者或其家屬簽署知情同意書。(2)排除標準:①存在手術禁忌癥;②伴有其他惡性病變;③合并全身感染、凝血功能障礙;④合并重要器官、系統功能障礙。
1.3 方法
1.3.1 觀察組 給予TLDG+DA術式:患者于手術臺上取平臥位,全身麻醉后行氣管插管。選取臍下做一切口,建立CO2腹氣;建立腹氣后置入腹腔鏡,探查腹腔情況。腹腔鏡引導下,選取平臍上腹直肌外緣、左側腋前線、雙側腋前線與劍突連線中點水平交點處做穿刺孔。并置入5 mm穿刺器。向近心端翻起大網膜。沿橫結腸邊緣至升結腸處游離大網膜,并游離橫結腸前葉直至胰腺下緣,之后沿胰腺下緣依次向上游離至上緣處。向左端切斷大網膜,并切斷胃短血管、韌帶,清掃胃大彎淋巴結。之后游離胃網膜,取不可吸收夾,夾閉并切斷胃網膜右血管及十二指腸動脈分支,之后清掃右血管處淋巴結。游離胰腺上端血管鞘,至肝總動脈、胃左動脈、冠狀靜脈暴露,切管,之后切斷胃左動脈及冠狀靜脈,清掃各部位淋巴結。選取十二指腸球部至腫瘤近端4 cm胃體游離,將臍部切口擴大后取出標本,病理檢測二級果呈陰性后,退出胃管,行消化道重建。切斷十二指腸球部,沿胃大彎至小彎游離胃組織,分別于十二指腸后壁殘端與殘胃大彎處作操作孔,之后將殘胃與十二指腸后壁吻合,于另一側將胃后壁拉伸至十二指腸殘端,常規止血后,生理鹽水沖洗腹腔,縫合、置胃管、引流管,術畢。
1.3.2 對照組 給予LADG+TA術式。術前操作同上觀察組,待淋巴結及胃組織清掃完畢后,選取上腹做切口,取出標本后,采用吻合器經切口進行胃十二指腸吻合術,常規止血縫合及后操作同上觀察組。
1.4 評價指標
①手術相關指標。記錄兩組手術、腸蠕動恢復以及住院的時間,術中出血量以及淋巴結清掃數目。②免疫功能。分別于術前、術后4 d抽取兩組患者3 ml外周靜脈血,離心取血清后置于-20 ℃冷藏柜待檢,儀器選用美國雅培公司提供的i2000SR型全自動微粒子化學發光免疫分析儀,使用免疫比濁法檢測血清免疫球蛋白M(IgM)、免疫球蛋白A(IgA)、免疫球蛋白G(IgG)水平,試劑盒均自購于美國雅培公司,檢測需按照說明嚴格操作,且全程需遵守無菌操作原則。③并發癥。統計術后并發癥發生情況。
1.5 統計學方法
應用SPSS 23.0軟件進行數據處理,以表示計量資料,組間用獨立樣本t檢驗,組內用配對樣本t檢驗,計數資料用百分比表示,采用χ2檢驗,P<0.05為差異具有統計學意義。
2 結果
2.1 手術相關指標
兩組淋巴結清掃數目相比,差異無統計學意義(P>0.05);與對照組相比,觀察組手術用時長,術中出血量少,腸蠕動恢復時間、住院時間短,差異有統計學意義(P<0.05),見表1。
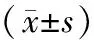
表1 兩組手術相關指標對比
2.2 免疫功能
術后4 d兩組IgA、IgG、IgM水平均比術前低,但觀察組降低幅度小,差異有統計學意義(P<0.05)。見表2。

表2 兩組免疫功能對比
2.3 并發癥
觀察組并發癥發生率(8.11%)略低于對照組(21.05%),差異無統計學意義(P>0.05)。見表3。

表3 兩組并發癥對比(例,%)
3 討論
腹腔鏡技術隨著科技發展速度而越發成熟,已被臨床廣泛應用于胃癌治療中,但該術對胃病灶進行切除后,仍需進行消化道重建術,還需要另作一輔助切口,以保證十二指腸和殘胃吻合[5]。但該輔助性切口可增大手術創傷,不利于患者術后恢復[6]。因此還應尋找可降低手術損傷的最佳術式,以保證預后。
本研究結果顯示,觀察組手術用時較對照組長,可能是因TLDG+DA對術者技術要求較高有關,且作為1種新型術式,術者對術中操作技術不熟練,從而增加手術時間。同時兩組淋巴結清掃數目無差異,分析原因在于,兩種術式除后期吻合不同外,前半部分的游離組織、夾閉血管以及清掃淋巴結的操作基本相同,因此兩組患者的淋巴結清掃個數差異無統計學意義[7]。但觀察組術中出血量較低,提示在進行消化道重建術操作時,TLDG+DA術式可明顯擴大手術的視野和操作空間,有效減少腹腔鏡相關器械對患者腸管的刺激程度,從而降低出血量[8-9]。同時觀察組術后腸蠕動恢復以及住院的時間均短于對照組,說明TLDG+DA術可減輕手術給機體帶來的損傷程度,進而利于術后機體康復[10-11]。觀察組IgA、IgG、IgM水平高于對照組,分析其原因在于,TLDG術具有一定損傷性,可誘發術中患者出現不同程度的應激和炎癥反應,抑制機體免疫功能,但TLDG+DA術全程與腹腔鏡的引導下操作,可避免手術過程中手術器械之間的相互轉換造成的機體損傷,減輕手術器械及術中操作對患者機體造成的刺激和損傷,進而減輕術中應激以及炎癥反應,保護機體免疫功能[12-13]。本研究愛最后還對兩種術式的安全性進行比較,結果可得觀察組安全性更高,究其原因在于,DA術中的吻合操作是利用指定6 cm的切割吻合器進行,可有效保證胃殘組織和十二指腸的吻合口處存在較的內腔空間,可盡可能避免出現狹窄[14];同時DA術的吻合方向也具有一定優勢,其方向和血管走向一致,說明該處的血液供應較為充足,因此其發生口瘺和、出血的風險較低[15];同時該術式無需于吻合術時作輔助切口,創傷面積較少,因此切口感染率也隨之降低。
綜上所述,胃癌患者采用TLDG聯合DA術治療減輕手術創傷,加快術后恢復,對免疫功能影響小,且可降低術后并發癥發生率。

