高效液相色譜-串聯質譜法測定人血漿中異煙肼、利福平及其在健康男性體內的藥物代謝動力學研究*
張美微,陸優麗,忻亮,李水軍,劉罡一,董春霞,張夢琪,梁立宇,繆怡,賈晶瑩(上海市徐匯區中心醫院&中國科學院上海臨床研究中心.中心實驗室,.輸血科,上海 200031)
異煙肼(isoniazid,INH)和利福平(rifampicin,RFP)是目前預防和治療結核病(tuberculosis,TB)的一線藥物,臨床上常將二者聯合應用以提高療效,延緩結核桿菌(mycobacterium tuberculosis,MTB)的抗藥性。
INH在體內經N-乙酰基轉移酶2(N-acetyltransferase,NAT2)和酰胺水解酶(amide hydrolase,AH)催化直接或間接生成乙酰異煙肼和肼,兩者均具有肝毒性[1]。慢性肝病或嚴重腎功能不全的患者使用INH后可發生嚴重甚至是致死性的藥物性肝炎。RFP 可誘導肝藥酶活性,加速乙酰異煙肼代謝為乙酰肼,INH與RFP 聯合應用時肝毒性明顯增強[2],已有治療后發生卟啉癥惡化的個案報道。有證據表明,NAT2的基因型決定RFP 的代謝基本分為快代謝[(半衰期t1/2)為1~2 h]和慢代謝(t1/2為2~5 h)兩種,其中RFP 慢代謝型的危險性是快代謝型的28 倍[3-6],并且基因型與表型結果基本一致。因此準確測定血藥濃度并結合代謝類型,合理地制定個性化用藥方案尤為重要。
本研究旨在建立簡便、可靠的高效液相色譜-串聯質譜(high performance liquid chromatography tandem mass spectrometry,HPLC-MS/MS)分析方法,檢測人血漿中INH和RFP 的濃度,研究中國健康男性體內藥物代謝動力學特征,為臨床進行治療藥物監測提供可靠的檢測手段和臨床數據。
1 材料與方法
1.1 主要儀器與試劑 API4000串聯質譜儀(美國應用生物系統公司);液相系統(日本島津公司)包括SIL-HTc 自動進樣器,LC-20AD 輸液泵,DGU-20A3在線脫氣儀,CBM-20A控制器;EHMA切換閥(美國Valco Instrument 公司);Milli-Q 超純水系統(美國Millipore公司)。
RFP、INH 標準品(歐洲藥典);利福平-氘3(RFP-d3)、異煙肼-氘4(INH-d4)購自加拿大TRC公司;甲酸、甲醇、甲酸胺(HPLC 級)購自德國CNW公司;乙腈(HPLC 級)購自美國DIKMA 公司;抗壞血酸(VC)(分析純)購自中國國藥集團;水為Millipore Advantage A10 制超純水;空白人肝素鈉抗凝血漿來源于健康志愿者。
1.2 RFP 和INH的色譜條件 見表1。
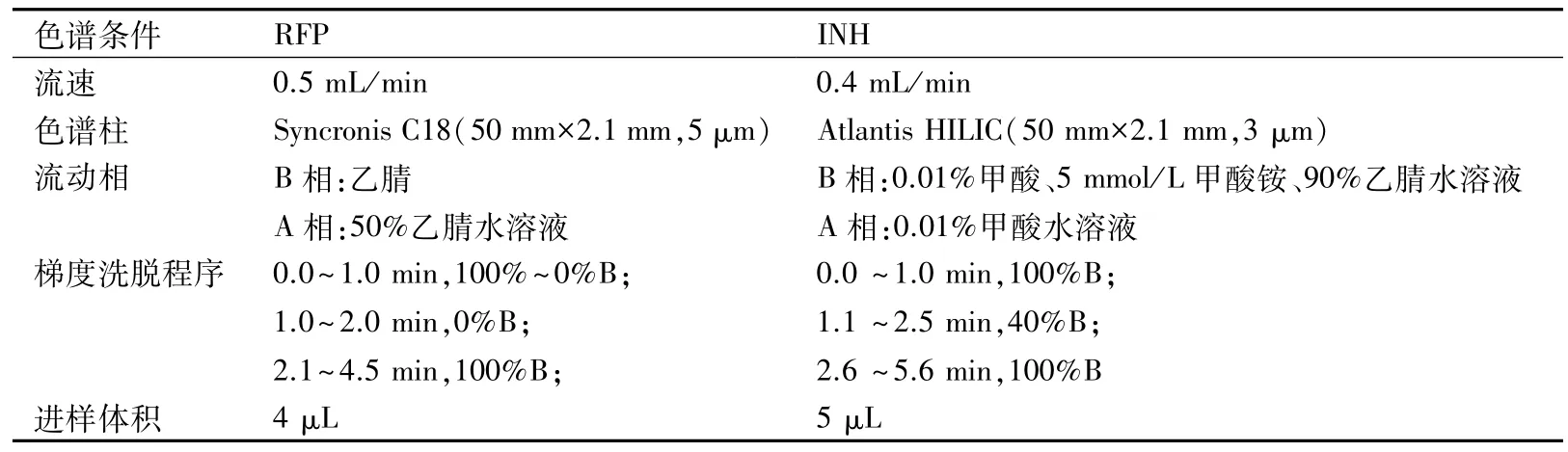
表1 RFP 和INH的色譜條件
1.3 INH和RFP 的質譜條件 采用電噴霧離子源正離子模式(ESI+)下多反應監測模式(MRM)進行質譜分析,質譜源參數:霧化氣(GAS1)為60 psi(1 psi=6.895 kPa),輔助加熱氣(GAS2)為60 psi,氣簾氣(CUR)為30 psi,離子源加熱溫度(TEM)分別為550 ℃(INH)和500 ℃(RFP);離子噴霧電壓(IS)分別為1 500 V(INH)和5 500 V(RFP);分析參數見表2。

表2 INH和RFP 的分析參數
1.4 溶液的制備 精密稱取適量RFP 和INH,用甲醇制備成446 μg/mL(INH)、864 μg/mL(RFP)的標準儲備液。取INH/RFP 儲備液,加入適當體積含9.5 mmol/L VC的50%乙腈水溶液(稀釋液),制成含INH/RFP 濃度為0.05/0.1、0.1/0.2、1/2、5/10、20/40、45/90、50/100 μg/mL 的標準添加液,0.05/0.1(定量下限)、0.15/0.3(低)、10/20(中)、40/80(高)、200/400(稀釋)μg/mL的質控添加液,添加液臨用時新鮮配制。精密稱取適量INH-d4和RFP-d3,用甲醇制備成98 μg/mL(INH-d4和RFP-d3)的內標儲備液,所有儲備液置于-90~-70 ℃保存。臨用時取稀釋液稀釋至所需濃度作為工作液備用。
1.5 血漿樣品預處理 樣品制備均在冰上操作且避免太陽光照射。取血漿100 μL,加入10 μL內標工作液和300 μL甲醇,混旋10 s,7 715×g(4 ℃)離心3 min。吸取上清液25 μL,加入100 μL 30%乙腈水溶液,混勻后用于RFP 的進樣分析;另取上清液25 μL,加入100 μL 80%乙腈水溶液,混勻后用于INH的進樣分析。
1.6 數據處理 用Analyst Software(1.6.1)軟件進行質譜數據采集及定量計算,用SAS軟件對血藥濃度-時間數據以非房室模型方法對其藥動學參數進行統計計算及分析。
2 實驗與結果
2.1 方法學評價
2.1.1 選擇性 分別取人空白血漿、加入標準添加液和內標工作液的血漿樣品和服用試驗藥物研究對象的血漿樣品,按“1.5”項下方法處理后進樣分析,得到色譜圖,見圖1、2,各樣品分離度良好,內源性物質對測定無干擾。
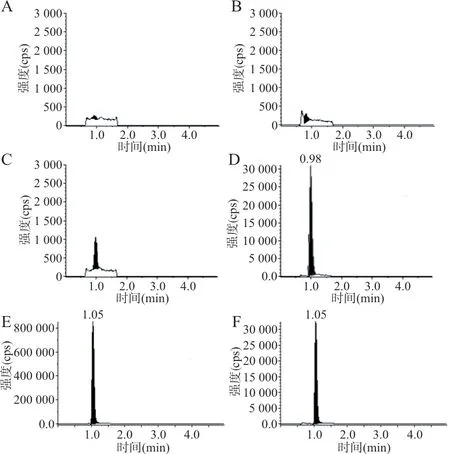
圖1 INH及INH-d4 典型色譜
2.1.2 標準曲線和定量下限 取空白血漿90 μL,加入10 μL INH/RFP 標準添加液,漩渦混勻,配制成含INH/RFP濃度為5/10、10/20、100/200、500/1000、2 000/4 000、4 500/9 000、5 000/10 000 ng/mL的標準曲線樣品,按“1.5”項下操作,以理論濃度為X軸,分析物和內標峰面積的比值為Y軸,按權重因子1/X,用最小二乘法進行線性回歸分析。INH在5~5 000 ng/mL范圍內,RFP 在10~10 000 ng/mL 范圍內,線性關系良好,相關系數均>0.99。
2.1.3 精密度 取空白血漿90 μL,加入10 μL INH/RFP 質控添加液,漩渦混勻,制得5、15、1 000、4 000、20 000 ng/mL質控樣品,每個濃度平行配制6份,按“1.5”項下操作,連續3 個批次,考察精密度,見表3。

圖2 RFP 及RFP-d3 典型色譜
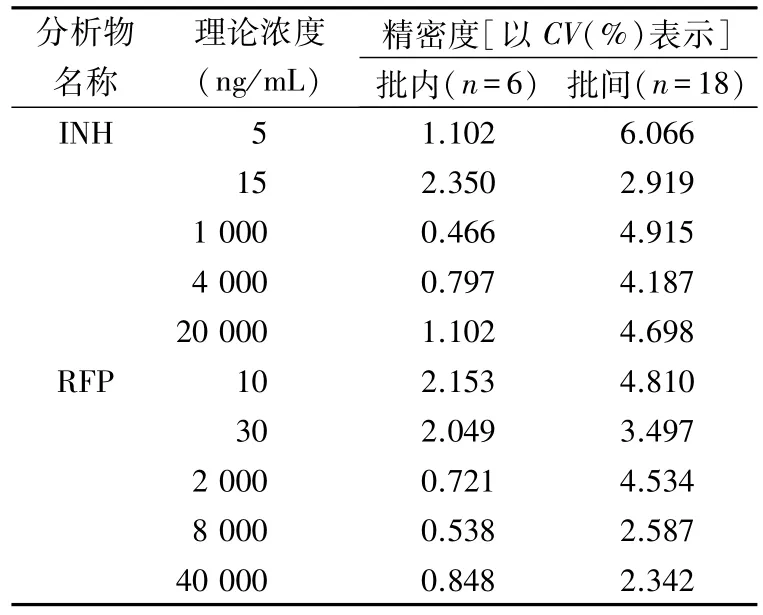
表3 HPLC-MS/MS法測定INH及RFP 濃度的精密度
2.1.4 提取回收率 制備低、中、高濃度質控樣品,按“1.5”項下操作,得峰面積EPA;另取空白血漿,經過同樣的預處理后,加入對應濃度的質控添加液和內標工作液進行分析,得峰面積UPA。以上樣品重復測定6 次,計算提取回收率,公式為R(%)=EPA/UPA平均值×100%,結果見表4。
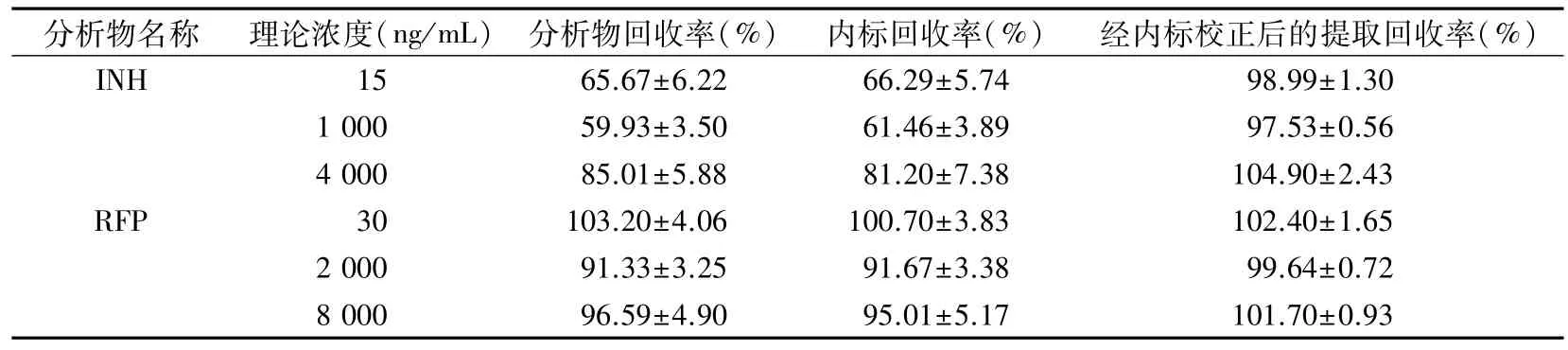
表4 HPLC-MS/MS法測定INH和RFP 的提取回收率
2.1.5 基質效應 取6個不同來源的空白血漿各6份,不加內標,按“1.5”項下操作,吸取上清液,加入低、高濃度質控添加液和內標工作液,進樣分析得峰面積A;對應濃度化學品溶液進樣分析得峰面積AC;以A/AC平均值的比值計算基質因子(MF),以MF(分析物)/MF(內標)的比值計算內標校正基質因子。結果表明,經內標校正后,INH 在0.899~1.294范圍內,RFP 在0.970~1.049范圍內,無明顯基質效應。
2.1.6 穩定性 制備(INH 為15 ng/mL,RFP 為30 ng/mL)、高(INH為4 000 ng/mL,RFP 為8 000 ng/mL)濃度的血漿質控樣品,考察短期(室溫/2~8 ℃)放置、多次凍融及長期凍存(-90~-70 ℃)的穩定 性。制 備 低(INH 為15 ng/mL,RFP 為30 ng/mL)、高(INH為4 000 ng/mL,RFP 為8 000 ng/mL)濃度的全血質控樣品,考察室溫放置的穩定性。結果表明,INH和RFP 的血漿樣品室溫(15~25 ℃)放置2 h、冷藏(2~8 ℃)放置24 h,反復凍融3次,冷凍(-90~-70 ℃)保存28 d均穩定;全血樣品室溫放置1 h較穩定。結果見表5。

表5 INH和RFP 在血漿及全血中的穩定性
將同一來源的儲備液和工作液分裝,考察分析物儲備液室溫及長期凍存(-90~-70 ℃)和工作液室溫放置的穩定性;內標工作液2~8 ℃和室溫放置的穩定性。INH和RFP 儲備液和工作液室溫至少可存放4 h,儲備液-90~-70 ℃下至少可保存31 d,內標工作液室溫至少可存放4 h,2~8 ℃至少可保存24 h,結果均較穩定。
2.2 臨床研究 選擇年齡為18~55 周歲(含18、55周歲)的24 例中國健康男性(符合方案的入選標準)作為研究對象,進行單次口服Rifinah?(INH片150 mg/RFP300 mg)藥動學研究。本研究經上海市徐匯區中心醫院倫理委員會批準(文號:2014-28),所有研究對象均簽署知情同意書。研究對象給藥開始前10 h內以及服藥后4 h內禁止飲食,分別于給藥前(0 h)和給藥后第15 min、30 min、45 min、1 h、1.5 h、2 h、2.5 h、3 h、3.5 h、4 h、5 h、6 h、8 h、10 h、12 h、14 h、24 h采集3 mL靜脈血,肝素鈉抗凝,并在2~8 ℃下,于采樣完成30 min內離心(1 500×g離心5 min)獲得血漿,血漿樣品保存于-90~-70 ℃冰箱中待測。
各時間點INH和RFP 平均濃度與時間的曲線見圖3,主要的藥代動力學參數見表6,本研究中RIF的各項藥代動力學參數個體間變異較小,而INH藥代動力學特征存在明顯個體差異,24例健康志愿者中11 例T1/2≥2 h 為慢乙酰化(45.8%),13例T1/2<2 h為快乙酰化(54.2%),峰濃度(Cmax)、個體間變異均較大(CV>30%)。本研究中NAT2酶快慢代謝能力、比率及INH半衰期與文獻報道基本一致,與說明書中描述的大多數亞洲人屬INH快代謝型相符。
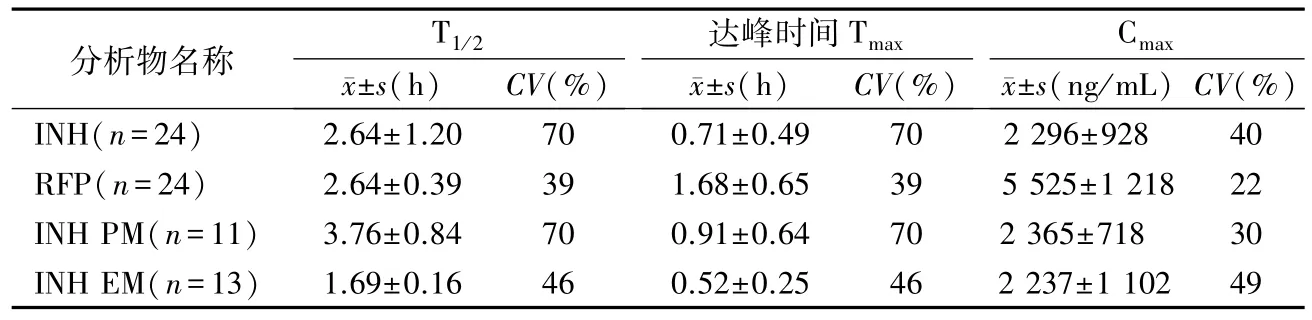
表6 研究對象單次口服150 mg INH和300 mg RFP 后的主要藥代動力學參數

圖3 研究對象口服150 mg INH 和300 mg RFP 后INH和RFP 的平均劑量-時間曲線(n=24)
3 討論
研究表明,RFP 易被氧化且對光略敏感,需加抗氧化劑增加穩定性,另外INH 和RFP 的混合物對熱不穩定,因此方法條件的探索時考察了抗壞血酸VC(含量分別為0、2.5、5.0、9.5 mmol/L)、光照(日光燈下2、6、24 h)、溫度(冷藏/2~8 ℃,室溫/15~25 ℃)對血漿樣本中分析物穩定性的影響。結果顯示,在血漿中加入VC 9.5 mmol/L 可顯著增加分析物的穩定性;光照對RFP 的影響不顯著,因此可在日光燈下進行樣品的采集和處理;分析物在2~8 ℃下保存穩定性時間延長,因此血漿樣品前處理在冰上操作。
從化合物結構判斷(見圖4),INH 屬于極性較大的化合物,在親水色譜柱上保留較好,因此選用Atlantis HILIC 作為分析柱,克服了INH 保留時間短的問題且提高了靈敏度。而RFP 極性中等偏弱,在反相色譜柱上有較好的色譜行為,所以選用Syncronis C18作為分析柱。
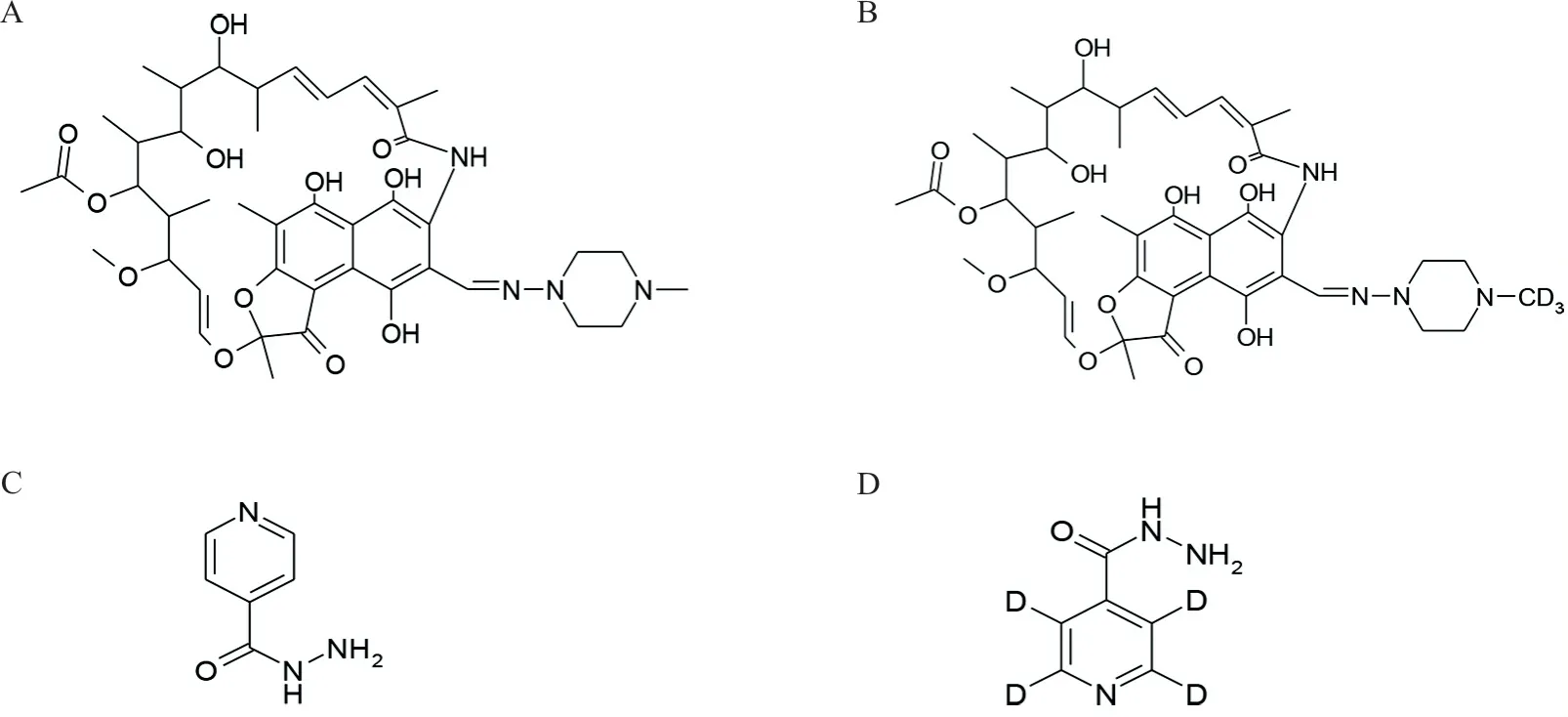
圖4 化合物RFP、RFP-d3、INH及INH-d4 的化學結構
本研究通過向血漿樣品中加入抗氧化劑來增加穩定性且樣本預處理方法簡便(蛋白質沉淀法),INH和RFP 的最低定量檢測限分別為5 ng/mL 和10 ng/mL(已報道的國內外文獻尚無低于本值者)。目前,國內外已有多篇文獻報道單獨或者同時檢測INH 和 RFP 血藥濃度的高效液相色譜法(HPLC-UV),但是這些方法有很多局限性,如樣品預處理采用固相萃取(SPE)及衍生化方法樣品制備步驟繁瑣,樣品使用體積較大,檢測靈敏度低,分析時間長等問題[7-9];大多數HPLC 分析方法使用C18色譜柱檢測INH,使其色譜保留有限,容易受內源性物質的干擾。
本研究中入組的男性體內INH 的藥動學特征符合文獻報道[10]的大多數亞洲人的代謝特征,INH代謝個體間差異顯著主要與NAT2基因型有關,如若不能根據患者代謝類型制定個體化給藥方案,直接影響到藥物的療效。臨床應用時可通過監測患者血藥濃度結合NAT2 代謝表型來判斷給藥劑量是否合理,后續可收集數據開發能指導臨床給藥的PK-PD模型,這對于患者(尤其是老年人,兒童等特殊群體患者)降低不良反應的發生率和程度,保證給藥劑量,提高療效、減少耐藥性,以及減輕患者經濟負擔具有重大意義。

