帕博利珠單抗聯合阿帕替尼致肝癌患者腎病綜合征1例伴文獻復習
劉 梓,胡志娟
0 引言
PD-1抑制劑是免疫哨點單抗藥物,腫瘤微環境中PD-1通路持續激活,T細胞功能被抑制,無法殺傷腫瘤細胞。PD-1抑制劑可以阻斷這一通路,激活T細胞的攻擊和殺傷功能,通過激活自身的免疫系統來抗癌[1-4]。VEGF拮抗劑阿帕替尼通過高度選擇性競爭細胞內VEGFR-2的ATP結合位點,阻斷下游信號轉導,從而抑制腫瘤組織新血管生成[5-6]。本文報道1例老年男性患者在使用PD-1抑制劑帕博麗珠單抗和VEGF拮抗劑阿帕替尼化療過程中出現的腎病綜合征,以期為臨床安全用藥提供參考。
1 病例資料
72歲男性患者,主因肝癌術后6個月,化療8周,蛋白尿3周于2019年12月26日入院。患者6個月前因原發性肝癌行手術治療,8周前應用PD-1抑制劑帕博利珠單抗2 mg/kg靜脈滴注,3周1個療程,共用3次,5周前加用VEGF拮抗劑阿帕替尼250 mg/d。3周前患者出現泡沫尿,查生化:總蛋白74.4 g/L,白蛋白41.2 g/L,肌酐87.0 μmol/L(53~132 μmol/L),腎小球濾過率76.33 ml/min;尿常規:潛血1+,蛋白質2+,紅細胞5.92個/HPF。2周前患者出現雙下肢水腫及尿量減少,伴皮膚瘙癢。1周前因癥狀加重,停用帕博利珠單抗和阿帕替尼。既往乙肝病史30余年,未口服抗病毒藥;糖尿病病史12年,應用胰島素治療,血糖控制可;發現血壓升高1月余,口服硝苯地平緩釋片20 mg/d,血壓控制良好。否認冠心病、腦梗死等慢性病史,有輸血史;無傷寒、結核等傳染病史,無外傷史,無過敏史。
入院后輔助檢查:血常規:白細數計數4.26×109/L,中性粒細胞1.43×109/L,血紅蛋白127 g/L,血小板計數123×109/L;尿常規:潛血±,葡萄糖±,蛋白質4+;生化:總蛋白53.6 g/L,白蛋白26.5 g/L,空腹血糖7.49 mmol/L,尿素3.3 mmol/L,肌酐94.6μmol/L(57~111 μmol/L),腎小球濾過率68.99 ml/min,總膽固醇5.64 mmol/L,三酰甘油1.32 mmol/L;乙肝表面抗體及核心抗體陽性,余均陰性;乙肝DNA熒光定量低于最小檢出量;甲功未見明顯異常;HIV抗體及TP抗體陰性;抗核抗體:1∶100;胞漿型;免疫球蛋白A 4.73 g/L(1.0~4.2 g/L),余免疫球蛋白及補體未見明顯異常。血清免疫固定電泳、抗中性粒細胞胞漿抗體、抗腎小球基底膜抗體、抗-dsDNA抗體和抗核抗體譜均陰性。D-二聚體定量2.1 mg/L FEU;糖化血紅蛋白 7.1%;24 h尿蛋白定量4.09 g,24 h尿量3.3 L,尿蛋白1.24 g/L;尿蛋白電泳:小分子蛋白0.4%,白蛋白46.9%,大分子蛋白52.7%;腹部CT:肝癌術后改變;膽囊未見明確顯示,腹腔內積液。泌尿系超聲:左腎113.9 mm×50.8 mm,右腎110.4 mm×52.5 mm,雙腎結構及雙側輸尿管未見明顯異常。胸部CT:雙肺下葉斑片狀磨玻璃密度增高影。
診斷、治療及轉歸。經鑒別診斷后確診為:①腎病綜合征;②2型糖尿病;③高血壓病3級(很高危);④慢性乙型病毒性肝炎;⑤原發性肝癌術后。患者已停用帕博利珠單抗及阿帕替尼。給予培哚普利8 mg,qd,并給予降糖及對癥支持治療。2019年1月8日復查尿液分析:葡萄糖1+,蛋白質2+;24 h尿蛋白定量2.26 g,尿量1.6 L,尿蛋白1.41 g/L;生化:總蛋白55.4 g/L,白蛋白28.8 g/L,肌酐 74.8 μmol/L(57~111 μmol/L),腎小球濾過率 87.22 ml/min。2020年1月9日,患者病情好轉出院。2020年1月30日門診復查生化:總蛋白72.8 g/L,白蛋白40.0 g/L,肌酐 76.8 μmol/L(57~111μmol/L),腎小球濾過率 86.28 ml/min;尿液分析:潛血弱陽性,蛋白質陰性,24 h尿蛋白定量:0.28 g,尿量2.1 L,尿蛋白0.13 g/L。患者化療期間尿蛋白及白蛋白水平,見表1。
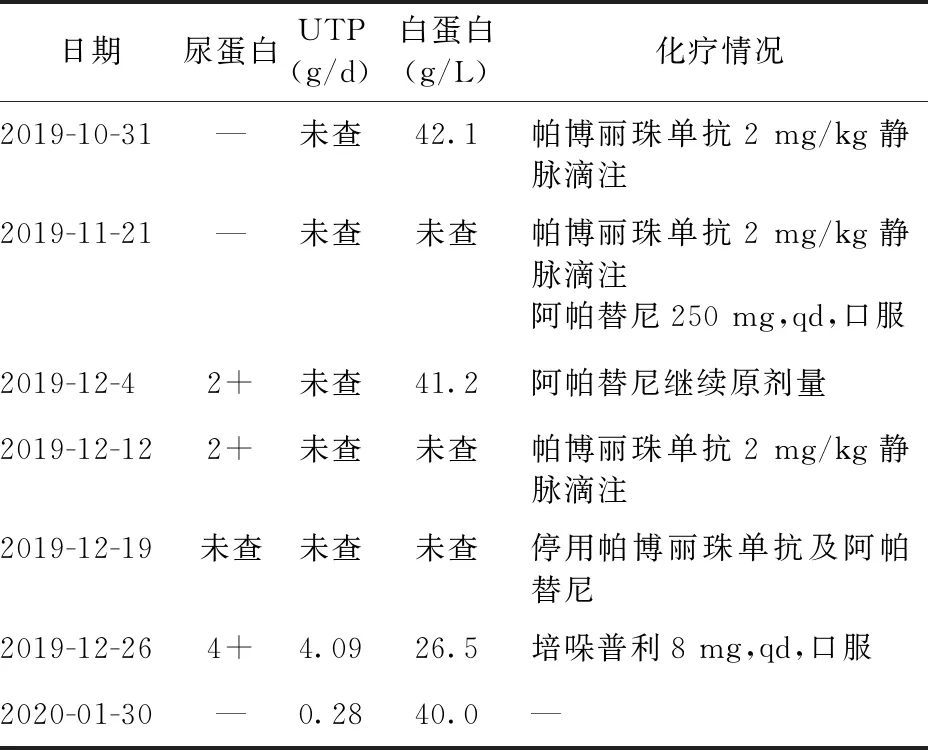
表1 患者化療期間蛋白尿及白蛋白的變化
2 討論
本文中的患者為老年男性,因原發性肝癌術后給予PD-1抑制劑帕博利珠單抗和VEGF拮抗劑阿帕替尼治療。應用帕博利珠單抗5周,阿帕替尼2周后出現蛋白尿。患者腎病綜合征的發生時間與帕博利珠單抗、阿帕替尼的應用存在明確的相關性。停用上述2種藥物6周后,患者完全緩解。
Roben等[7]觀察到PD-1抑制劑帕博利珠單抗的不良反應主要為乏力、皮疹、瘙癢癥、腹瀉、甲減和甲亢。在KeyNote-021研究[8]中發現的不良反應與Roben等[7]所觀察到的相似。這兩項研究均未發現使用PD-1抑制劑帕博利珠單抗發生蛋白尿的不良反應。本患者應用PD-1抑制劑帕博利珠單抗5周后出現蛋白尿,考慮該患者應用PD-1抑制劑帕博利珠單抗可能與蛋白尿關系不大。
VEGF拮抗劑阿帕替尼在臨床Ⅲ期治療胃癌的研究中,觀察到最常見的不良反應為蛋白尿、手足綜合征、高血壓,發生率分別為47.7%(其中3/4級占2.3%)、27.8%、35.2%[9]。在秦叔逵等[10]的研究中,VEGF拮抗劑阿帕替尼的不良反應與上述研究結果相似,蛋白尿的發生率為41.3%~45.7%,其中3/4 級蛋白尿發生率為1.4%~3.9%。蛋白尿的發生時間,Wang等[11]曾報道了1例肝內膽管癌患者應用阿帕替尼500 mg,qd,口服,5 d后出現顏面水腫,10 d后出現全身水腫的病例。Chen等[12]曾報道了1例直腸腺癌肺轉移患者應用阿帕替尼500 mg,qd,口服(后因高血壓調整為425 mg,qd),4個月后因出現蛋白尿而停藥的病例。但大多發生在服藥后 2 ~3 周,大多數不良反應是一過性或可逆的,且在可控制的范圍內[13]。結合文獻,蛋白尿是VEGF拮抗劑阿帕替尼的常見不良反應,但該藥物導致腎病綜合征的報道國內外少見。楊香瑜等[14]報道了1例69歲子宮內膜癌女性患者加用阿帕替尼250 mg,qd,3周后出現蛋白尿并進展為腎病綜合征的病例。馮春景等[15]報道了1例64歲乳腺癌女性患者加用阿帕替尼250 mg,qd,口服,3周后出現蛋白尿并進展為腎病綜合征的病例。袁曉剛等[16]報道了1例72歲肺鱗癌男性患者口服阿帕替尼250 mg,qd,約6周后進展為腎病綜合征的病例(蛋白尿出現時間不詳)。本例患者應用阿帕替尼2周后出現蛋白尿,約5周后蛋白尿加重并進一步發展為腎病綜合征,停藥6周后完全緩解,考慮患者腎病綜合征與VEGF拮抗劑阿帕替尼有關。
VEGF拮抗劑阿帕替尼引起蛋白尿,一方面可能是阿帕替尼增加了腎小球濾過膜通透性。腎小管內皮細胞有多種VEGF 受體表達,足細胞和腎小管內皮細胞之間的跨膜信號傳導維持腎小球結構和功能的完整性,阿帕替尼導致腎小球內皮細胞功能障礙及濾過屏障破壞[17-18],從而引起蛋白尿。另一方面,可能是阿帕替尼抑制血管內皮生長,作用于血管平滑肌的NO釋放減少,從而導致腎臟血流動力學改變,導致高血壓和蛋白尿[19]。
多數腫瘤患者可從VEGF拮抗劑阿帕替尼治療中長期獲益,但忽視蛋白尿則可能會導致腎損傷。應用阿帕替尼期間如果發生>2級的蛋白尿,建議暫停用藥(不超過 2 周),直至癥狀緩解或消失,隨后繼續按原劑量服用。如果恢復用藥后仍然出現>2級的蛋白尿,建議下調1個劑量單元的阿帕替尼劑量。如果需要第3次調整劑量,則永久停藥。如果出現腎病綜合征或腎損傷時,應立即停藥并給予對癥支持治療。應用阿帕替尼最初2個月,應每 2周檢查1次尿液分析和/或24 h尿蛋白定量,之后每4周檢查 1次,發生蛋白尿要及時就醫。關于蛋白尿的分級及防治建議見表2。

表2 蛋白尿分級標準(NCI-CTC AE 4.0)和防治建議
VEGF拮抗劑誘發的蛋白尿目前尚無特殊的治療方案。多數患者通過下調劑量或者停藥后即可恢復。血管緊張素轉化酶抑制劑(Angiotensin converting enzyme inhibitors,ACEI) 可拮抗血管緊張素抑制NO釋放效應,改善腎小球微循環,可以通過降低腎小管內壓力等作用降低尿蛋白,還可通過降低血清中纖溶酶原激活物抑制劑-1(Plasminogen activator inhibitor-1,PAI-1)水平來減少動脈血栓的發生。有部分患者停藥后蛋白尿持續加重,甚至出現血栓性微血管病變,這類患者的預后以及是否給予激素或血液透析及血漿置換等治療目前尚有爭議。
綜上,PD-1抑制劑帕博利珠單抗與VEGF拮抗劑阿帕替尼是新型抗腫瘤藥物,仍需密切監測其不良反應。該病例提示臨床上即使以低劑量應用阿帕替尼時仍應密切監測肝腎功能及尿蛋白,警惕腎病綜合征以及腎損傷的發生。

