3D打印結合橋接固定系統進行有限元分析在治療粉碎性復雜髖臼骨折中的應用
黃佳軍, 藍孝全, 董德鵬, 黃智勇, 馬建林, 趙敦旭
(山東第一醫科大學附屬青島醫院, 1. 創傷顯微外科, 2. 3D打印醫學轉化中心, 山東 青島, 266000)
粉碎型復雜髖臼骨折多采取切開復位內固定治療,但術中需反復復位,存在手術創傷大、時間長、術后恢復慢等問題[1-2]。橋接系統是一套多元化支架復合體,能克服應力集中的問題,并用彈性固定代替剛性固定,生物力學性能良好[3]。研究[4]證實,橋接固定系統具有三維、彈性、橋接固定等特點,結合3D打印技術可在術前個性化預構橋接內固定系統,并通過有限元分析調整螺釘位置與深度,優化復位模型,強化手術效果。本研究選取112例粉碎型復雜髖臼骨折患者,創新性地將3D打印結合橋接固定系統用于患者的治療,并建立有限元模型,現將結果報告如下。
1 資料與方法
1.1 一般資料
本研究為前瞻性研究,采取隨機對照設計。選取2017年1月—2020年5月山東第一醫科大學附屬青島醫院收治的112例粉碎性復雜髖臼骨折患者,隨機分為觀察組和對照組,每組56例。納入標準: ① 年齡18~60歲者; ② 符合《實用骨科學》[5]中粉碎性復雜髖臼骨折診斷標準并經影像學檢查證實者; ③ 患者受傷時間10 d內; ④ 無骨折手術史者; ⑤ 受傷前雙側髖關節活動度正常者; ⑥ 符合手術指征、單側手術、精神狀態正常者; ⑦ 簽署知情同意書者。排除標準: ① 過度肥胖或營養不良者; ② 病理性骨折、合并血管神經損傷者; ③ 入組前使用大劑量激素類、免疫抑制劑類藥物者; ④ 伴骨質疏松、血友病、自身免疫性疾病、肝腎功能障礙、腫瘤者。
1.2 方法
1.2.1 設備與軟件: Windows 10(64位)操作系統,醫學三維重建軟件Mimics 20.0(Materialise公司), Dell M6600圖形工作站,光敏樹脂3D打印機(聯泰公司)及配套3D-ORTHO三維手術規劃系統,螺旋雙源CT(西門子)。
1.2.2 術前準備: 患者入院后行抗休克治療,處理開放傷及臟器損傷,病情穩定后行骨盆X線片、CT檢查,明確髖臼骨折分型[6]。
1.2.3 對照組: 采取傳統鋼板內固定,全身麻醉下手術,漂浮體位,常規消毒、鋪單。雙柱骨折采取髂腹股溝及K-L聯合入路,前柱骨折采取髂腹股溝入路,后壁骨折采取K-L入路。術中注意保護股動、靜脈,股神經及股外側皮神經,辨認髂恥束筋膜,將筋膜與內外側結構分開,游離筋膜至骨盆入口緣后切斷,進入四邊體表面和真骨盆腔。沿骨盆入口緣、四邊體表面及恥骨上支剝離,依次暴露3個窗口,顯露骨折部位。利用骨盆復位器械進行復位,采用術前預彎的內固定鋼板及合適長度的螺釘進行固定(鈦合金材料)。
1.2.4 觀察組: 采取3D打印結合橋接固定系統,術前進行個體化有限元分析并預構橋接固定系統。① 建立復位模型。采取雙源CT進行骨盆掃描,電流35~264 mAs, 電壓80~120 kV, 螺距0.6 mm, 數據以DICOM格式保存。通過三維編輯分離粉碎骨塊并指定顏色,虛擬復位并合成三維復位模型,保留骨折線,保存STL格式。② 3D打印。以STL格式導入3D打印軟件中打印等比例樹脂實物模型,光固化成型法成型。③ 橋接固定系統。結合打印的復位模型,微調、預彎處理內固定物,模擬內固定物密切貼合骨面并精準定位螺絲釘部位與擰入深度,構建復位模型。④ 有限元分析。掃描復位模型并導入Mimics 20.0軟件,將模型各部分建立對應元件,經quick edit處理后劃分體網格,有限元模型共生成789 543個結點、48 312個單元。模型材料屬性及韌帶強度見表1, 材料特性被認為是均勻和各向同性。
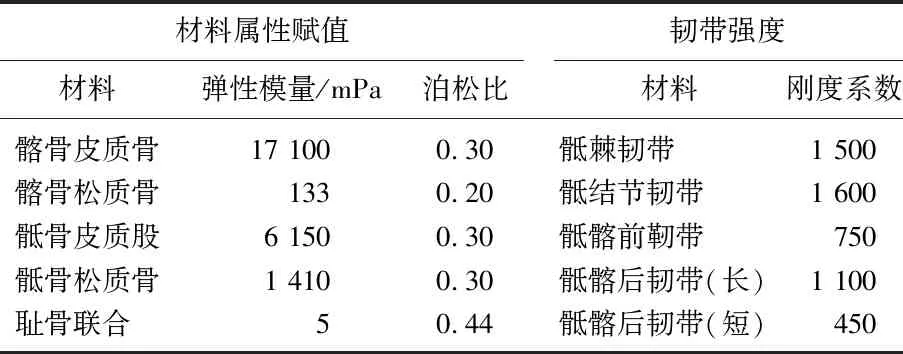
表1 材料屬性賦值與韌帶強度
模擬人體狀態對模型施加個性化邊界條件和載荷: ① 骨盆上端施加500 N力模擬直立。② 骨盆上端施加500 N力、在+X、-X方向施加7.5 Nm力矩模擬前屈、后伸。③ 骨盆上端施加500 N力、+Y方向施加7.5 Nm力矩模擬前屈側彎。④ 骨盆上端施加500 N力、+Z方向施加7.5 Nm力矩模擬旋轉狀態。坐標系基于股骨定義, X軸指向股骨內側, Y軸指向股骨前方, Z軸豎直向上。根據模擬狀態得到內固定物應力分布及位移,并調整螺絲釘部位與擰入深度,減小應力與位移,實現模型優化。觀察組在對照組基礎上采取有限切開復位,根據術前模擬的內固定方案將內固定物精準植入人體。
1.2.5 術后處理: C臂機透視滿意后采用生理鹽水沖洗,術后常規傷口內放置引流管48 h, 應用抗生素48 h。24 h后開始股四頭肌及屈髖、屈膝練習, 4周后扶雙拐下地, 8周部分負重, 12周后完全負重行走。
1.3 觀察指標
① 比較2組住院時間、骨折愈合時間。② 2組術后第3天行骨盆正位、髂骨及閉孔斜位X線檢查,復位標準參照Matta影像學標準[7]。骨折移位<1 mm判定為解剖復位,骨折移位1~3 mm判定為復位良好,骨折移位>3 mm判定為復位不佳。復位滿意率=(解剖復位+復位良好)/總例數×100%。③ 術后隨訪6個月,采用Harris評分[8]評估髖關節功能,包括疼痛、功能、關節活動度、肢體畸形等項目,總分100分, ≥90分為優, 80~<90分為良, 70~<80分為可, <70分為差。④ 統計患者術后6個月內并發癥發生情況,計算并發癥發生率。
1.4 統計學方法
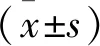
2 結 果
2組一般資料比較,差異無統計學意義(P>0.05), 見表2。觀察組住院時間、骨折愈合時間短于對照組,差異有統計學意義(P<0.05), 見表3。觀察組復位滿意率高于對照組,差異有統計學意義(P<0.05), 見表4。觀察組術后3、6個月的Harris評分高于對照組,差異有統計學意義(P<0.05), 見表5。觀察組并發癥發生率低于對照組,差異有統計學意義(P<0.05), 見表6。
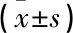
表2 2組一般資料比較
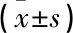
表3 2組術后恢復情況比較

表4 2組復位效果比較[n(%)]
表5 2組髖關節Harris評分比較
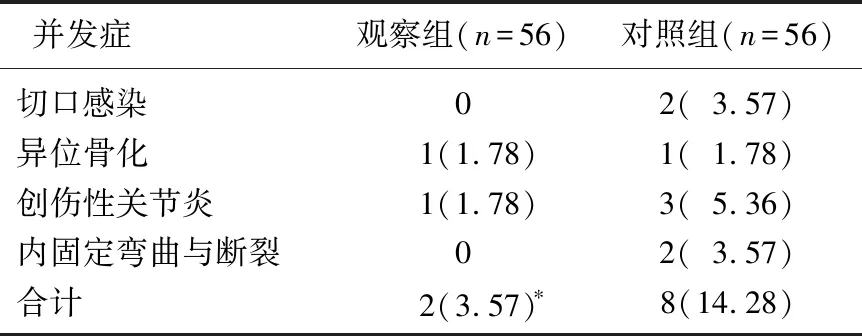
表6 2組術后并發癥發生情況比較[n(%)]
典型病例分析: 患者男性, 38歲,Letournel-Judet分型為“T”型骨折,采取3D打印結合橋接固定系統治療,取得滿意的復位效果,隨訪結果顯示骨折愈合良好。術前X線檢查提示骨盆及髖臼骨折,術前CT檢查顯示骨盆及髖臼骨折情況, 3D打印骨折模型直觀顯示骨盆及髖臼骨折情況; 術前骨折模擬復位,有限元分析設計內固定物大小、形狀及固定位置的正位效果; 術前骨折模擬復位,有限元分析設計內固定物大小、形狀及固定位置的側位效果; 3D打印骨折復位模型,進行手術固定設計制作; 術后X線片提示骨折復位固定良好; 術后2個月復查X線片提示骨折愈合良好。見圖1。
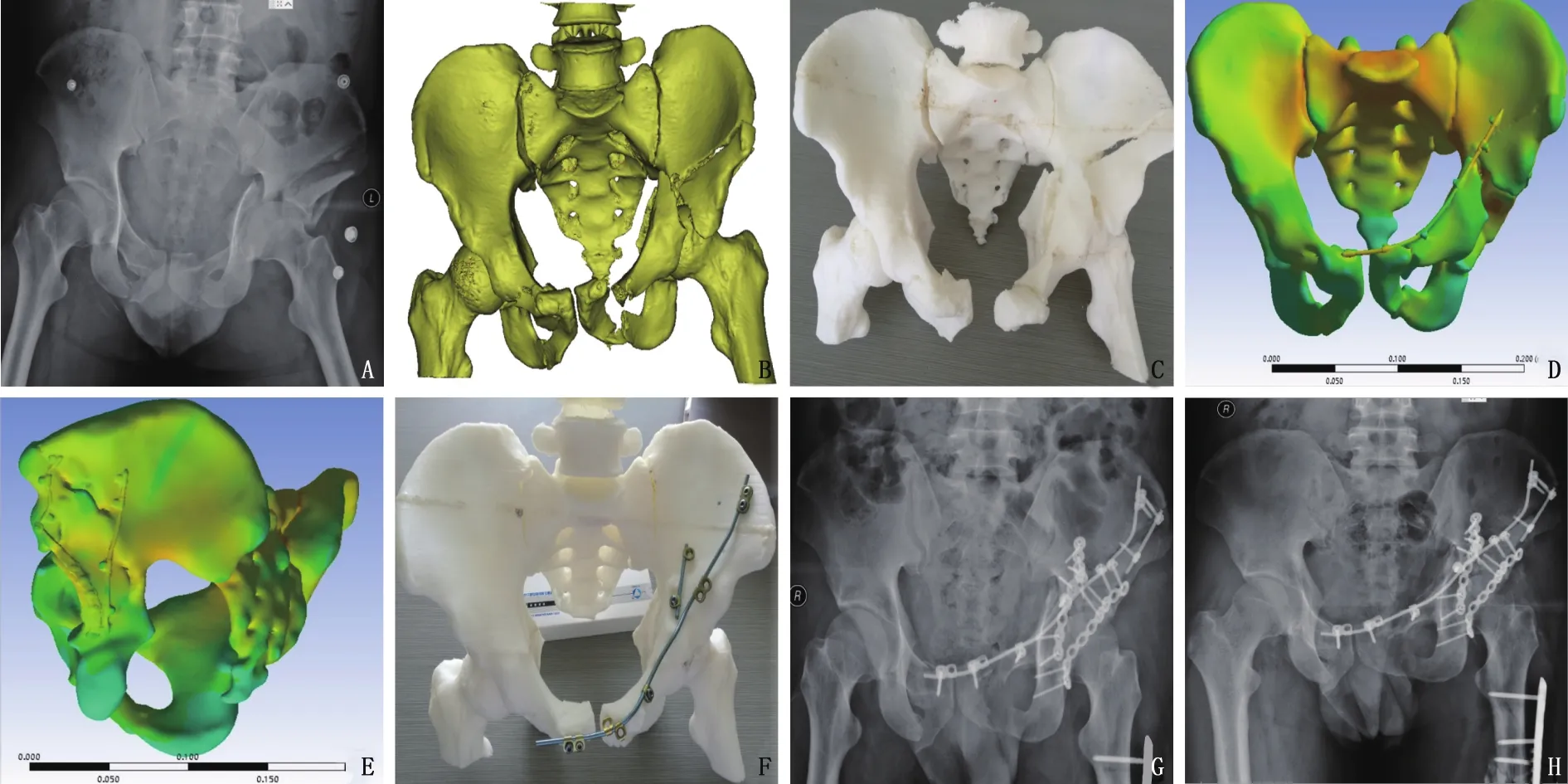
A: 術前X線檢查; B: 術前CT檢查; C: 3D打印骨折模型; D: 術前骨折復位模擬;E: 復位模型的有限元分析; F: 基于骨折復位模型的手術固定設計; G: 術后即刻X線檢查; H: 術后2個月X線復查。
3 討 論
粉碎性復雜髖臼骨折移位形式復雜,手術難度大,復位與固定是手術成功的關鍵。傳統鋼板內固定存在較大局限性及主觀性,術中復位效果依賴于術者臨床經驗,存在創傷大、復位不理想等缺點[9]。醫學3D打印多基于CT或MRI原始數據來建立三維模型并完成打印。有限元分析是建立三維數字模型后進行的模擬力學測試,近年來已逐漸用于膝關節、髖關節骨折手術患者治療中[10]。有限元分析可模擬不同咬合狀態下的力學效應,運算骨折內固定取出前的骨愈合模型及內固定取出后的穩定性,同時預判內固定斷裂風險。
本研究創新性地將3D打印與橋接固定系統結合,根據術前模型個性化預構橋接組合內固定系統,依據解剖部位、應力強度等實施個性化手術,術后3、6個月觀察組的Harris評分均高于對照組,髖關節功能恢復優于對照組,差異均有統計學意義(P<0.05), 考慮與橋接系統通過多方向螺釘置入實現多維固定,具有更強的抗剪切、抗旋轉及抗彎曲作用,精確預彎可增強橋接固定系統與骨面的貼合程度,以及獲得更高的固定生物力學性能有關[11-12]。本研究中,觀察組復位滿意率達83.93%, 高于對照組的66.07%, 差異有統計學意義(P<0.05), 與既往研究[13-14]結論一致。
觀察組采用3D打印技術在術前打印出原始骨折模型及復位模型,預測手術難度及演練手術操作,同時使用復位模型精準預構橋接組合式系統,并進行醫學有限元分析,而后精準植入機體,有利于減輕手術創傷。觀察組僅需要進行有限切開復位,實現了微創治療[15],因此住院時間及骨折愈合時間較對照組縮短。本研究中,對照組2例內固定彎曲或折斷主要是因內固定放置不當導致應力過分集中以及與骨質接觸不良造成。橋接鋼板安裝更為靈活,經有限元分析定位螺絲釘部位,減小了應力集中,避免了術后內固定彎曲或折斷。創傷性關節炎的發生多因移位的髖臼骨折未能準確復位,術后在肢體行走與活動過程中不斷摩擦周圍相關關節及組織而誘發[16]。異位骨化、切口感染等多因軟組織創傷大引起,觀察組采取有限切開復位,減輕手術創傷,是觀察組并發癥發生率低于對照組的主要原因。
本研究的不足有: ① 研究證據等級不高,缺乏中遠期療效評價; ② 3D打印制備骨折模型、預彎橋接固定系統等均是在排除骨折周圍血管、神經的情況下進行的,實際上過多地暴露、分離軟組織可能會造成“二次創傷”; ③ 研究樣本量較少,缺乏大宗數據結果。值得注意的是, 3D打印結合橋接固定系統的術前準備時間較長,患者術前住院時間會相應延長,增加了住院花費; 個性化預構橋接固定系統需針對患者實際情況進行個性化設計與優化,治療費用也會明顯增加,會加重部分患者經濟負擔,臨床應用可能受限。
綜上所述, 3D打印結合橋接固定系統進行有限元分析在治療粉碎性復雜髖臼骨折患者中效果顯著,可獲得滿意的復位與固定效果,減少術后并發癥,促進髖關節恢復。

