早產兒出生時骨代謝狀況相關因素分析
汪海波 王玉美 潘兆軍 陳 瑩▲ 林小飛 劉 娟
1.揚州大學醫學院附屬淮安市婦幼保健院兒科,江蘇淮安 223002;2.揚州大學醫學院附屬淮安市婦幼保健院兒童保健科,江蘇淮安 223002;3.揚州大學醫學院附屬淮安市婦幼保健院新生兒科,江蘇淮安 223002
早產兒骨骼發育情況對于成年期的骨骼健康尤為重要。目前與早產兒骨代謝相關的指標有血清鈣、磷、堿性磷酸酶、甲狀旁腺激素、25 羥維生素D 等,早產兒出生時鈣、磷及維生素D 儲備不足,骨代謝活躍,易發生骨代謝指標的異常[1]。近年來研究發現[2-3],胰島素樣生長因子-Ⅰ(insulin like growth factor-Ⅰ,IGF-Ⅰ)在成骨細胞的協同作用下可作用于破骨細胞,促進骨吸收,其作為一種新的骨代謝指標正逐步被人們所接受。本研究以在新生兒重癥監護室(NICU)住院治療的早產兒為研究對象,通過檢測其出生時血清鈣、磷、堿性磷酸酶、25-羥維生素D 及IGF-Ⅰ水平,分析其與早產兒胎齡、體重、生長等因素的內在聯系,為臨床預防早產兒骨代謝疾病提供參考。
1 資料與方法
1.1 一般資料
收集2017 年3 月—2018 年2 月揚州大學醫學院附屬淮安市婦幼保健院NICU 住院治療的287 例早產兒為研究對象。根據胎齡將早產兒分為<32 周組(68 例)、32~33+6周組(77 例)、≥34 周組(142 例);根據體重分為<1500 g 組(38 例)、1500~2499 g 組(202 例)、≥2500 g 組(47 例);根據出生時體重與胎齡的關系分類[4]分為小于胎齡兒組(SGA 組,50 例)、適于胎齡兒組(AGA 組,231 例)與大于胎齡兒組(LGA 組,6 例)。
胎齡<32 周組,男40 例,女28 例;出生體重900~2600 g,平均(1556.91±310.09)g。32~33+6周組,男45例,女32 例;出生體重1110~2670 g,平均(1937.14±344.57)g。≥34 周組,男70 例,女72 例;出生體重1180~4100 g,平均(2318.03±434.76)g。<1500 g 組,男19 例,女19 例;出生胎齡27+1~35+3周,平均(30.98±2.19)周。1500~2499 g 組,男109 例,女93 例;出生胎齡27+3~36+6周,平均(33.57±1.89)周。≥2500 g 組,男27例,女20 例;出生胎齡30+4~36+6周,平均(35.23±1.21)周。不同分組依據中早產兒性別比較,差異無統計學意義(P >0.05),具有可比性。本研究經醫院醫學倫理委員會批準,所有患兒家屬和/或監護人均知情同意并簽署知情同意書。
排除出生胎齡≥37 周;入院日齡≥2 h;無完整的入院時生長指標(體重、身長、頭圍)等資料;患有先天性遺傳代謝病,青紫型先天性心臟病或伴有心功能不全,消化道畸形,內分泌異常,新生兒期行各種外科手術治療者;母親患有嚴重內分泌、代謝性疾病者。
1.2 方法
記錄所有早產兒完整的入院生長指標(體重、身長、頭圍)等資料,采集外周靜脈血2 mL 分離血清,全自動生化分析儀測定血清鈣、磷、堿性磷酸酶水平,全自動化學發光免疫分析儀測定25-羥維生素D 和IGF-Ⅰ水平。
1.3 觀察指標
分別對早產兒孕齡、體重、身長等進行統計,檢測早產兒出生后2 h 內血清鈣、磷、堿性磷酸酶、25-羥維生素D 和IGF-Ⅰ水平。
1.3.1 主要儀器 AU 5800 型全自動生化分析儀(美國Beckman 公司);MAGLUMI 4000 型全自動化學發光免疫分析儀(深圳新產業生物醫學工程股份有限公司)。
1.3.2 試劑來源 血清鈣試劑(17100512)、血清磷試劑(20180312)及定標液(915UE)由英國朗道公司提供;血清堿性磷酸酶試劑(20171201)由上海科華公司提供;血清25-羥維生素D 試劑盒及定標液(103171103 02)、血清IGF-Ⅰ試劑盒及定標液(10018001012)均由深圳新產業生物醫學工程股份有限公司提供。
1.4 統計學方法
采用SPSS 21.0 統計學軟件進行數據分析,計量資料用均數±標準差(±s)表示,多組間比較采用單因素方差分析,兩兩比較采用LSD-t 檢驗;不符合正態分布的改用中位數(M),四分位間距(Q)表示,兩組間比較采用Kruskal-Wallis 檢驗。計數資料用例數或百分率表示,組間比較采用χ2檢驗。相關性用Pearson相關分析。以P <0.05 為差異有統計學意義。
2 結果
2.1 不同胎齡組早產兒出生時骨代謝相關指標比較
不同胎齡組早產兒血清磷、堿性磷酸酶、25-羥維生素D 水平比較,差異無統計學意義(P >0.05);而不同胎齡組血清鈣、IGF-Ⅰ水平比較,差異有統計學意義(P <0.05)。≥34 周組血清鈣水平高于<32 周組及32~33+6周組,32~33+6周組血清鈣水平高于<32 周組,差異均有統計學意義(均P <0.05)。≥34 周組、32~33+6周組IGF-Ⅰ水平高于<32 周組,差異均有統計學意義(均P <0.05)。見表1。

表1 不同胎齡組早產兒出生時骨代謝指標比較
2.2 不同體重組早產兒出生時骨代謝相關指標比較
不同體重組血清磷、堿性磷酸酶、25-羥維生素D水平比較,差異無統計學意義(P >0.05);而不同體重組血清鈣、IGF-Ⅰ水平比較,差異有統計學意義(P <0.05)。≥2500 g 組、1500~2499 g 組血清鈣、IGF-Ⅰ水平高于<1500 g 組,差異均有統計學意義(均P <0.05)。見表2。
2.3 早產兒出生時骨代謝指標與出生時身長的相關性分析
287 例早產兒出生時身長37.0~50.0 cm,平均(43.99±3.10)cm。血清鈣與出生時身長呈正相關(r=0.419,P <0.05);IGF-Ⅰ水平與出生時身長呈正相關(r=0.221,P <0.05);而血清磷、堿性磷酸酶及25-羥維生素D與出生時身長均無明顯相關性(r=-0.064、0.018、0.094,P >0.05)。
2.4 SGA 組、AGA 組及LGA 組早產兒出生時骨代謝相關指標比較
SGA 組、AGA 組及LGA 組血清鈣、堿性磷酸酶、25-羥維生素D 及IGF-Ⅰ水平比較,差異無統計學意義(P >0.05)。SGA 組、AGA 組及LGA 組血清磷水平比較,差異有統計學意義(P <0.05)。AGA 組血清磷水平高于SGA 組,差異有統計學意義(P <0.05)。見表3。
3 討論
骨骼是一個動態活性組織,其生長發育包括骨骼的延長、塑型及重塑,這個生物學過程及其復雜[5]。新生兒由于其骨骼生長的特殊性,易受體重、胎齡、營養和疾病等因素的影響。早產兒因其骨礦物質的存儲不充足,加上自身組織器官功能發育不完善、并發癥的出現及追趕生長等多因素的影響,因此更易出現骨代謝的紊亂,發生代謝性骨病[6]。本研究以NICU 早產兒為研究對象,通過檢測出生時骨代謝指標(血清鈣、磷、堿性磷酸酶、25-羥維生素D 及IGF-Ⅰ)水平,尋找影響早產兒早期骨代謝的重要指標,為臨床預防早產兒骨代謝疾病提供參考。
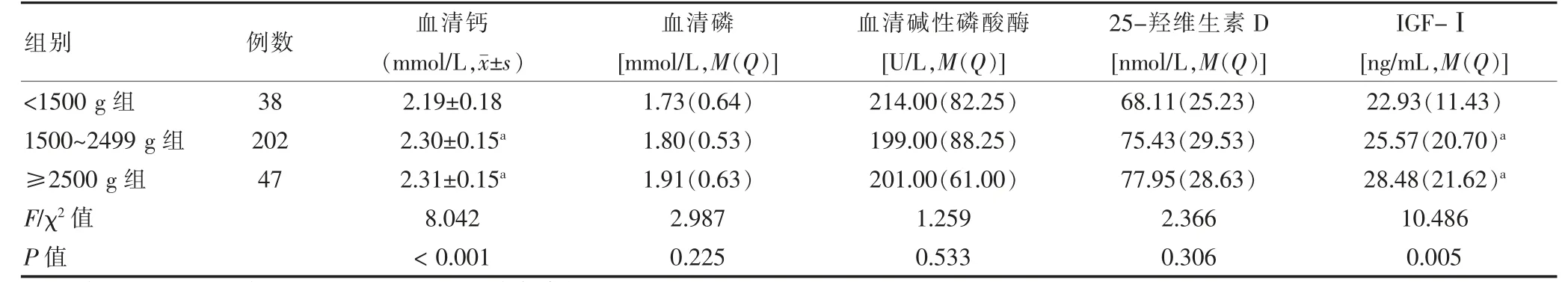
表2 不同體重組早產兒出生時骨代謝指標比較
本研究結果顯示,≥34 周組、32~33+6周組血清鈣水平高于<32 周組;≥2500 g 組、1500~2499 g 組血清鈣水平高于<1500 g 組(均P <0.05)。與滕志麗等[7]研究結果相似。原因可能是鈣經胎盤輸入胎兒的量從孕晚期才逐漸增多,而在宮內時間越少,鈣儲備時間越短,由于甲狀旁腺功能尚未發育成熟,腎環磷酸腺苷(cAMP)對甲狀旁腺反應低下,尿磷排泄減少,維生素D 代謝異常,因而早產兒無法對血鈣水平進行合理的調節[8],故胎齡越小,出生時的血鈣越低,與相關資料[9]描述一致。因此孕期注意鈣營養補充有助于新生兒骨骼發育,改善骨代謝水平[10]。
Langdahl 等[11]的體外研究顯示,IGF-Ⅰ是骨骼中含量豐富的生長因子,可以增強成骨細胞的生長、聚集、合成及分泌功能,具有促進成骨細胞的成骨作用。Chiesa 等[12]研究結果顯示,新生兒體格發育指標如出生體重、身長、頭圍及體重指數與其血清IGF-Ⅰ水平呈正相關。本研究結果顯示,小胎齡組和低體重組早產兒的血清IGF-1 水平較低,且IGF-Ⅰ水平與早產兒出生時身長呈正相關,與國內研究結果[13-14]相符。de Jong 等[15]報道極低出生體重兒的早期IGF-Ⅰ水平對于追趕生長具有重要意義。張永芬[16]發現血清IGF-Ⅰ與胎兒生長受限存在一定的相關性,故監測IGF-Ⅰ可能對早產兒早期的生長及營養有用處[17],其可以作為評估骨代謝的新指標,用于評價早產兒早期骨營養狀況。
另外,本研究結果顯示,SGA 組血清磷水平低于AGA 組,差異有統計學意義(P <0.05);而堿性磷酸酶水平高于AGA 組,差異無統計學意義(P >0.05);與楊火燃等[18]研究相符。高血清堿性磷酸酶水平是早期發現代謝性骨病的最佳生化指標[19]。代謝性骨病(MBD)多發生于出生后10~16 周,其診斷基于臨床表現、影像學檢查、生化檢測和骨密度監測[20],但只有到骨質減少20%~40%才發現,也就是說早產兒代謝性骨病早期很難發現。且32 周以下早產兒MBD 發生率較高,尤其是合并宮內發育遲緩的早產兒或極低出生體重兒[21]。有資料顯示血堿性磷酸酶、血磷值有助于MBD 的早期診斷[22]。動態監測骨代謝生化標志物的變化對早期發現骨代謝異常,及時治療和防止骨質疏松、骨折的發生是非常重要的[23]。對易發生代謝性骨病的高危早產兒及時有效的補充骨礦物質營養素,并定期進行血清堿性磷酸酶、磷、鈣等指標的監測,有助于預防MBD[24]。
綜上所述,評價早產兒早期骨代謝狀況,要關注其血清中骨代謝指標的水平,血清鈣、磷和IGF-Ⅰ與早產兒(尤其是極早產兒和極低出生體重兒)出生時生長和營養狀況密切相關。早產兒住院期間不僅應重視液體及能量支持,也應適時的監測這些骨代謝指標的動態變化,及時補充生長所需的鈣磷等礦物質及適量的維生素D[25],促進其骨骼的健康生長,預防MBD的發生。

