MRI常規序列聯合磁共振動態增強掃描成像及彌散加權成像序列在卵巢腫瘤診斷中的應用
魏明忠
京山仁和醫院放射科 (湖北京山 431800)
卵巢腫瘤是嚴重危害女性身心健康的疾病,尤其是卵巢惡性腫瘤,會影響女性的生殖健康,并降低其生命質量。目前,臨床主要采用手術治療卵巢腫瘤患者,可較好地控制病情,而早期確診治療、術前腫瘤性質的判斷與手術效果密切相關,并可對預后產生影響。目前,在腫瘤的篩查中,MRI應用較廣泛,具有較高的分辨力,且可多平面、多序列、多參數成像,有助于直觀、清晰地探查病灶結構[1]。在現代影像學新技術的研究與應用中,磁共振動態增強掃描成像(dynamic contrast enhanced MRI,DCE-MRI)、彌散加權成像(diffusion-weighted imaging,DWI)等檢查手段可提供腫瘤量化指標[2]。鑒于此,本研究探討在MRI常規序列檢查卵巢腫瘤中聯合應用DCE-MRI及DWI序列的診斷效能,現報道如下。
1 資料與方法
1.1 一般資料
收集我院2017年1月至2020年1月收治的150例卵巢腫瘤患者的臨床資料,將79例良性腫瘤患者納入良性組,71例惡性腫瘤患者納入惡性組。良性組年齡33~65歲,平均(46.24±5.31)歲。惡性組年齡30~66歲,平均(46.58±5.64)歲。兩組一般資料比較,差異無統計學意義(P>0.05),具有可比性。本研究經醫院醫學倫理委員會批準,患者均已簽署研究知情同意書。 納入標準:經手術病理證實;術前行常規MRI、DCE-MRI、DWI檢查;無嚴重精神系統疾病;具有全面的診斷及臨床資料。排除標準:術前放化療;存在其他惡性腫瘤;心、肝、腎等器官功能異常。
1.2 方法
患者術前均采用磁共振掃描儀(美國GE公司,1.5T超導型)行常規MRI、DCE-MRI及DWI檢查。(1)MRI常規序列:即快速自旋回波序列,設置橫軸位T1加權像(T1weighted image,T1WI) 回波時間(Echo time,TE)為12 ms,重復時間(Repetition time,TR)為450 ms,視野(field of view,FOV)為250 mm×250 mm;矢狀位T2加權像(T2WI) TE為91 ms,TR為3 310 ms,FOV為230 mm×230 mm;橫軸位T2WI TE為87 ms,TR為2 512 ms,FOV為250 mm×250 mm。(2)DWI掃描:設置TE為77 ms,TR為5 000 ms,FOV為306 mm×306 mm,層厚為5 mm,彌散敏感系數為0、800 s/mm2。(3)DCE-MRI掃描:行T1-vibe-fs掃描,設置TE為1.39 ms,TR為4.09 ms,FOV為260 mm×260 mm,層厚為3.5 mm,反轉角為2°、15°;采用高壓注射器,選擇釓噴酸葡胺注射液(北京北陸藥業股份有限公司,國藥準字H20013088,12 ml:5.63 g)作為對比劑,在肘正中靜脈處以4 ml/s速度注入,并用20 ml 0.9%氯化鈉注射液沖洗,設置增強掃描參數TE為1.77 ms,TR為5.08 ms,FOV為260 mm×260 mm,層厚為3.5 mm,共采集35次。(4)圖像分析:由工作站接收DWI圖像并進行處理,獲取表觀彌散系數(apparent diffusion coeffecient,ADC)圖,在病灶囊性及實性區域設置感興趣區(region of interest,ROI),測量3次,并取平均值為最終ADC值;采集DCE-MRI圖像后,設置ROI,測量血管外細胞外容積分數(extravascular extracellular volume fraction,Ve)、速率常數(rate constant,Kep)、容量轉運參數(volume transfer con-stant,Ktrans),結果取3次的均值。
1.3 臨床評價
比較兩組的ADC值、DCE-MRI參數(Kep、Ve、Ktrans),并分析單項及聯合診斷的效能。
1.4 統計學處理
2 結果
2.1 ADC值
惡性組囊性及實性部分的ADC值均小于良性組,差異有統計學意義(P<0.05),見表1。
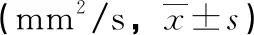
表1 兩組ADC值比較
2.2 DCE-MRI參數
惡性組Ve、Kep、Ktrans均高于良性組,差異有統計學意義(P<0.05),見表2。
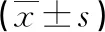
表2 兩組DCE-MRI參數比較
2.3 診斷價值
MRI常規序列聯合DCE-MRI及DWI序列診斷的準確度、特異度、靈敏度均高于各單項診斷,見表3~4。
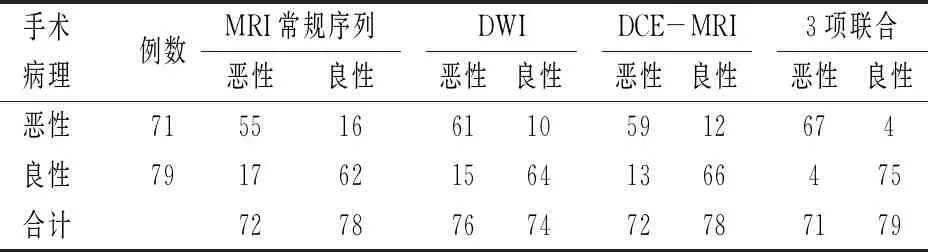
表3 單項及聯合診斷的結果分析(例)
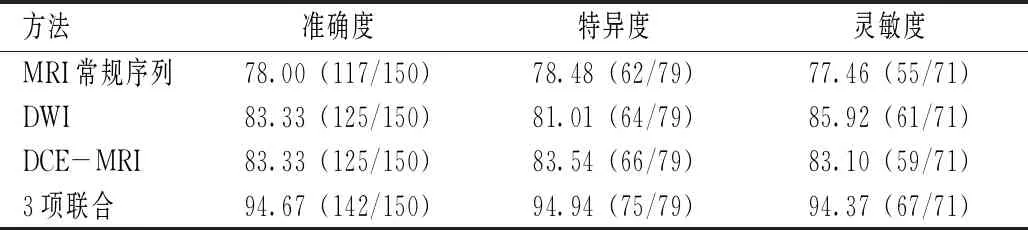
表4 單項及聯合診斷的準確度、特異度、靈敏度比較(%)
3 討論
卵巢腫瘤包括良性及惡性兩種類型,因組織種類繁多,且來源較廣,同時存在實質成分不豐富、多間隔、多囊等問題,導致腫瘤良惡性鑒別困難。卵巢惡性腫瘤的病死率在婦科惡性腫瘤中居首位,患者5年生存率較低,且病死率持續增高[3],因此,為提高卵巢腫瘤患者的生命質量,尋求一種有效的診斷方法對早期確診治療尤為重要。
目前,臨床常采用MRI診斷卵巢腫瘤,作為無創檢查手段,其無放射性,安全性較高,同時可多參數、多方位成像,軟組織對比較好,可清晰顯示病灶部位及卵巢結構[4]。MRI常用序列為DWI,基于組織中水分子,顯示微觀運動成像,并通過ADC值量化;而水分子運動易受細胞密度、血管通透性等的影響,且隨著組織內外間隙、數量、密度等的變化,ADC值具有差異性[5]。在MRI常規序列檢查中常采用DCE-MRI補充,利用對比劑藥代動力學特點,可動態觀察強化全程,同時可獲取病灶血流灌注情況,并可提供客觀的參數[6]。本研究結果顯示,與良性組比較,惡性組囊性及實性部分的ADC值均較小,Ve、Kep、Ktrans均較高,表明DWI及DCE-MRI均可用于腫瘤良惡性的鑒別中,分析原因在于,惡性病變的腫瘤細胞間隙較小,密集度更高,且體積更大,會限制并制約水分子彌散,故ADC值較小;此外,DCE-MRI參數受細胞外滲空間、血管床滲透性、微血管密度、血流灌注等的影響,而卵巢腫瘤可通過不同的血流學信息判斷良惡性。本研究結果顯示,MRI常規序列聯合DCE-MRI及DWI序列診斷的準確度、特異度、靈敏度均較各單項診斷高,提示在應用MRI常規序列篩查卵巢腫瘤的基礎上,聯合應用DCE-MRI及DWI序列的診斷效能較高。因此,在卵巢腫瘤應用DCE-MRI及DWI序列等量化分析的基礎上,可結合MRI常規序列,對腫瘤良惡性進行綜合評估,以提高診斷準確度。
綜上所述,在MRI常規序列檢查卵巢腫瘤中,聯合應用DCE-MRI及DWI序列的診斷效能較高,可為疾病的臨床診療提供可靠的影像學資料。