復方乳酶生散雜菌檢查方法驗證
劉興國 劉 荔 王月玲 田妮娜
(蘭州市食品藥品檢驗所,甘肅 蘭州 730050)
復方乳酶生散是胰酶與乳酶生組成的復方制劑,由乳酶生、胰酶和葡萄糖組成,治療消化不良、腹瀉、腹脹、小兒厭食等。其活性成分乳酶生為傳統的活菌素,具有微生態活菌制品的特性。雜菌是復方乳酶生散質量控制的重要指標。中國藥典2015年版三部微生態活菌制品總論項下列出雜菌檢查法,但并沒有列出不同活菌制劑具體檢測雜菌的方法[1]。為了檢測復方乳酶生散的微生物限度,根據中國藥典非無菌產品微生物限度檢查法(四部附錄1105/1106)和微生態活菌制品雜菌檢查法的要求,對復方乳酶生散雜菌檢查項目中的控制菌檢查、非致病性雜菌和真菌計數分別開展了適用性研究,建立了復方乳酶生散雜菌檢查方法。
1 儀器與材料
1.1 儀器:梅里埃VITEK 2 Compact 全自動細菌鑒定及藥敏分析系統,恒溫振蕩培養箱。
1.2 菌株:大腸埃希菌[CMCC(B)44102]、枯草芽孢桿菌[CMCC(B)63501]、銅綠假單胞菌[CMCC(B)10104]、金黃色葡萄球菌[CMCC(B)26003]、乙型副傷寒沙門菌[CMCC(B)50094]、痢疾志賀菌[CMCC(B)51252]和白色念珠菌[CMCC(F)98001]均由中國食品藥品檢定研究院提供。
1.3 培養基:胰酪大豆胨液體培養基(TSB),胰酪大豆胨瓊脂培養基(TSA),沙氏葡萄糖液體培養基(SDB),沙氏葡萄糖瓊脂培養基(SDA),營養瓊脂,玫瑰紅鈉,膽鹽乳糖培養基,曙紅亞甲藍瓊脂培養基,沙門、志賀菌屬瓊脂培養基,甘露醇氯化鈉瓊脂培養基,北京陸橋技術股份有限提供。7.5%氯化鈉肉湯培養基NAC液體培養基、NAC液體培養基由青島海博生物技術有限公司提供。以上培養基適用性檢查均符合規定。
1.4 樣品:復方乳酶生散(醫院制劑,批號:12011,12012,12013,活菌含量5×108cfu/g)。
2 結果
2.1 菌液制備:將枯草芽孢桿菌、銅綠假單胞菌、金黃色葡萄菌、大腸埃希菌、乙型副傷寒沙門菌、痢疾志賀菌分別接種于胰酪大豆胨液體培養基中,培養溫度30~35 ℃,培養時間18~24 h;將白色念珠菌接種于沙氏葡萄糖瓊脂培養基(SDB)中,培養溫度20~25 ℃,白色念珠菌培養時間為2~3 d。每種新鮮培養物用0.9%無菌氯化鈉溶液制成適宜濃度的菌懸液,備用。
2.2 供試品的處理:稱取本品1 g,加到9 ml0.9%無菌氯化鈉溶液制成1∶10供試液[1]。
2.3 非致病性雜菌、真菌計數方法適用性試驗:①試驗組:取1∶10供試液4份,分別加入制備好的菌懸液0.1 mL,混勻,使0.1 mL供試液中含菌量含菌數50~100 cfu。非致病性雜菌:取供試液0.1 mL,加到已備好的磷酸鹽緩沖液營養瓊脂培養基[每1000 mL營養瓊脂培養基中,加人磷酸二氫鉀3.56 g、磷酸氫二鈉7.23 g,溶解,混勻,分裝,121 ℃濕熱滅菌20 min上],以L形涂布棒涂勻,一式3份,倒置,置30~37 ℃培養,在48 h內觀察結果[1]。真菌:取供試液0.1 mL,加到已備好的玫瑰紅鈉瓊脂培養基基上,以L形涂布棒涂勻,一式3份,倒置,置20~28 ℃培養,在96 h內觀察結果[1]。②供試品對照組:測定供試品的含菌量。③菌液對照組:測定每一菌株的試驗菌數。見表1。
2.4 控制菌檢查方法驗證
2.4.1 大腸埃希菌檢查方法適用性試驗:取供試品lg,加到9 mL膽鹽乳糖培養基中制成1∶10的勻液,加入不大于100 cfu的大腸埃希菌,混勻,培養18 h,取上述培養物0.1 mL滴加到曙紅亞甲藍瓊脂平皿上,以L形涂布棒涂勻,一式3份,培養18 h,曙紅亞甲藍瓊脂平皿呈紫黑色帶有金屬光澤的典型菌落。陰性對照組及供試品對照組均無菌落生長。
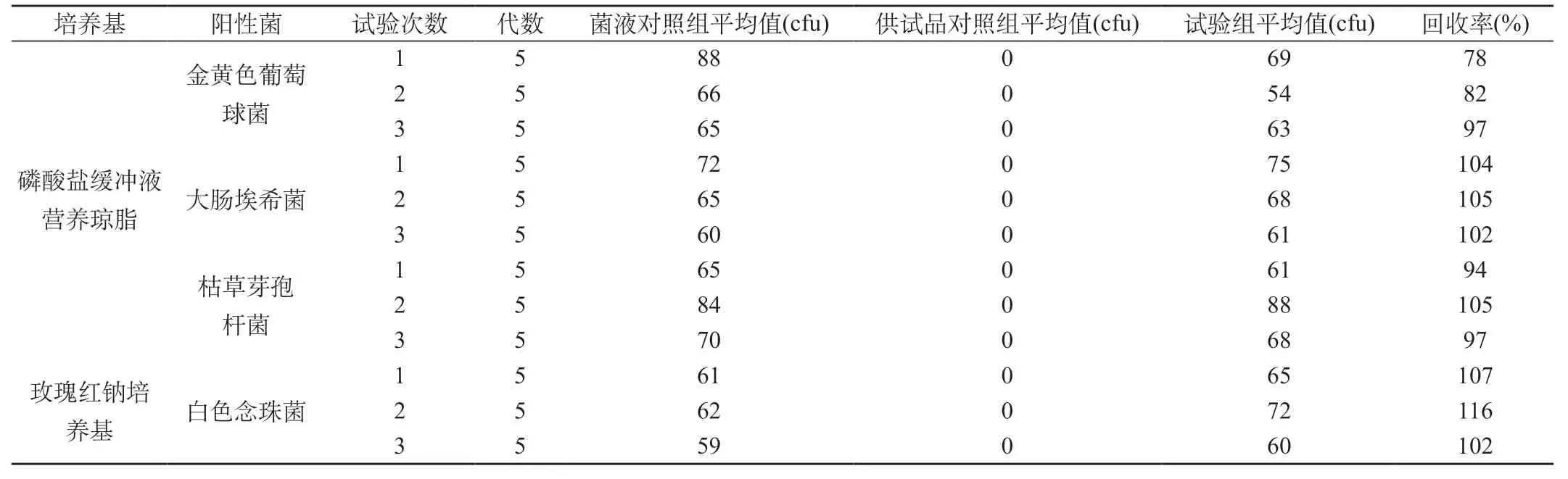
表1 非致病性雜菌、真菌計數試驗結果
2.4.2 志賀菌、沙門菌檢查方法適用性試驗:取供試品l g,加到9 mL膽鹽乳糖培養基中制成1∶10的勻液,制備兩份,分別加入不大于100 cfu的痢疾志賀菌、乙型副傷寒沙門菌,混勻,培養18 h,取上述培養物0.1 mL滴加到沙門、志賀菌屬瓊脂平皿上,以L形涂布棒涂勻,一式3份,培養24 h,乙型副傷寒沙門菌在沙門、志賀菌屬瓊脂平皿呈無色透明、中心呈黑褐色的菌落。痢疾志賀菌在沙門、志賀菌屬瓊脂平皿呈無色、半透明、微凸、光滑的菌落。陰性對照組及供試品對照組均無菌落生長。
2.4.3 銅綠假單胞菌檢查方法適用性試驗:取供試品1 g,加到9 mL NAC液體培養基中制成1∶10的勻液,加入不大于100 cfu的銅綠假單胞菌,混勻,培養18 h,取上述培養物0.1 mL滴加到NAC瓊脂平皿上,以L形涂布棒涂勻,一式3份,培養18 h,NAC瓊脂平皿呈產綠色色素的菌落。陰性對照組及供試品對照組均無菌落生長。
2.4.4 金黃色葡萄球菌檢查方法適用性試驗:取供試品1 g,加到9 mL 7.5%氯化鈉肉湯培養基中制成1∶10的勻液,加入不大于100 cfu的金黃色葡萄球菌,混勻,培養18 h,取上述培養物0.1 mL滴加到甘露醇氯化鈉瓊脂平皿上,以L形涂布棒涂勻,一式3份,培養18 h,甘露醇氯化鈉瓊脂平皿呈金黃色菌落。陰性對照組及供試品對照組均無菌落生長。
3 討論
3.1 微生態制劑雜菌含量檢測常用的方法為顯微鏡檢法和微生物學檢驗法。顯微鏡檢法無法確切區分活菌、死菌和雜菌,只能大致了解微生物的數量;微生物學檢驗法主要通過平板法進行計數[2]。中國藥典2015年版雜菌檢查法采用涂布法進行檢測。本實驗控制菌檢查和真菌計數將供試液涂布于選擇性培養基平板的方法對復方乳酶生散進行適用性檢查,結果滿足要求。由于樣品中含活菌數高達5×108cfu/g以上,非致病性雜菌的菌落數限度僅為樣品的1/500000(中國藥典規定口服微生態活菌制品成品的非致病性雜菌數不得超過1000 cfu/g)[3],在非選擇性平板上巨量的活菌會掩蓋雜菌,使菌落計數非常困難,主要由于大量活菌產生乳酸改變培養基酸堿度,從而抑制雜菌的生長,因此為了增加培養基緩沖能力,使其pH值保持相對穩定,試驗中改用磷酸緩沖液營養瓊脂培養基,有效降低活菌對雜菌檢查的干擾[4]。
3.2 雜菌檢查法要求進行控制菌、非致病性雜菌總數及真菌數檢查。復方乳酶生散采用常規方法均能滿足方法適用性要求。
3.3 復方乳酶生散為醫院制劑,歸屬生化藥品管理,在執行微生物限度檢查時,一般會出現活菌和雜菌之間相互干擾的情況,結果判斷困難。本研究改良培養基的緩沖能力,有效降低了活菌的干擾。

