通陽利濕方對腰椎間盤突出癥大鼠的影響
程 杰, 王 鵬, 關勝江, 趙 建, 張春旭, 趙 倩, 張裕翔
(河北省中醫院,河北 石家莊050000)
腰椎間盤突出癥是當今社會常見病、多發病,也是引起腰腿痛最常見的原因,其臨床癥狀大多因腰椎間盤退變、纖維環破裂、髓核向后方突出或突至椎板內,致使相鄰組織受刺激或壓迫而出現,以L4-5、L5-S1間隙發病率最高[1]。腰椎間盤突出癥急性期疼痛劇烈,腰椎功能嚴重受限,極大影響了患者生存質量,如果治療不當轉為慢性,則病情反復發作,遷延難愈。
該疾病屬于中醫“腰腿痛” “痹證” 范疇[2]。通陽利濕方是河北省中醫院名中醫趙建教授在多年臨床經驗基礎上確定的方劑,由黃芪、桂枝、木瓜、蠶沙、白芍、白術、茯苓等成,具有補陽通脈、運化水濕功效,在臨床使用多年,療效顯著,但作用機制不明。因此,本實驗從抑制炎癥因子、調節細胞外基質合成角度考察通陽利濕方對腰椎間盤突出模型大鼠的影響,以期為治療該疾病提供科學依據。
1 材料
1.1 藥物 通陽利濕方由黃芪、桂枝、木瓜、蠶沙、白芍、白術、茯苓、青風藤、澤瀉、苦杏仁、絲瓜絡、漢防己、桑枝、薏苡仁、狗脊、懷牛膝、路路通、酒大黃、獨活、姜黃、威靈仙組成,藥材購自河北省中醫院,經國藥樂仁堂石家莊藥材有限公司專家鑒定為正品,制備方法為頭煎加800 mL 水,煎至300 mL 濾出,然后加500 mL 水煎至300 mL,濾出,兩煎相兌后濃縮到最濃。陽性藥為腰痛寧膠囊(頸復康藥業集團有限公司,生產批號620153,0.3 g/粒),內容物用0.5%羧甲基纖維素鈉溶解,配制0.02 g/mL 混懸液。注射用青霉素鈉(哈藥集團制藥總廠,生產批號16121205-1),160 萬單位/支。
1.2 動物 SPF 級雄性SD 大鼠70 只,體質量180~200 g,由河北醫科大學實驗動物中心提供,實驗動物使用許可證號SYXK(冀)2013-1-003,動物合格證號1705188,飼養于實驗動物屏障系統中,自由進食滅菌鼠糧和攝取重蒸水,人工照明(12 h 黑暗/12 h 光照),保持溫度20~25 ℃,濕度(55±5)%。
1.3 試劑 腫瘤壞死因子(TNF-α) (批號C06PZB)、白細胞介素1β(IL-1β) (批號C09PDB)、白細胞介素6(IL-6) (批號C12PDB) 試劑盒均購自于北京北方生物技術研究所;RT-PCR 試劑盒購自寶生物工程(大連) 有限公司;Trizol 購自美國Invitroge 公司。PCR 引物序列為成纖維細胞生長因子2(FGF-2) 正向5′-CGAACCGGTACCTGGCTATG-3′,反 向5′-ACTGCCCAGTTCGTTTCAGT-3′, 預 擴 增 片 段162 bp;基質金屬蛋白酶2(MMP-2) 正向5′-AGCAAGTAGACGCTGCCTTT-3′, 反 向 5′-CAGCACCTTTCTTTGGGC AC-3′,預擴增片段469 bp;GAPDH 正 向5′-AGGAAATGATGACCTCCTGAACT-3′,反向5′-CAGGCATTGTCTGAGAG GCA-3′,預擴增片段605 bp。
1.4 儀器 756MC 型紫外-可見分光光度計,購自上海精密科學儀器有限公司;PE9600 型PCR 擴增儀,購自美國PE 公司;電泳儀、電泳槽,購自北京六一儀器廠;MDF-382E 超低溫保存箱,購自日本SANYO 公司;1-15K 高速冷凍離心機,購自美國Sigma 公司;ASB240 生物信號采集系統,購自重慶生物科技技術有限公司。
2 方法
2.1 模型制備[3]大鼠適應性飼養3 d 后禁食12 h,腹腔注射10%水合氯醛(350 mg/kg) 麻醉,俯臥位固定,距肛門1 cm 處扎緊尾部,將結扎處遠心端的尾部切下,壓迫止血并縫合,將尾椎關節椎間盤組織中乳白色膠凍樣髓核組織取出,合并后備用,背部手術區碘伏消毒,備皮,切開皮膚(長約3 cm),從左側棘突上將L5,6段腰椎鈍性分離,暴露橫突,咬除橫突及其附帶的椎板,切除左側部分L5,6段的椎板和上下關節突,將大鼠自體尾椎髓核組織(約10 mg) 植入左側L5神經根出硬膜囊的交界處,對于神經根及硬膜囊不造成壓迫,逐層縫合組織;假手術組大鼠除不植入髓核外,其余操作同模型大鼠。造模完成后,各組大鼠每天肌肉注射青霉素鈉(1.6 萬單位)1 次,連續3 d。
2.2 分組與給藥 將造模成功的大鼠按照初始痛閾值隨機分為5 組,分別為模型組、腰痛寧膠囊組(混懸液0.2 g/kg,根據不同動物等效劑量的折算系數表計算,相當于臨床等效劑量)、通陽利濕方組(60、30、15 g/kg) (依據課題組前期預實驗,進行劑量探索而定),每組10 只,另設假手術組大鼠10 只。造模成功3 d 后,各組大鼠按照10 mL/kg 劑量灌胃給藥(或蒸餾水),連續30 d。
2.3 指標測定
2.3.1 機械壓痛痛閾值 初次給藥前和末次給藥后1 h,將各組大鼠放入固定器內,左后肢暴露于外,待其安靜后將左后肢置于壓痛儀上測定痛閾值。
2.3.2 血清TNF-α,IL-1β、IL-6 水平 末次給藥后,各組大鼠禁食12 h,腹腔注射水合氯醛麻醉,腹主動脈取血,30 min 內分離血清,ELISA 法測定血清中TNF-α,IL-1β 及IL-6 水平。
2.3.3 椎間盤組織FGF-2、MMP-2 mRNA 表達 采用RTPCR 法。分離、剝取大鼠腰椎間盤組織,置于-80 ℃冰箱保存,取大鼠椎間盤組織100 mg 左右,置于勻漿器中,加適量RNAiso Plus,勻漿器勻漿后提取總RNA,將其反轉錄成cDNA,進行PCR 擴增。FGF-2 擴增條件為94 ℃預變性3 min,94 ℃變性40 s,54 ℃退火50 s,72 ℃延伸90 s,共30 個循環,72 ℃延伸10 min;MMP-2 擴增條件為52 ℃退火50 s,其余同FGF-2;GAPDH 擴增條件為55 ℃退火50 s,其余同FGF-2。取每個標本PCR 產物各6 μL,在含1%GV 核酸染料的瓊脂糖凝膠中電泳,以DNA Marker(DL2000) 為標準片段標記,電泳后以紫外透射儀觀察并拍照,采用Quantity One 圖像分析系統分別檢測各組FGF-2、MMP-2、GAPDH 電泳條帶灰度值,將兩者與GAPDH比值為mRNA 相對表達。
2.4 統計學分析 通過SPSS 19.0 軟件進行單因素方差分析,數據以() 表示,組間比較采用LSD-t 檢驗。以P<0.05 為差異具有統計學意義。
3 結果
3.1 通陽利濕方對大鼠機械壓痛痛閾值的影響 表1 顯示,模型組、腰痛寧膠囊組、通陽利濕方組大鼠初始痛閾值均顯著低于假手術組(P<0.05,P<0.01),而模型組大鼠最終痛閾值顯著低于假手術組(P<0.01);與模型組比較,通陽利濕方組大鼠最終痛閾值顯著升高(P<0.05),并且60、30 g/kg 組痛閾增加值顯著增加(P<0.05,P<0.01),但15 g/kg 組無顯著性差異(P>0.05)。
表1 通陽利濕方對大鼠機械壓痛痛閾值的影響(n=10)

表1 通陽利濕方對大鼠機械壓痛痛閾值的影響(n=10)
注:與模型組比較,*P<0.05,**P<0.01;與假手術組比較,#P<0.05,##P<0.01
組別 劑量/(g·kg-1) 初始痛閾值/g 最終痛閾值/g 痛閾增加值/g假手術組 — 345.1±111.2** 468.9±91.8** 123.3±103.7模型組 — 214.0±65.2## 272.5±81.6## 58.5±21.3腰痛寧膠囊組 0.2 240.9±61.1## 421.8±149.5** 180.9±108.3**通陽利濕方組 60 247.4±79.1## 405.0±139.0* 157.6±79.2**通陽利濕方組 30 266.8±76.4# 394.9±120.7* 128.1±63.0*通陽利濕方組 15 268.3±72.7# 391.2±100.2* 122.9±54.2
3.2 通陽利濕方對TNF-α、IL-1β、IL-6 水平的影響 表2顯示,模型組TNF-α、IL-1β、IL-6 水平均較假手術組顯著升高 (P <0.01)。 與模型組比較, 通陽利濕方 (60、30 g/kg) 組TNF-α、IL-1β 水平顯著降低(P<0.05),但15 g/kg 組無顯著差異(P>0.05);通陽利濕方(60 g/kg)組IL-6 水平顯著降低(P<0.05),而30、15 g/kg組雖無顯著差異(P>0.05),但也呈現降低趨勢。
表2 通陽利濕方對TNF-α、IL-1β、IL-6 水平的影響n=10)

表2 通陽利濕方對TNF-α、IL-1β、IL-6 水平的影響n=10)
注:與模型組比較,*P<0.05,**P<0.01
組別 劑量/(g·kg-1) TNF-α/(ng·mL-1) IL-1β/(ng·mL-1) IL-6/(pg·mL-1)假手術組 — 0.85±0.35** 0.17±0.02** 87.8±23.2**模型組 — 1.29±0.16 0.32±0.10 134.2±40.8腰痛寧膠囊組 0.2 1.02±0.23* 0.21±0.07** 98.8±40.1*通陽利濕方組 60 1.05±0.20* 0.22±0.05* 101.9±34.0*通陽利濕方組 30 1.06±0.28* 0.24±0.11* 108.3±30.7通陽利濕方組 15 1.25±0.15 0.25±0.11 113.9±29.8
3.3 通陽利濕方對FGF-2、MMP-2 mRNA 表達的影響 表3、圖1 顯示,模型組FGF-2、MMP-2 mRNA 表達較假手術組顯著升高(P<0.01);與模型組比較,通陽利濕方組兩者mRNA 表達顯著降低(P<0.01)。
表3 通陽利濕方對FGF-2、MMP-2 mRNA 表達的影響n=10)
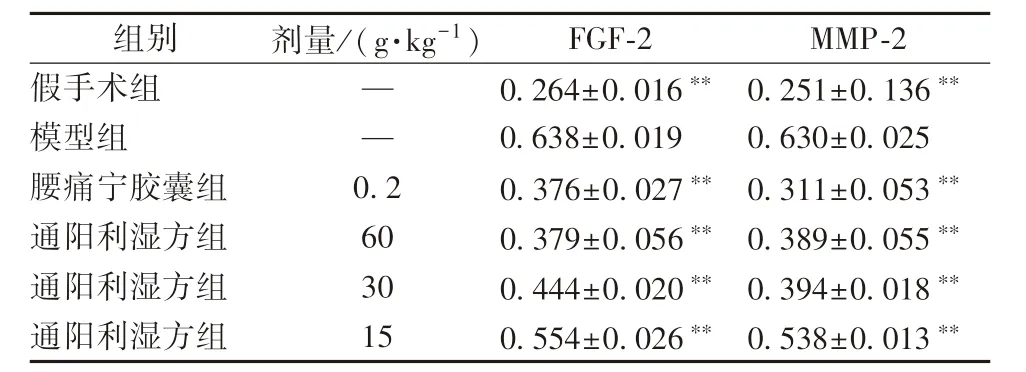
表3 通陽利濕方對FGF-2、MMP-2 mRNA 表達的影響n=10)
注:與模型組比較,**P<0.01
組別 劑量/(g·kg-1) FGF-2 MMP-2假手術組 — 0.264±0.016** 0.251±0.136**模型組 — 0.638±0.019 0.630±0.025腰痛寧膠囊組 0.2 0.376±0.027** 0.311±0.053**通陽利濕方組 60 0.379±0.056** 0.389±0.055**通陽利濕方組 30 0.444±0.020** 0.394±0.018**通陽利濕方組 15 0.554±0.026** 0.538±0.013**

圖1 各組FGF-2、MMP-2 mRNA 表達
4 討論
隨著我國進入到老齡化社會的進程,腰椎間盤突出癥已經成為臨床常見病和多發病,主要表現為反復腰痛和坐骨神經痛,對患者工作和生活影響極大。國內外文獻報道腰椎間盤突出癥在急性期時,西醫大多以20%甘露醇、甘油、果糖等進行治療,此類滲透性脫水劑靜脈滴注后能迅速提高血漿滲透壓,使組織水分向血漿轉移,產生脫水作用,該療法效果雖好,但多次輸注可引起部分患者靜脈受損,加重組織損傷,局部出現皮膚發紅、腫脹、疼痛,致血栓性靜脈炎等發生,甚至引起無菌性炎癥、壞死、潰爛,這些不良反應限制了其應用時間,而且患者耐受性差。
中醫并無腰椎間盤突出癥,該病屬“腰腿痛” “痹證”范疇,一般分為寒濕型、濕熱型、血瘀型、肝腎虧虛型等,對其大多采用活血化瘀、補益肝腎的治法,起效較慢。河北省中醫藥名老中醫趙建教授受西醫脫水劑治療腰椎間盤突出癥療效理想的啟發,通過大量臨床觀察發現急性期患者大多有濕邪留滯經絡、阻遏陽氣調達的表現,據此確立了一個新的證型——濕阻陽遏型,并提出治療法則——通陽利濕法,以融解滯澀于腰部經絡的水濕,以及水濕日久所化的瘀滯之邪,通行陽氣以四部條達,自擬通陽利濕方。方中君藥黃芪、桂枝、狗脊,補陽通脈;白芍、白術、茯苓、澤瀉為臣藥,其中白芍與桂枝合《傷寒論》 桂枝湯之意,疏解太陽經之痹,太陽融雪;茯苓、豬苓、白術、澤瀉與桂枝共用,暗合五苓散、苓桂術甘湯方義,健運脾陽使水濕得以運化,溫煦腎陽來氣化陰邪;苦杏仁、粉防己、白芍、薏苡仁亦為臣藥,意在調臟腑之氣,其中苦杏仁提壺揭蓋,宣啟肺之上源,粉防己肅泄肺之雍閉,薏苡仁淡滲中焦之濕,白芍暢肝解郁;酒軍為佐,制約黃芪、桂枝、狗脊、威靈仙之熱性;通經之藥蠶沙、桑枝、絲瓜絡、青風藤、路路通為佐,通利經絡之風寒濕之痹邪;獨活、威靈仙、懷牛膝、木瓜為使,是為引經,其中獨活善入膀肌經下部,威靈仙通行十二經, “牛膝行到膝,木瓜行到底”,引方中諸藥以達病所,以上諸藥合用,能通達四臟一腑之陽氣,利行滯澀之濕瘀,共奏通陽利濕之功。
前期課題組已證實,通陽利濕方對醋酸所致小鼠扭體反應有良好的鎮痛作用,對大鼠棉球肉芽腫也有抑制作用。本實驗采用大鼠自身尾椎髓核移植入腰椎神經根復制腰椎間盤突出癥模型,并檢測大鼠左后肢機械壓痛痛閾值,發現模型組大鼠痛閾值明顯低于假手術組,證實髓核突出可引起大鼠痛敏感反應,與文獻[4] 報道一致;給予通陽利濕方后,大鼠左后肢機械壓痛痛閾值明顯增加,表明該方對痛敏感有良好的改善作用。
關于引起腰椎間盤突出癥痛覺過敏的原因眾說紛紜,傳統觀點認為與髓核機械壓迫有關[5];也有學者研究發現,髓核引起自身免疫反應所致的神經根炎癥是引起神經根癥狀的主要原因[6];現代醫學普遍認為,椎間盤組織突出區域的細胞能合成和分泌TNF-α、IL-1β、IL-6 等多種炎性介質,均與退變程度密切相關[7],其中高水平TNF-α 可促進I 型膠原合成的增加,并逐步取代II 型膠原而進一步發展成椎間盤纖維化[8],而大量分泌的TNF-α 又通過誘導產生IL-1β、IL-6 等來加速了骨吸收,促進了破骨細胞的增殖和分化,進而引起骨量減少,骨組織結構退變,通過破壞骨質促進腰椎間盤退變[7],此外TNF-α、IL-1β 還能促進PGE2等致痛介質釋放,對神經根有直接刺激作用,并能增強其對緩激肽的敏感性,故與LDH 的疼痛密切相關[5,9];臨床研究也證實,腰椎間盤突出癥患者椎間盤組織中TNF-α、IL-1β、IL-6 表達顯著增加[10],髓核組織的炎性細胞浸潤時TNF-α 和IL-1β 大量分泌,會引起MMPs 分泌增加[11]。
炎癥反應主要通過激活蛋白激酶來引起細胞外基質內蛋白成分水解,造成細胞外基質降解,而髓核組織中細胞外基質最主要的成分為多種類型的膠原。MMP-2 能水解Ⅳ型和Ⅴ型膠原,進而造成髓核發生退行性病變[12-13],臨床研究顯示腰椎間盤突出癥患者椎間盤組織中其蛋白量明顯高于對照組,證實該疾病發生與MMP-2 水平增高,并引起細胞外基質丟失有關[14]。在椎間盤退變過程中,可代償性地引起軟骨組織增生和細胞外基質合成增加,表現為組織中FGF-2 及其受體mRNA 表達明顯增加[15]。鑒于此,本實驗主要通過分析炎癥因子水平及MMP-2、FGF-2 mRNA 表達,探究通陽利濕方改善腰椎間盤突出癥的作用機制,發現該方能明顯降低大鼠血清TNF-α、IL-1β、IL-6 水平,下調組織MMP-2、FGF-2 mRNA 表達,推測可能與抑制炎癥因子,調節細胞外基質合成有關。

