末端脫氧核酸轉移酶介導的功能核酸生物傳感器研究進展
張媛 梁嘉慧 羅云波 田晶晶 田洪濤 許文濤
(1. 河北農業大學食品科技學院,保定 071001;2. 農業部農業轉基因生物安全評價(食用)重點實驗室 中國農業大學食品科學與營養工程學院,北京 100083)
基因工程重要的特點之一是在體外實行DNA分子的切割和重新連接,因此工具酶是DNA體外操作必不可少的工具。工具酶種類繁多、功能各異,主要包括限制酶、聚合酶、連接酶、修飾酶和核酸酶5大類。獲得某種特殊的目的基因,大多需要工具酶——限制性內切酶,將目的基因和載體DNA連接到一起,也需要工具酶——DNA連接酶。這些酶具有特異性的序列識別能力以及高效的生物催化活性,在一定的條件下可以對核酸分子進行切割、連接、擴增以及修飾等,同時工具酶的反應條件溫和且具有出色的生物相容性。基于這些優勢,工具酶被廣泛地應用于核酸、蛋白質和小分子等生物活性分子的分析檢測。常用的工具酶包括:限制性核酸內切酶、甲基化酶、DNA連接酶、DNA聚合酶、末端脫氧核苷酸轉移酶、磷酸酶和磷酸激酶、單鏈核酸內切酶、核酶等。在基因工程的研究中,多傾向于將兩種或多種工具酶混合使用,充分發揮各工具酶的功能,以達到最優的應用效果,如本文所述,可以利用甲基化酶和TdT酶共同作用構建電化學傳感器、利用核酸外切酶和TdT酶構建熒光生物傳感器等。
末端脫氧核苷酸轉移酶(Terminal deoxynucleotidyl transferase,TdT)是一種催化脫氧核苷酸結合到DNA或RNA分子的3′羥基端的無需模板的DNA聚合酶[1]。1958年,Bollum等[2]從小牛胸腺中純化并稱為小牛胸腺DNA聚合酶,后來因其催化聚合時不需要模板的特點改名為末端脫氧核苷酸轉移酶。此酶大量存在于胸腺中[3],少量存在于骨髓細胞內[4],在煙草培養細胞中也含有此酶[5]。自1973年McCaffrey等[6]在急性淋巴母細胞白血病人的白細胞中發現此酶后,科學家們對此酶進行了大量的研究,發現其對生物功能有很大的影響,TdT酶在體內表達被認為僅發生于原發性淋巴組織(胸腺和骨髓)中[7-9],現已被廣泛應用于腫瘤的檢測和治療[6,10]、免疫組織化學分析[11]、作為某些白血病的診斷指標[12-13]和某些人類癌細胞的生物標志等方面[13-14]。自1958年來,科學家對末端脫氧核苷酸轉移酶的研究從未間斷,但是對于核心特征即可以不依賴于模板聚合的發生原因卻仍未探究清楚。即使如此,其獨特無模板便可擴增的特性卻使得其在核酸標記中具有很廣闊的前景,被廣泛應用于核酸生物傳感、核酸納米技術和基因芯片技術等領域中。
1 TdT酶的簡介
1.1 TdT酶的結構
DNA聚合酶的X家族是核酸轉移酶家族的亞類,TdT酶屬于DNA聚合酶的X家族,是基因結構具有高度保守性的多結構域蛋白[15-16]。1971年,Change等[17]提出了用于純化末端脫氧核苷酸轉移酶的簡化程序,通過平衡離心和凝膠電泳顯示該酶是均相的,其可被十二烷基硫酸鈉解離成α和β兩個亞基。后來Sabbioni[18]用放射性活性分析法證明它是含鋅的金屬酶,實驗時常用Mg2+作為激活嘌呤核苷三磷酸聚合的激活劑,Co2+作為嘧啶核苷三磷酸聚合的激活劑,Srivastava[19]實驗證明了Mg2+不能代替Zn2+,而Co2+可以代替Zn2+。
1.2 TdT酶的性質
TdT酶的分子量為60 kD的金屬酶,最適pH值為7.2,二價離子如Mg2+、Mn2+和Co2+等可作為其輔因子,加速酶催化反應[13,20]。核酸類似物如5-甲基-dCTP、6-O-甲基-dGTP等可作為反應的底物,三磷酸雙脫氧胸腺嘧啶和三磷酸蟲草菌素作為為反應的終止物。EDTA是非常有效的TdT酶抑制劑,只要微克分子水平的EDTA就可抑TdT酶的活性。金屬鰲合劑因除去了二價金屬離子而起到抑制作用,但它并不能改變酶的結構,也不與dNTP競爭,而與起始物競爭,阻礙了起始物和酶的結合,是一種金屬配基抑制劑。
1.3 TdT酶催化的生物反應
TdT酶可催化dNTP或標記了小分子的dNTP,如Cy3-dNTP和biotin-dNTP。聚合于RNA或單雙鏈DNA的3′-OH末端的反應,該反應無需特定模板,但引物須至少有3個以上堿基的寡核苷酸。以RNA為模板時,TdT性能嚴格依賴于受體RNA3′-末端的三級結構和核苷酸種類。一般來說,TdT對RNA模板的作用效率比DNA模板低,目前的研究也多以DNA為模板進行。TdT酶對于引物分子的具體序列無特殊要求,凡是帶有突出、凹陷或平滑的3′末端的單雙鏈DNA分子均可作為引物,其中3′突出末端摻入效率最高,而延伸產物的堿基序列則由反應池中的dNTP的成分所決定[21-22],TdT酶已廣泛用于溶液中DNA的延伸或在表面制備DNA納米結構[23-24]。
2 3′端羥基生成機制介導的TdT酶功能核酸傳感器
2.1 TdT酶和界面納米材料聯合介導的生物傳感器
隨著對核酸研究的不斷深入,核酸參與的反應不僅僅局限于液相體系,很多反應也可在固相表面進行,有使產物更容易分離等優點,如在核酸表面修飾巰基,可通過金硫鍵將核酸固定在金電極表面以進行一系列的反應,具有類似性質的界面材料如氧化石墨烯、玻碳電極和介孔二氧化硅等。
Wan等[25]基于靶標誘導的莖環探針(Stemloop probe,SLP)和表面引發的酶促聚合(Surface initiated enzymatic polymerization,SIEP)的結構轉換開發了兩種電化學DNA傳感器。首先,通過金硫鍵將5′末端巰基標記的探針(命名為5-SLP)和3′末端標記的探針(命名為3-SLP)固定在金電極表面。在傳感器的初始狀態下,兩種探針均采用莖環結構,從而避開捕獲探針未標記的末端。當探針與靶標DNA雜交時,SLP被改變為剛性雙鏈,因此5-SLP釋放了可由TdT酶催化的3′-OH末端,而3-SLP由于3′-OH末端被巰基標記,阻止了TdT酶的作用,使用信號探針與3-SLP的5′末端雜交并提供3′-OH。經過TdT酶的末端延伸反應后,通過使用天然dNTP和生物素化的2′-脫氧腺苷-5′-三磷酸(Biotinylated 2′-deoxyadenosine 5′-triphosphate,biotin-dATP)的混合物,將生物素標記到長單鏈DNA中,然后使用抗生物素蛋白-辣根過氧化物酶(Avidin-horseradish peroxidases,Av-HRPs)特異性結合生物素標記以產生電化學信號,實驗原理如圖1所示。3-SLP介導的傳感器靈敏度更高,可用來區分單個堿基錯配,可應用于疾病相關DNA、microRNA和疾病相關蛋白的檢測。
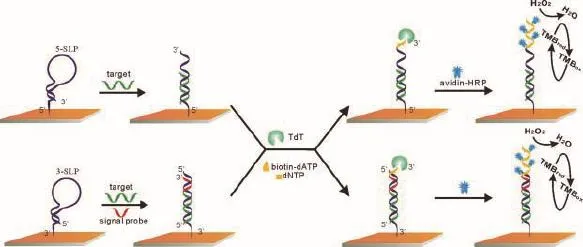
圖1 5-SLP和3-SLP介導的生物傳感器實驗原理圖[25]
2.2 TdT酶和核酸酶聯合介導的生物傳感器
由于TdT酶需在3′-OH端進行延伸,所以要利用TdT酶可以延長核酸序列這一特點構建生物傳感器時,可利用不同的工具酶對核酸進行切割以產生3′-OH。能夠將聚核苷酸鏈的磷酸二酯鍵切斷的酶,稱為核酸酶。不同來源的核酸酶,其專一性、作用方式都有所不同,根據核酸酶作用的位置不同,又可將核酸酶分為核酸外切酶和限制性內切酶,能識別特定的核苷酸順序,并從特定位點水解核酸的內切酶稱為限制性核酸內切酶。核酸外切酶Ⅰ、核酸外切酶Ⅲ、核酸外切酶Ⅶ等核酸外切酶和限制性核酸內切酶如EcoR Ⅰ、SmaⅠ、甲基化酶等都能切割核苷酸產生3′-OH端。
Wu等[24]將DNA分子探針的3′末端設計成為巰基的發夾結構,且分子探針設計成包含了能被DNA甲基化轉移酶特異性識別的特定序列,通過金硫鍵的強結合作用,將探針固定在金電極表面,避免在空氣中有3′端裸露。當DNA甲基化轉移酶存在時可將腺苷甲硫亮氨酸(SAM)上的甲基轉移到這個序列中腺嘌呤殘基上N6的位置上,形成的5′-G-Am-T-C-3′序列,該序列可被甲基化敏感的限制性內切酶Dpn I特異性識別并切割,在電極表面產生具有3′-OH末端的新探針。隨后,通過TdT酶介導的延伸將biotin-dUTP并入到新探針的3′-OH末端,再加入鏈霉親和素標記的堿性磷酸酶(streptavidinalkaline phosphatase,SA-ALP)與新探針上的標記生物素結合,ALP酶催化1-萘基磷酸酯(1-naphthyl phosphate,1-NP)水解,產生一個放大的電化學信號。在沒有DNA甲基轉移酶時,不會產生電化學信號,進而實現對DNA甲基轉移酶活性的檢測。
Ma等[26]設計了在其3′末端被磷酸化的識別探針的發夾DNA,由于DNA探針在沒有DNA甲基轉移酶(Dam MTase)時不含游離的3′-OH官能團,因此不能被TdT酶延長。在Dam MTase的存在下,它可以甲基化識別序列以產生作為DpnI底物的甲基化 DNA(5′-GmA-T-C-3′)。然后,DpnI將甲基化探針切割成含有兩個游離3′-OH末端的3個短的單鏈DNA片段,含有游離3′-OH末端的DNA片段可以被TdT酶延長。TdT酶生產的富含G的產品可以被硫代黃素T(Thioflavin T,ThT)染料迅速識別,產生高度特異性的熒光增強信號,以檢測DNA甲基轉移酶的活性。
Xu等[27]開發了一種特異而靈敏的microRNA檢測方法,設計了一種與靶miRNA完全互補的3′-磷酸化的 DNA 探針(DNA-3′-PO3),由于該探針無3′-OH的ssDNA,所以不會被雙鏈特異性核酸酶(Duplex-specific nuclease,DSN)切割及TdT酶識別。當靶標存在的情況下,DNA-3′-PO3將與miRNA雜交形成雙鏈體,可被DSN酶識別。由于DSN酶只切割DNA / RNA雙鏈體中的DNA,目標miRNA可被釋放與另一個DNA-3′-PO3探針雜交,同時,可以在目標循環反應后收集帶有3′-OH的DNA片段作為TdT酶的引物,形成的超長多T尾的2′-脫氧胸苷5′-三磷酸(dTTP)與Cu2+結合形成聚(胸腺嘧啶)銅納米粒子(poly(thymine)-hosted copper nanoparticle,poly T-CuNps),產生強烈熒光。
3 TdT酶介導的四聯體生物傳感器
3.1 C-四聯體生物傳感器
Lu等[28]使用 TdT 酶在富含胞嘧啶(Cytosine,C)的dNTP(60% dCTP,40% dTTP)庫將引物延伸成富含C的DNA序列,并且富含C的序列可以折疊成i-基序,i-基序是非規范的DNA二級結構,其由兩個平行雙鏈體通過插入的C-C+堿基對氫鍵合在一起組成。新生的富含C的寡核苷酸序列將在酸性條件下折疊成i-基序結構,然后可被具有增強發光響應的發光Ir(III)絡合物識別,產生強烈的熒光信號,原理如圖2-A所示。因此,該系統可以用作TdT酶活性測定的接通發光檢測平臺,與傳統的生物化學或免疫學測定相比,這種無標記的基于i-基序的發光接通平臺相對簡單且成本較低。
3.2 G-四聯體生物傳感器
Leung等[29]基于銥(iridium,Ir)(III)與 G-四聯體結合能夠形成增強發光響應的復合物這一性質,開發了無標記與結構無關的傳感平臺。實驗原理如圖2-B所示,在靶標不存在的情況下,適配體將在3′-5′方向上被核酸外切酶(Exonucleautomotive,ExoI)消化,被切割成很多單核苷酸。因此,TdT酶將不能使核苷酸鏈延伸產生G-四聯體序列并且由于Ir(III)配合物的背景發射弱,所以系統的發光將會很弱。但是,增加了目標誘導適體折疊成抗ExoI消化的二級結構,在由60% dGTP和40%dATP組成的dNTP庫的存在下,加入0.33 U/μL TdT酶在37℃反應1 h后即可將DNA寡核苷酸延伸成隨機的富含鳥嘌呤的序列,在加入K+離子后,DNA將被誘導成G-四聯體結構,隨后被G-四聯體選擇性Ir(III)復合物識別并具有強烈的發光響應。該傳感平臺不需要適體的特定二級結構,因此極大地簡化了DNA的設計步驟。
4 TdT酶介導的金屬納米簇生物傳感器
金屬納米簇是由幾個至幾十個原子組成的具有熒光性、水溶性的分子級聚集體。它因特有的量子尺寸效應、光穩定性強、反聚合能力強、生物相容性好等特點,被廣泛應用于生物傳感器、新型催化劑、腫瘤細胞的檢測及環境監測等領域[30-32]。
4.1 銀納米簇生物傳感器
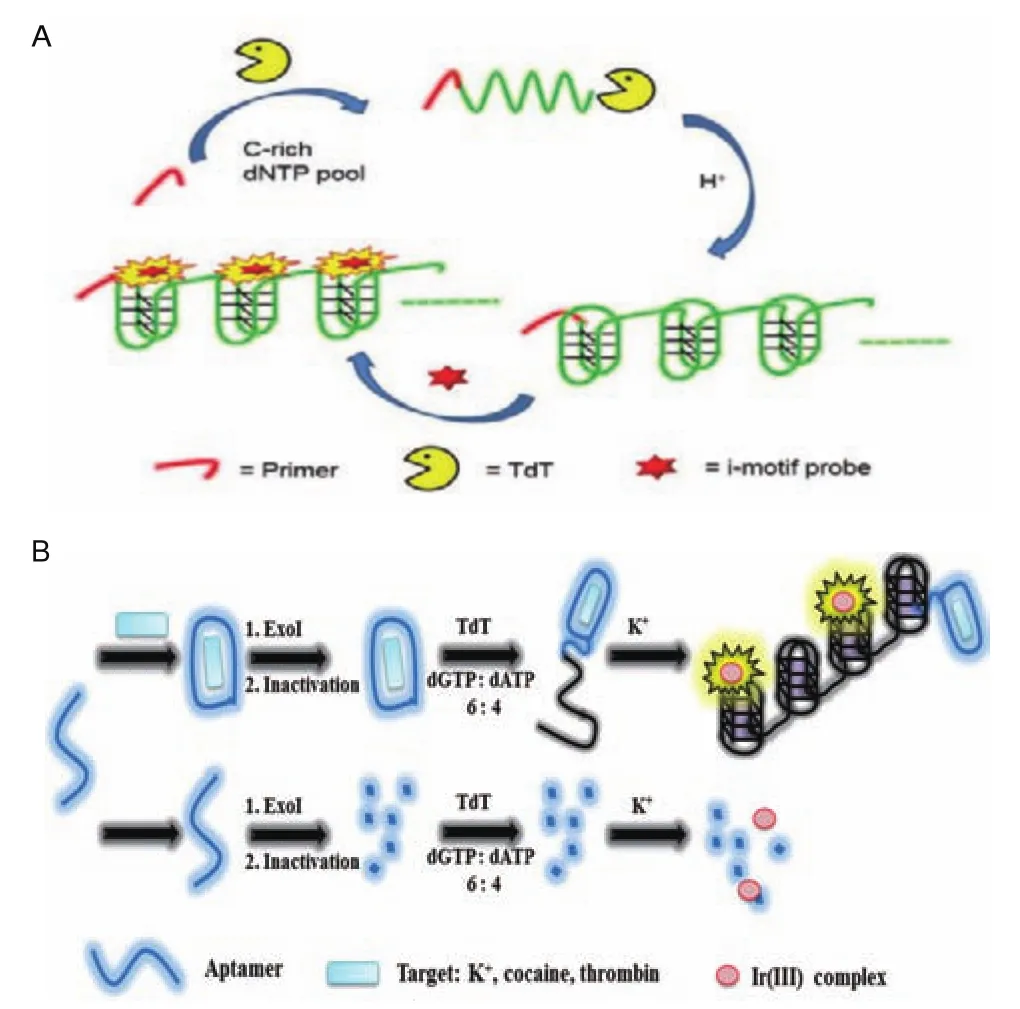
圖2 TdT酶介導的四聯體生物傳感器實驗原理圖[28-29]
Yuan等[33]利用Ag+與胞嘧啶之間的特異性相互作用強于其他3種堿基,在dCTP存在下,TdT酶催化脫氧核苷酸的重復添加以延長DNA引物的3′-OH末端,并因此產生富含胞嘧啶的長單鏈DNA模板。長鏈富含胞嘧啶的DNA可以作為寡核苷酸封裝的銀納米簇的合成模板,合成的DNA-AgNCs發出強烈的熒光(圖3-A)。根據這一性質,可構建檢測核酸酶活性的新型生物傳感系統。Hu等[34]基于氧化石墨烯(Graphene oxide,GO)支持的末端脫氧核苷酸轉移酶生成的富含胞嘧啶的DNA納米微粒模板化銀納米簇(DNA nanotailtemplated silver nanoclusters,DNA-AgNCs)的獨特電催化活性,建立了一種新型的無標記的生物傳感器。在dCTP存在下,TdT酶催化脫氧核苷酸的重復添加以延長DNA引物的3′-OH末端,并且生長的富含胞嘧啶的DNA可用于制備具有銀原子的胞嘧啶堿基的DNAAgNCs,可吸附在GO修飾的玻碳電極(GO-modified glassy carbon electrodes,GO/GCE)上,對H2O2還原具有較高的電催化活性,能夠實現良好的電化學信號輸出。該方法為TdT酶活性檢測及其相關抑制劑篩選提供了一種簡便的方法,由于其具有較高的靈敏度和優異的選擇性,因此在基于TdT酶的生物化學研究、疾病診斷和藥物發現的實際應用中具有很大的潛力。
4.2 銅納米簇生物傳感器
Zhou等[35]在引物和底物脫氧核糖核苷酸三磷酸(dNTP)存在下,TdT酶催化重復添加dNTP以延長DNA引物的3′-OH末端并因此產生長DNA序列,37℃孵育2.5 h后所得到的DNA可以用作合成熒光CuNCs的模板。因此,可以通過熒光的強度反映TdT酶的活性。實驗還得出當底物池由50% dATP和50% dTTP組成時,相應的聚合產物是用于合成熒光CuNCs的最佳模板。Zhang等[36]使用獨立于模板的DNA聚合酶-TdT酶,在單鏈DNA(ssDNA)的3′-OH末端連續添加脫氧胸苷三磷酸(deoxythymidine Triphosphate,dTTP)37℃孵育2 h即可產生長的富含T的DNA納米線,該納米線可作為模板用來形成DNA銅納米簇(DNA nanowirestemplated copper nanoclusters,DNA-CuNCs),通過非共價 π-π 堆積作用自組裝到GO-修飾的玻碳電極(GO/GCE)表面上來建立電化學測定,可以催化H2O2的還原,產生與TdT酶量成比例的強電化學信號,這種新的生物傳感策略對于進一步開發基于CuNCs的生物傳感器具有積極作用,實驗原理如圖3-B所示。。
4.3 金納米簇生物傳感器
Hu等[37]開發了一種基于TdT酶和DNA金納米 簇(Nucleic acid functionalized Au nanoparticles,DNA-AuNPs)的“樹枝狀”信號放大的無標記電化學生物傳感器,用于DNA的檢測。制備過程具有3步放大:首先,“主干”(富含T的長序列)通過引入脫氧胸腺嘧啶三磷酸(Deoxythymine triphosphate,dTTP)作為底物池來構建,這一過程需在37℃下反應1 h;其次,將由poly-A DNA功能化的AuNPs與上述“主干”雜交,30 min后可形成更多的枝放大信號;最后,使用dATP∶dGTP=4∶6的混合dNTPs通過TdT酶使AuNPs上的核酸延伸,這種隨機形成的包含豐富G的DNA序列可以通過Pb2+誘導在室溫下形成G-四聯體,三苯基甲烷染料結晶紫(Crystal violet,mCV)可與G-四聯體特異性結合實現電信號輸出,實驗原理如圖3-C所示。作者還將3步放大法與直接形成G-四聯體的一步信號放大法進行對比,這種新型無標記多步放大電化學DNA傳感器與單步放大實驗相比具有更低的檢測限。
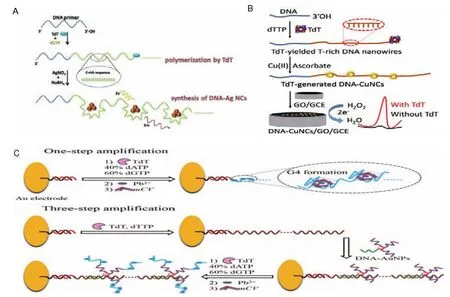
圖3 TdT酶介導的金屬納米簇實驗原理圖[33,36-37]
5 TdT酶介導的電化學生物傳感器
電化學方法可以快速的分析酶活性,基于TdT酶介導的延伸策略,可以建立簡單且高效的電化學測定法,用于敏感且無標記的DNA相關酶活性檢測。Hu和 Zhang等[33,35]證明了原位生長的 DNA 納米模板AgNCs和CuNCs可以吸附在GO修飾電極上,對H2O2還原具有較高的電催化活性,為電化學傳感器的構建提供良好的輸出信號。由于TdT酶可使dNTP延伸,吸附金屬離子產生金屬納米簇,因此可以利用以上兩種性質進行電化學生物傳感器的構建。
Wei等[38]利用了三重級聯信號放大效應設計了用于檢測 Pb2+的電化學脫氧核酶(DNA enzyme,DNAzyme)傳感器。當存在靶標Pb2+時,3′端磷酸化的DNAzyme催化DNA 序列(8-17 E)被激活,且雙巰基功能化發夾(HP)底物鏈可以被切割以暴露3′-OH,可以被TdT酶催化將生物素標記的dUTP依次添加到底物鏈的3′-OH 端。用牛血清白蛋白(Bovine serum albumin,BSA)封閉后,鏈霉親和素標記的5 μg/mL的20 μL堿性磷酸酯酶(SA-ALP)通過其與生物素的親和作用連接到電極上,ALP催化1-萘基磷酸酯(1-NP)生成電活性物質1-萘酚,產生電化學信號,實現對Pb2+的靈敏檢測,最低檢測限為0.043 nmol/L,當不存在Pb2+時,電化學響應較弱。
6 TdT酶介導的光學生物傳感器
6.1 熒光生物傳感器
Liu等[21]通過TdT酶聚合制備富含G的隨機DNA序列,并證明了這種隨機富含G的DNA能夠形成G-四聯體,通過實驗得出當dNTP池中有60%dGTP和40% dATP時G-四聯體活性最高。此外,這些G-四聯體可以結合到氯化血紅素上以形成過氧化物酶模擬脫氧核酶,并與G-四聯體特異性染料產生熒光配合物。基于以上原理Liu等研發了兩種檢測簡單且無標記的檢測TdT酶活性的策略,包括基于脫氧核糖核酸酶的比色測定法和實時熒光測定法,后者的檢測限為0.05 U。該實驗的實時檢測方法為臨床診斷中關鍵酶的生化分析提供了一種可行的方法,且操作相對傳統方法更加簡便。
6.2 可視化生物傳感器
Tian等[39]基于多重超聚合酶鏈式反應(Multiplex super polymerase chain reaction,MS-PCR) 和 不 對稱尾部雜交鏈反應(Asymmetric tailing hybridization chain reaction,AT-HCR)開發并驗證了超靈敏的比色雙重檢測病原體的方法。實驗采用20 U/L的TdT酶催化ssDNA尾部的延伸,孵育60 min后與hemin形成G-四聯體DNA核酶,表現出辣根過氧化物酶(HRP)模擬酶的活性,新形成的脫氧核酶可以通過H2O2催化ABTS2-變為綠色的ABTS·-,該方法可直接進行可視化分析,且靈敏度較高用時較短。
Miao等[40]開發了一種新的比色性DNA酶納米線傳感器,用于靈敏和選擇性定量測定脂多糖(Lipopolysaccharides,LPS),其用肉眼觀察的半定量極限可達20 ng/mL。在存在LPS的情況下,適體-引發劑(Aptamer-Initiator,AI)的一端的LPS-適體與LPS形成LPS/適體復合物,AI另一端的引發劑開始通過HCR交替打開H1和H2。此外,在HCR過程之后,TdT酶誘導的G-四聯體DNA核酶沿著帶切口的超dsDNA多聯體納米線自組裝。氯化血紅素(Hemin)作為嵌入G-四聯體結構中的配體形成辣根過氧化物酶(Horse Radish Peroxidase,HRP)模擬DNA酶,催化過氧化氫(H2O2)/ TMB產生明顯的亮黃色。在不到2 h時內,實現了比色反應,檢測到的LPS濃度可低至100 pg/mL,它也可以靈活地轉化為其他適配子識別的非核酸靶標,如離子、蛋白質、生物分子和細胞等,具有廣闊的應用前景。
Zhang等[41]開發了一種無標記、高通量的生物發光方法,通過酶介導的三環級聯信號放大來靈敏檢測尿嘧啶DNA糖基化酶(Uracil DNA Glycosylase,UDG),此法高靈敏度,檢測限低至0.000 31 U/mL。在UDG的存在下,DNA雙鏈體中的一條鏈可產生嘌呤/脫嘧啶(Apurinic/apyrimidinic,AP)位點,可被嘌呤/嘧啶核酸內切酶(Apurinic/apyrimidinic endonuclease,APE1)切割,得到帶有游離3′-OH末端的DNA片段可啟動TdT酶介導的聚合反應,在dTTPs存在下產生長的富含T的序列。再用富含A的輔助探針,通過T7 核酸外切酶(T7 Exonuclease,T7Exo)從其5′末端特異性降解以釋放大量的AMP和dAMP,在磷酸烯醇式丙酮酸(Phosphoenolpyruvate,PEP)和dCTP存在下腺苷酸激酶(Adenylate kinase,AK)和丙酮酸激酶(Pyruvate kinase,PK)酶促反應的組合將釋放的AMP轉化成ATP,并且隨后將ATP轉化成AMP產生強烈的生物發光信號。
7 TdT酶介導的表面離子共振生物傳感器
Yuan等[42]進行了基于高效表面等離子體共振(Surface plasmon resonance,SPR)的DNA檢測研究,兒茶酚紫(Catechol violet,CV)能夠聚合成寡聚物或與金屬離子螯合,實驗中CV與dsDNA-復合的銅納米簇(CuNPs @ dsDNA)結合或形成寡聚體,引起顯著的質量增加并作為提高SPR響應,通過原位合成由聚-T序列dsDNA模板化的CuNPs并與納米效應沉積協同地開發了新的SPR-DNA傳感器。首先,tDNA與探針雜交,以將TdT酶介導的DNA延伸活化到SPR芯片的表面上,從而在雙鏈DNA末端到金芯片表面形成長的poly-T序列ssDNA鏈,并通過與優化的探針雜交產生巨大的SPR響應。然后,在單鏈核苷酸鏈上同步產生的CuNPs錨定在dsDNA衍生物中,導致明顯的SPR信號擴大。最后,CuNPs@ dsDNA通過添加CV和H2O2觸發沉淀的實時轉化,以實現最終的信號放大。
8 總結與展望
目前基于TdT酶輔助的信號放大策略,構建得到了一系列簡單靈敏的功能核酸生物傳感器,其顯著的優勢在于TdT酶利用脫氧核苷酸在3′羥基末端延伸時不需要特定的模板,具有普遍適用性;其次,經TdT酶延伸形成的信號輸出產物多樣,可以實現多種模式的信號輸出,滿足不同的生物傳感器需求。更重要的是,由于TdT酶獨特的性質其介導的生物傳感器檢出限相對較低,可顯著提高檢測的靈敏度。
現今對TdT酶的生物傳感器研究仍屬于初級階段,還存在一些問題亟待解決,要想使其得到更廣泛的應用,則需對TdT酶的核心特征即可以不依賴于模板聚合的具體生物學機制進行進一步的研究,確定其空間構象結構與功能發揮的關系,便于進一步從合成生物學的角度來提升酶活及改造酶的特性。目前TdT酶介導的生物傳感器大多是對單一物質進行檢測,在今后的研究中如何利用TdT酶的性質將TdT酶介導的生物傳感器與其他類型的傳感器相結合,以實現多種靶物質的同時快速檢測,將成為未來研究的主要方向。另外,TdT酶與功能核酸聯合介導的生物傳感器的設計相對簡單,且構建方便,人們可以充分利用不同功能核酸的性質發揮功能核酸的優勢,結合TdT酶的信號放大功能,使TdT酶介導的功能核酸生物傳感器應用于更多的領域,如快速檢測領域。快速檢測即在采樣現場即刻進行分析,省去標本在實驗室檢驗時的復雜處理程序,快速得到檢驗結果的一類方法,由于其耗時短,操作簡便等優點被廣泛的應用到各種檢測領域,要想使TdT酶在快速檢測領域得到應用,則應需尋找一種方法封閉酶的活性以便于酶的貯存和運輸。

