卵泡膜細胞瘤的超聲聲像圖表現及診斷分析
王冠杰 曹云云 龔曉萍 王海飛 楊 田 孔曉曉 王亞梅 牛建梅
上海交通大學醫學院附屬國際和平婦幼保健院超聲科,上海 200230
卵巢卵泡膜細胞瘤起源于卵巢的特殊間胚葉組織,由卵泡膜細胞構成,是卵泡性索間質腫瘤中的一種,為實性腫瘤。卵泡膜細胞瘤及卵巢纖維瘤占卵巢所有腫瘤的4.1%,約占性索間質腫瘤的76.3%[1]。卵泡膜細胞瘤絕大部分是良性腫瘤,其具有雌激素分泌功能,可以產生異常的陰道出血等癥狀。卵泡膜細胞瘤缺乏特征性臨床表現,超聲診斷中卵泡膜細胞瘤易被診為其他卵巢性索間質腫瘤,如卵巢纖維瘤等及外突性子宮肌瘤和卵巢惡性腫瘤等。對超聲圖像準確的判讀有助于臨床醫生快速判斷患者病情,亦有助于減輕患者的精神壓力。本研究收集在上海交通大學醫院附屬國際和平婦幼保健院(以下簡稱“我院”)經手術病理證實為卵巢卵泡膜細胞瘤患者的相關資料,對其聲像圖表現及臨床特點進行總結,以提高對該疾病的術前診斷正確率,降低誤診及漏診率。
1 資料與方法
1.1 一般資料
選擇2015年1月~2016年10月在我院經手術病理證實為卵巢卵泡膜細胞瘤的患者47例。年齡30~77歲,中位年齡55歲,30例發生在絕經后,中位絕經年齡51歲,絕經2~27年。因月經紊亂、不規則出血、絕經后出血及下腹部墜脹或疼痛就診13例,34例因體檢時超聲檢查發現病灶就診。排除標準:①超聲提示為卵巢來源實質性占位但手術病理證實為非卵泡膜細胞瘤的患者;②超聲提示卵泡膜細胞瘤而未經手術病理證實的患者。本研究所有資料按醫院倫理委員會要求進行脫敏處理。
1.2 方法
1.2.1 超聲檢查 采用Philips公司生產的11XE、GE公司生產的730等彩色多普勒超聲儀對患者進行檢查,所有患者術前均接受腹部及陰道超聲常規檢查,所用探頭頻率分別為 3.5~5.0 MHz、7.0~9.0 MHz。
1.2.2 腫瘤指標檢測 采用羅氏公司Eppendorf Centrifuge 5804離心機以3000 r/min離心,獲得血清;采用羅氏公司COBAS6000生化免疫分析儀檢測相關腫瘤標志物。
1.3 觀察指標
記錄患者的年齡、是否絕經及絕經年齡、相關實驗室檢查資料、超聲聲像圖特點以及手術標本病理結果。實驗室檢查主要記錄術前腫瘤標志物指標。所有患者均在術前進行血清腫瘤標志物癌胚抗原(carcinoembryonic antigen,CEA)、血清糖類抗原 125(carbohydrate antigen 125,CA125)、血清糖類抗原 199(carbohydrate antigen 199,CA199)、血清糖類抗原 153(carbohydrate antigen 153,CA153)及甲胎蛋白(α-fetoprotein,AFP)的檢測。超聲檢查中行多方位、多切面及多角度掃查子宮及雙附件區,并記錄子宮與卵巢的大小、內膜的厚度及回聲情況,發現病灶記錄其發生部位、大小、形態、內部及后方回聲、邊界、周邊及內部血流信號情況,檢查并記錄有無盆腔及腹腔積液。
2 結果
2.1 一般臨床資料
卵巢卵泡膜細胞瘤患者發生年齡30~77歲,中位年齡55歲,63.8%(30/47)發生在絕經后,中位絕經年齡 51歲,其中 30~39歲占 17.0%(8/47)、>39~49歲19.1%(9/47)、>49~59 歲 27.7.0%(13/47)、>59~69 歲31.9%(15/47)、>69~79 歲 4.3%(2/47)。其中>59~69 歲比例最高,為 95.7%(45/47)。 病灶 95.7%(45/47)發生單側卵巢(左側26例,右側19例),2例發生在雙側。
術前超聲診斷病灶大小 (11 mm×9 mm×8 mm)~(98 mm×93 mm×82 mm),19例伴有盆腔積液,最大深度約39 mm;無伴腹腔積液病例。患者因月經紊亂、不規則出血,絕經后出血及下腹部墜脹或疼痛就診為13例,34例患者無明顯臨床癥狀。
患者術前血清腫瘤標志物檢測中僅1例CA125測值升高(81.64 U/mL),其余患者CA125的結果均正常。
2.2 超聲聲像圖表現
形態:88.9%(40/45)病灶形態尚規則,余形態欠規則。邊界:51.1%(23/45)病灶邊界欠清或不清(主要為側方及后方邊界),余病灶邊界尚清晰。內部回聲及后方回聲衰減情況:86.7%(39/45)病灶呈低回聲,其中20例后方回聲出現衰減,3例內見點狀強回聲;4例呈混合回聲,其中1例后方回聲伴衰減;2例呈無回聲,其中一例為多房無回聲。見圖1。彩色多普勒血流圖(color Doppler flow imaging,CDFI)情況:37.8%(17/45)病灶周邊和/或內部測及點狀或條狀血流信號,余病灶周邊及內部均未測及明顯血流信號。超聲診斷結果提示,卵巢纖維瘤、子宮漿膜下肌瘤及卵巢惡性腫瘤可能共8例,2例提示囊性占位,2例提示性索間質來源腫瘤可能,3例提示卵泡膜細胞瘤可能,余30例提示實質性占位。合并子宮肌瘤24例,子宮肌腺癥2例。
2.3 超聲診斷的準確性
因絕經后病灶較小合并多發性肌瘤而漏診2例,在多發肌瘤手術時發現,病灶發生在單側卵巢(術中測值最大直徑分別約3 cm,4 cm)。超聲對病灶的檢出率為 95.7%(45/47),定位正確率為 100.0%(45/45),誤診率為 17.8%(8/45),漏診率為 4.3%(2/47)
2.4 病理結果
36例為單純性卵巢卵泡膜細胞瘤,4例為卵巢卵泡膜細胞瘤伴鈣化,3例為卵巢卵泡膜細胞瘤伴出血壞死,1例卵巢卵泡膜纖維瘤伴局部水樣變性,2例卵巢卵泡膜細胞瘤伴黃素化,1例卵巢卵泡膜細胞瘤伴扭轉。病灶中合并子宮肌瘤24例,子宮肌腺癥2例,內膜息肉1例。
3 討論
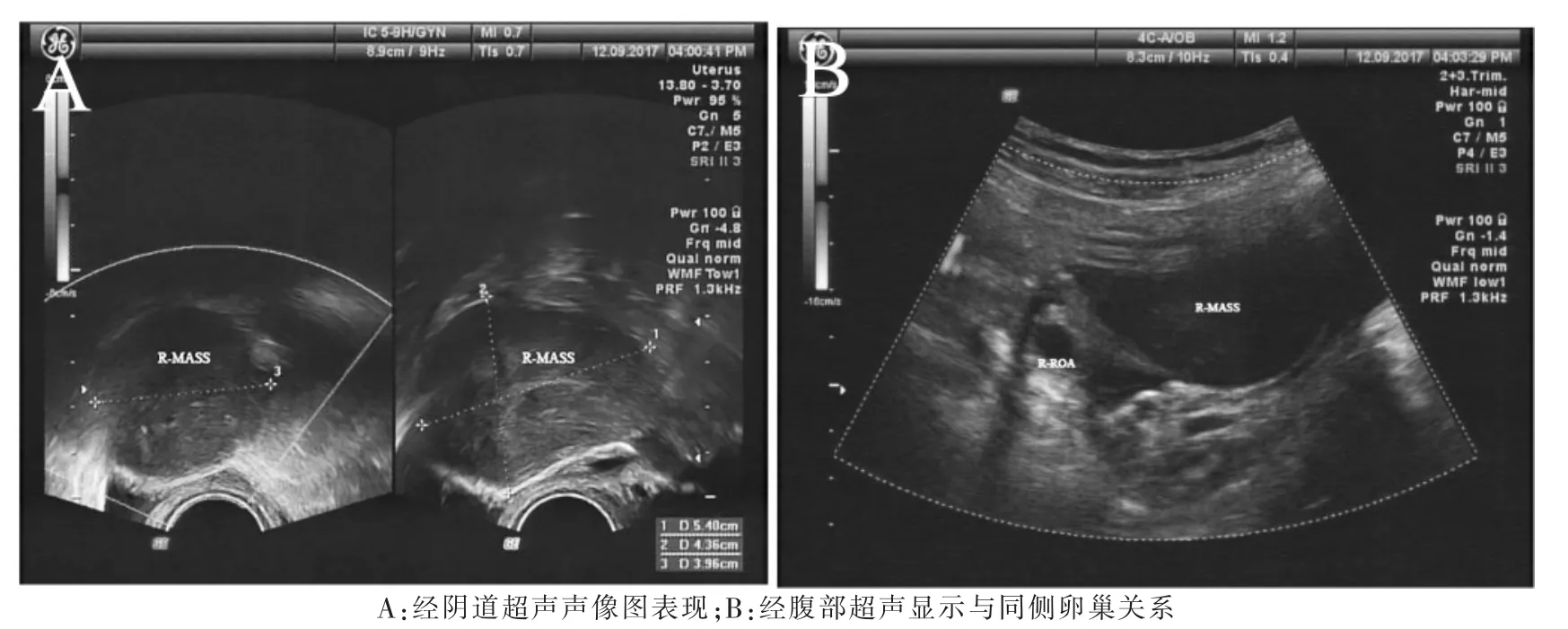
圖1 單純性卵巢卵泡膜細胞瘤超聲圖像
卵泡膜細胞瘤屬于卵巢性索間質腫瘤,為來源于儲脂的間質細胞的卵巢腫瘤,可分為典型卵泡膜細胞瘤和黃素化卵泡膜細胞瘤,主要見于40歲以上的女性,平均發病年齡為55歲,2/3以上發生在絕經后,可分泌雌激素,常伴有月經不調、乳腺增大、絕經后不規則陰道出血等癥狀,少數可出現男性化,以單側受累多見,累及雙側極少[2-3]。本組患者的病灶95.7%(45/47)發生于單側,63.8%(30/47)發生在絕經后,中位年齡55歲,其中60~69歲占比為31.9%(15/47)。有報道稱大約60%的卵泡膜細胞瘤伴有陰道流血,超過20%的卵泡膜細胞瘤伴有子宮內膜癌[4],少數患者可并發胸腹水,系由瘤蒂靜脈回流受阻所致,并且在手術切除腫瘤后治愈,被稱為Meigs綜合征[5]。本研究患者因月經紊亂、不規則出血,絕經后出血及下腹部墜脹或疼痛等癥狀而至醫院就診的占比為27.7%(13/47),余34例無明顯臨床癥狀,為常規健康體檢時超聲檢查發現病灶而就診。卵泡膜細胞瘤病理學檢查主要表現為實性腫瘤,包膜完整,質地堅硬,可合并鈣化等各種變性。影像學檢查中主要以超聲、CT以及MR為主。CT卵泡膜細胞瘤的影像學主要表現為一側附件區均質實性腫塊,界清,類圓形或橢圓形,可有淺分葉。卵巢泡膜細胞富含脂質成分,腫瘤CT值多略低于子宮。實質區多為輕度漸進性強化,少數無強化。CT對卵巢顯示欠佳,特別是對絕經女性。這限制了CT在本病診斷中的應用。MRI具有較高的軟組織分辨力,能清晰顯示腫瘤的內部結構及周圍組織的關系,并能反映組織的生物學特性。卵泡膜細胞瘤的信號改變較具特征性,與子宮肌層相比,T1WI腫瘤呈等或稍低信號。T2WI腫瘤實性部分以低信號為主,少部分成等、稍高信號,腫瘤較大時腫塊內部常可見散在小片狀、結節狀或條狀高信號。MRI檢查花費大、費時等缺點限制了其廣泛應用。超聲檢查具有耗時少、費用低、無輻射等優點,這使得其成為婦產科首選的影像學檢查。因此,分析和總結卵泡膜細胞瘤的超聲圖像特點,以提高疾病的準確率,具有較大臨床應用及經濟價值。卵泡膜細胞瘤超聲像圖特點主要為:常為類圓形或分葉狀,表面光整,可呈低回聲,后方常伴有不同程度的聲衰減,邊界尚清或欠清,內回聲可均勻或不均勻,CDFI示內部血流信號多不明顯[6]。
病灶誤診分析如下:
外突性子宮肌瘤:外突性子宮肌瘤一般包括漿膜下肌瘤、闊韌帶肌瘤及部分肌壁間肌瘤,主要向外生長形成宮外腫塊,當腫瘤較小時表現為局限性向外突出[7]。病灶內部回聲及解剖結構:卵巢卵泡膜細胞瘤的聲像圖回聲在一定程度上與子宮肌瘤回聲相似,當病灶內發生各種變性如玻璃樣變、囊性變及鈣化等,可使病灶內部回聲各異;另外病灶大多發生在絕經后,卵巢不易探查,致解剖位置不易定位,此時應仔細探查雙側卵巢,注意病灶與卵巢的關系以便進行診斷[8]。卵巢卵泡膜細胞瘤起源于卵巢,當腫瘤體積較小或雖體積較大卻活動度較大時,與子宮沒有直接接觸,與子宮外壁之間可見脂肪間隙。超聲彩色多普勒檢測:盆腔原發性腫瘤的血供一般來自于起源組織的供血動脈,尋找供血來源是判斷腫瘤組織來源的直接征象。外突性肌瘤的血供主要來由子宮動脈或其分支,常可測及血流信號進入腫塊內。卵巢卵泡膜細胞瘤的血供主要來自卵巢動脈和/或子宮動脈卵巢支,超聲測及血流信號多不明顯或測及少許點狀血流信號。結合婦科檢查:從陰道推動宮頸、宮體或從腹部推動腫塊,觀察腫塊與子宮相對移動情況來判斷腫塊來源。若腫物與子宮關系密切且同步運動,則多為子宮肌瘤;反之觸碰及腫物有浮球感并可活動,則多為卵巢來源腫塊,但當卵巢腫塊發生蒂扭轉出現出血或壞死時,與周圍組織(子宮、腸管或腹壁)發生粘連,觸之不易活動。超聲造影(contrast-enhanced ultrasound,CEUS)技術:卵泡膜細胞瘤造影劑灌注強度以稀疏,弱灌注為主,多呈周邊向中央灌注[9]。常規二維超聲很難將兩者進行鑒別,通過CEUS技術有望鑒別卵巢卵泡膜細胞瘤和漿膜下子宮肌瘤,能夠為臨床的診斷及治療提供更多信息。考慮思路:由于外突性子宮肌瘤比卵巢卵泡膜發病率高,容易首先考慮為外突性子宮肌瘤,診斷時思路應更廣一些,應在盡量排除卵巢病變的情況再下結論。
卵巢纖維瘤:卵巢纖維瘤屬于卵巢性索間質腫瘤,是來源于梭形膠原纖維細胞的卵巢腫瘤,90%患者發病在30歲以上,以50~60歲多見,累及單側為主,僅4%~8%發生于雙側,而痣樣基底細胞綜合征患者出現卵巢纖維瘤的概率較大,患者一般較年輕,常為雙側性或多灶性;卵巢纖維瘤為無分泌功能的良性腫瘤,其中約10%患者伴有腹水形成,僅1%伴有Meigs綜合征,且腹水的形成與腫瘤的大小存在一定的關系,直徑在100 mm以上的纖維瘤40%可出現腹水并伴有Meigs綜合征[10]。超聲造影:卵巢纖維瘤為乏血供腫瘤,在增強早期大多表現為絮狀低增強,增強晚期則表現為低增強[12],與卵泡膜細胞膜相似。僅從超聲上很難將兩者進行診斷,這時應結合相關臨床癥狀進行鑒別。卵巢纖維瘤與卵泡膜細胞瘤聲像圖上兩者表現極相似,不易區別,但纖維瘤發生率低于卵泡膜細胞瘤,故臨床工作中遇到此類腫瘤應先考慮后者[11-12]。
卵巢惡性腫瘤:當卵巢卵泡膜發生變性壞死或伴有胸、腹積液,且CA125指標升高時,易被誤認為惡性腫瘤;而卵巢惡性腫瘤的聲像圖表現常為外形不規則,邊界不清,內回聲不均勻,CDFI示內部血流信號較豐富,常呈低速低阻型,應結合患者其他相關臨床癥狀及實驗室檢查以助診斷。尚建紅等[13]認為不同年齡階段發生的卵巢惡性腫瘤,其病理類型及聲像學特征存在差異。青少年期以生殖細胞腫瘤為主,一般單側發病,腫瘤最大徑較大,多為實性或實性為主的混合性腫塊。生育年齡和絕經期以上皮性腫瘤為主,多為混合性腫塊。但生育年齡期卵巢腫瘤種類復雜,交界性腫瘤多,良惡性鑒別較困難;而絕經期惡性腫瘤聲像表現較典型,實性腫塊比例高,低速血流的特征更明顯[13-15]。
超聲造影:國內外一些研究[16-19]表明卵巢惡性腫瘤超聲造影表現為灌注開始早于良性腫瘤,消退晚于良性腫瘤,為實性部分快速整體不均勻高增強。增強模式惡性組多呈快進緩退表現,良性組多表現為相對緩進相對快退型。
病灶漏診分析如下:因絕經后病灶較小合并多發性肌瘤而漏診2例。檢查病灶操作時要善于選擇合適的探頭,仔細檢查卵巢內部結構可在一定程度上提高敏感性、減少漏診率,應該在時間和其他條件允許的情況下盡可能使用陰道超聲,發揮其在婦科腫瘤檢查方面的作用。
綜上所述,典型的卵巢卵泡膜聲像圖特點為低回聲,部分可伴后方回聲衰減,形態尚規則,邊界欠清或不清,CDFI示內部及周邊血流信號多不明顯,多發生于單側;易被誤診為外突性子宮肌瘤、卵巢纖維瘤及卵巢惡性腫瘤,臨床癥狀無明顯特異性。術前綜合超聲檢查及臨床相關資料可在一定程度上提高卵巢卵泡膜細胞瘤的診斷率,降低漏診及誤診率。

