左乙拉西坦與醒腦靜聯合重復經顱磁刺激治療癲癇臨床觀察
趙紅艷 鄭文權 馬建功
1)平煤神馬醫療集團總醫院神經內科,河南 平頂山 467099 2)河南大學第一附屬醫院神經外科,河南 開封 475000
癲癇為一種由于大腦神經元突發異常放電而造成的慢性短暫腦功能失調綜合征,主要癥狀為全身肌肉抽動、意識障礙,可伴精神、自主神經、感覺、運動癥狀,且具有反復發作的特點,對神經功能及生命健康造成極大損害[1-3]。藥物治療為目前臨床治療癲癇的主要方案,左乙拉西坦為新型抗癲癇藥物之一,可通過與大腦中突觸囊泡蛋白2A(SV2A)相結合、阻止海馬CA1區錐體神經元經過高電壓激活N型鈣離子通道等一系列機制發揮抗癲癇作用[4]。醒腦靜注射液為一種中藥制劑,成分主要包括梔子、冰片、麝香、郁金等,能緩解腦部炎癥反應,促進微循環,發揮腦保護的功效,最終緩解臨床癥狀[5]。同時,隨著近年來神經電生理技術不斷發展,重復經顱磁刺激逐漸被引入各種神經系統疾病治療中,研究指出,其磁信號可有效透過顱骨,對大腦神經產生良性刺激,進而改善大腦神經元的放電狀況,且具有無痛無創、不良反應少等優勢[6]。本研究選擇114例癲癇患者,隨機分為2組給予不同方案治療,旨在分析左乙拉西坦與醒腦靜注射液聯合重復經顱磁刺激的療效及對血清ICAM-1、TNF-α水平變化的影響。
1 資料與方法
1.1一般資料選取2015-09—2017-10平煤神馬醫療集團總醫院癲癇患者114例,以抽簽法分為觀察組和對照組各57例。觀察組男32例,女25例;年齡19~73(47.52±11.26)歲;病程1~14(6.92±1.67)a;發作類型:局灶性起源發作(無意識障礙)11例,局灶性起源發作(有意識障礙)20例,局灶性進展為雙側強直-陣攣10例,全面性起源16例。對照組男33例,女24例,年齡21~74(48.19±10.43)歲;病程1~15(7.45±1.81)a;發作類型:局灶性起源發作(無意識障礙)10例,局灶性起源發作(有意識障礙)24例,局灶性進展為雙側強直-陣攣8例,全面性起源15例。2組性別、年齡、疾病類型、發作類型、病程等比較差異無統計學意義(P均>0.05),且本研究經醫院倫理協會批準。
1.2納入及排除標準(1)納入標準:符合《神經病學》(第7版)中癲癇相關診斷標準,且經MRI、CT、腦電圖檢查確診[7];發作頻率≥4次/2周;年齡19~74歲;患者或其家屬知曉本研究并簽訂知情同意書。(2)排除標準:心、肝、腎等臟器功能存在嚴重障礙者;合并嚴重感染、腦血管疾病、惡性腫瘤及其他神經系統疾病者;入組前采取系統抗癲癇治療者;依從性差,無法配合完成治療者;存在重復經顱磁刺激治療禁忌證及對左乙拉西坦、醒腦靜注射液過敏者。
1.3方法對照組采取左乙拉西坦(比利時UCB Pharma S.A,批準文號:H20091019)與醒腦靜注射液(無錫濟民可信山禾藥業股份有限公司,國藥準字:Z32020564)治療,左乙拉西坦初始劑量500 mg/次,2次/d,后每2周增加1次劑量,每次增加500 mg/d,最大劑量不超過3 000 mg/d;20 mL醒腦靜注射液+250 mL生理鹽水靜滴,1次/d,持續治療4周。
觀察組采取左乙拉西坦與醒腦靜注射液聯合重復經顱磁刺激治療。應用重復經顱磁刺激治療儀(武漢依瑞德有限公司,YRDCCY-I)治療,采取重復低強度(閾值90%)與高頻經顱磁刺激,線圈直徑14 cm;運動閾值以刺激患者頭皮位置后引發其右手運動作為標準;磁刺激部位包括左右顳部、前額正中,刺激頻率設定為0.5 Hz,每次治療20 min,2次/d;左乙拉西坦、醒腦靜注射液使用方法及劑量與對照組一致,持續治療4周。
1.4血清指標測定采集受檢者清晨空腹血4 mL,離心提取血清,以酶聯免疫吸附法測定血清腫瘤壞死因子-α(TNF-α)與細胞間黏附分子-1(ICAM-1)水平,試劑盒均購于天津銳爾康生物科技有限公司,相關操作嚴格按照試劑盒說明書進行。
1.5臨床效果評價標準治療4周后患者腦電圖情況顯著改善,癲癇發作頻率下降>75%為顯效;腦電圖情況有所改善,癲癇發作頻率下降50%~75%為有效;腦電圖情況無明顯好轉,癲癇發作頻率較治療前下降<50%為無效。總有效率=(顯效+有效)/病例數×100%[8]。
1.6觀察指標(1)臨床效果;(2)治療前后認知功能狀況,以蒙特利爾認知評估量表(MoCA)進行評價,總分30分,分值越低認知功能越差[9];(3)治療前后腦電圖情況(尖波時程、尖波數量);(4)治療前后血清ICAM-1、TNF-α水平;(5)不良反應。

2 結果
2.1臨床效果觀察組治療4周后總有效率高于對照組(P<0.05)。見表1及圖1。
2.2MoCA評分2組治療前MoCA評分對比,差異無統計學意義(P>0.05),2組治療4周后MoCA評分升高,且觀察組高于對照組(P<0.05)。見表2。
2.3腦電圖情況2組治療前腦電圖尖波時程及尖波數量相比,差異無統計學意義(P>0.05),治療4周后2組腦電圖尖波時程及尖波數量降低,且觀察組低于對照組(P<0.05)。見表3。

表1 2組臨床效果比較 [n(%)]

圖1 2組臨床效果比較

組別n治療前治療4周后t值P值觀察組5719 21±1 5925 64±2 1917 9380 000對照組5718 87±1 4023 27±2 0513 3820 000t值1 2125 965P值0 2280 000
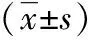
表3 2組腦電圖情況比較
2.4血清ICAM-1、TNF-α水平2組治療前血清ICAM-1、TNF-α水平相比,差異無統計學意義(P>0.05),治療4周后2組血清ICAM-1、TNF-α水平降低,且觀察組低于對照組(P<0.05)。見表4。
2.5不良反應觀察組不良反應發生率與對照組對比差異無統計學意義(P>0.05)。見表5及圖2。
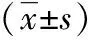
表4 2組血清ICAM-1、TNF-α水平對比

表5 2組不良反應發生率對比 [n(%)]

圖2 2組不良反應對比
3 討論
癲癇發病機制尚不明確,可能與神經膠質細胞增生、神經遞質失衡、離子通道異常、免疫功能紊亂、氧化應激損傷等多種因素有關,長期癲癇發作可造成患者中樞神經系統神經元發生病理性改變,損害其認知功能,嚴重威脅其生命健康和生活質量[10-11]。流行病學調查顯示,我國癲癇的總體發病率約7.0‰,活動性癲癇發病率(1 a中有發作)約4.6‰,且有逐步升高趨勢[12]。尋找安全、有效治療方案成為臨床關注焦點。
目前,藥物治療為臨床治療該病的首選方案,左乙拉西坦屬新型抗癲癇藥物之一,其與大腦中SV2A親和力較強,同其結合后,能有效阻止神經元異常放電;可阻止海馬CA1區錐體神經元通過高電壓激活N型鈣離子通道,進而緩解癲癇癥狀;能解除負性變構劑對于甘氨酸能神經元及γ-氨基丁酸(GABA)能神經元的抑制,間接強化中樞抑制作用;可降低大腦皮質中GABA受體含量,并將其滯留在海馬中,進而增強GABA對神經元回路抑制作用,最終發揮抗癲癇效果[13]。有關研究指出,左乙拉西坦可明顯改善患者認知功能,促進患者病情轉歸,且安全性較高[14]。醒腦靜注射液屬一種中藥制劑,主要成分包括梔子、郁金、冰片、麝香等,可有效清除自由基,減少腦脊液中的內源性致熱原,減輕腦水腫,抑制因缺血再灌注造成的腦神經細胞衰亡,進而緩解腦部炎癥反應,改善腦循環,起到腦保護作用,有效緩解患者臨床癥狀[15-16]。
隨神經電生理技術不斷進步,重復經顱磁刺激逐漸用于治療癲癇中,其可通過流經線圈高強度電流形成一個磁場,由該磁場透過顱骨于腦組織中引發電流,實現深部腦刺激,有效調節神經細胞電活動,控制其抑制或興奮的平衡,進而促使異常放電神經細胞恢復到正常狀態,發揮治療癲癇的作用[17-18]。其還具有操作簡單、創傷小、價格低、安全性高等特點[19]。本研究顯示,治療4周后觀察組總有效率、MoCA評分高于對照組,腦電圖尖波時程及尖波數量低于對照組,說明采取該方案治療可有效提高臨床效果,改善患者腦電圖及認知功能狀況。
近年來,有研究顯示,炎癥反應及免疫功能異常在癲癇發生、發展中起重要作用,而TNF-α為一種重要炎性細胞因子,可促使B、T及單核巨噬細胞活化,促進白細胞介素-6、白細胞介素-2等其他炎性細胞因子表達,并加速抗原提呈細胞分泌人白細胞Ⅱ類抗原,從而參與癲癇發生、進展[20]。ICAM-1為一種免疫球蛋白,可通過與其受體相結合,促使內皮細胞骨架重組,加速血管內皮細胞與白細胞黏附,引發級聯反應,致使白細胞骨架重排及白細胞活化,促進炎癥發生、進展,進而造成神經細胞損傷,引發腦細胞水腫,致使患者病情進一步惡化[21]。本研究顯示,治療4周后觀察組血清ICAM-1、TNF-α水平低于對照組,表明左乙拉西坦與醒腦靜注射液聯合重復經顱磁刺激可降低血清ICAM-1、TNF-α水平,緩解機體炎癥反應,從側面證實其治療有效性。本研究中,2組不良反應較接近,提示該治療方案安全性較高。本研究所選樣本量少,結果有無代表性,仍需臨床多渠道和多中心選擇樣本以擴大樣本量進一步觀察。
[1]HECK C N,KINGSTEPHENS D,MASSEY A D,et al.Two-year seizure reduction in adults with medically intractable partial onset epilepsy treated with responsive neurostimulation:Final results of the RNS System Pivotal trial[J].Epilepsia,2014,55(3):432-441.
[2]MARTIN H C,KIM G E,PAGNAMENTA A T,et al.Clinical whole-genome sequencing in severe early-onset epilepsy reveals new genes and improves molecular diagnosis[J].Hum Mol Genet,2014,23(12):3 200-3 211.
[3]趙新春,邢效如,臺立穩.拉莫三嗪對癲癇患者療效和安全性及生活質量影響研究[J].現代預防醫學,2015,42(14):2 663-2 665.
[4]黃立華,沈碧峰.左乙拉西坦對癲癇患者血清瘦素及hs-CRP水平的影響[J].中國生化藥物雜志,2017,37(4):232-234.
[5]王麗,唐冬云,阮玉泉.醒腦靜輔助卡馬西平治療腦卒中后繼發性癲癇的臨床療效及安全性評價[J].醫學綜述,2015,21(17):3 243-3 245.
[6]楊霄鵬,楊顏滋,楊瑞玲.重復經顱磁刺激治療癲癇的臨床療效及安全性分析[J].中國實用神經疾病雜志,2016,19(12):85-86.
[7]賈建平,陳生弟.神經病學[M].7版.北京:人民衛生出版社,2013:297.
[8]盧軍,曾其昌,王琴,等.奧卡西平與左乙拉西坦治療新診癲癇的療效[J].神經損傷與功能重建,2016,11(2):125-127.
[9]皮鳳蘭,胡化俠,張渺,等.不同抗癲癇藥物對新診斷癲癇患者認知功能的影響[J].精神醫學雜志,2016,29(4):299-301.
[10]CARDAMONE M,FLANAGAN D,MOWAT D,et al.Mammalian target of rapamycin inhibitors for intractable epilepsy and subependymal giant cell astrocytomas in tuberous sclerosis complex[J].J Pediatr,2014,164(5):1 195-1 200.
[11]梅晶,李惠允.癲癇患者認知功能障礙及其影響因素相關性分析[J].疑難病雜志,2016,15(5):445-448.
[12]李昌敏,孫丹,楊梅,等.1例燙傷患者術后癲癇持續狀態的短篇病例報道[J].重慶醫學,2016,45(32):4 603-4 604.
[13]金超.左乙拉西坦對癲癇兒童認知功能的影響研究[J].中國婦幼保健,2014,29(13):2 121-2 123.
[14]胡淑麗.醒腦靜靜脈注射聯合左乙拉西坦治療癲癇患者的療效觀察及對甲狀腺功能的影響[J].國際醫藥衛生導報,2016,22(9):1 288-1 290.
[15]劉燦.醒腦靜注射液對癲癇持續狀態患者的療效及對血清神經元特異性烯醇化酶的影響[J].中國實用神經疾病雜志,2016,19(9):49-51.
[16]莫林林.醒腦靜注射液輔助治療外傷性癲癇的臨床效果[J].醫學理論與實踐,2015,28(4):425-426.
[17]周平,鄧燕,胡鈞濤,等.重復經顱磁刺激治療顱腦外傷性癲癇患兒的療效及對血清IGF-1和NSE水平的影響[J].現代中西醫結合雜志,2017,26(5):510-512.
[18]田繼剛.應用經顱磁刺激治療癲癇的臨床療效及安全性分析[J].中國社區醫師,2016,32(31):59-60.
[19]王迎紅,周正.重復經顱磁刺激對腦性癱瘓并發癲癇患兒運動功能的影響[J].中國康復理論與實踐,2016,22(1):98-102.
[20]袁婕,宋江莉,張虹,等.奧卡西平治療對癲癇患者血清炎性因子、細胞間粘附分子1及免疫功能的影響[J].海南醫學院學報,2017,23(11):1 571-1 574.
[21]郭留芹.醒腦靜注射液聯合奧卡西平對癲癇患者T淋巴細胞亞群及血清ALP、ICAM-I水平變化影響[J].中國實用神經疾病雜志,2017,20(12):88-90.

