右美托咪定在肝臟腫瘤切除患者肝臟缺血再灌注損傷中的作用
陳貴珍,魯開智,文欣榮
(第三軍醫(yī)大學(xué)西南醫(yī)院麻醉科,重慶 400038)
?
·經(jīng)驗(yàn)交流·
右美托咪定在肝臟腫瘤切除患者肝臟缺血再灌注損傷中的作用
陳貴珍,魯開智,文欣榮
(第三軍醫(yī)大學(xué)西南醫(yī)院麻醉科,重慶 400038)
目的 觀察右美托咪定在腹腔鏡下肝臟腫瘤切除患者肝臟缺血再灌注損傷中的作用。方法 將40例ASA Ⅰ~Ⅱ級(jí)擬在腹腔鏡下行肝臟腫瘤切除術(shù)患者,分為右美托咪定組(D組)和對(duì)照組(C組)。D組:將右美托咪定稀釋為4 μg/mL,麻醉誘導(dǎo)后,予右美托咪定1 μg/kg負(fù)荷劑量泵注,10 min輸注結(jié)束,之后再改為0.4 μg/(kg·h)進(jìn)行維持,直到肝門阻斷前。C組:注入等容量生理鹽水。分別于麻醉前(T1)、最后一次肝門開放即刻(T2)、再灌注后1 h(T3)、6 h(T4)、24 h(T5)、48 h(T6)記錄其血流動(dòng)力學(xué)情況,并抽取靜脈血行天門冬氨酸氨基轉(zhuǎn)移酶(AST)、丙氨酸氨基轉(zhuǎn)移酶(ALT)、總膽紅素(TBIL)測(cè)定。結(jié)果 兩組患者術(shù)中各時(shí)間點(diǎn)的血流動(dòng)力學(xué)情況差異無統(tǒng)計(jì)學(xué)意義。與T1相比,D組與C組T2~T6時(shí)的ALT、AST活性均明顯增強(qiáng)(P<0.05),T4~T6時(shí)的TBIL活性明顯增強(qiáng);與C組相比,T2~T6時(shí)D組的ALT和AST活性及T4~T6時(shí)TBIL活性明顯降低(P<0.05)。結(jié)論 右美托咪定能減輕肝臟缺血再灌注損傷,對(duì)腫瘤切除患者的肝功能有保護(hù)作用。
右美托咪定;肝門阻斷;肝臟缺血再灌注損傷
手術(shù)切除是目前治療肝臟腫瘤的首選方法和最有效的措施。隨著微創(chuàng)技術(shù)的發(fā)展,在腹腔鏡下行肝臟腫瘤切除的技術(shù)也日漸成熟。但肝臟缺血再灌注損傷(hepatic ischemia reperfusion injury,HIRI)是肝臟外科手術(shù)常遇到的問題[1]。在術(shù)中采用何種藥物或方法來防止或減輕HIRI有重要意義。目前研究提示,氧化應(yīng)激和炎性反應(yīng)對(duì)HIRI起重要作用。右美托咪定(dexmedetomidine,Dex)是一種新型高選擇性α2腎上腺素受體激動(dòng)劑,除鎮(zhèn)靜催眠作用外,還表現(xiàn)出抗炎和重要臟器缺血再灌注損傷的保護(hù)作用[2-3]。已有基礎(chǔ)研究表明[4],右美托咪定對(duì)肝臟的缺血再灌注損傷有保護(hù)作用。本研究旨在研究右美托咪定在臨床中對(duì)肝臟腫瘤切除患者肝臟缺血再灌注損傷中的保護(hù)作用。
1 資料與方法
1.1 一般資料 選擇ASA Ⅰ~Ⅱ級(jí),年齡18~65歲,肝功能Child-Pugh分級(jí)Ⅰ~Ⅱ級(jí),經(jīng)腹腔鏡肝門阻斷下行肝臟腫瘤切除術(shù)的患者40例,分為Dex組(D組)和對(duì)照組(C組),每組20例。
1.2 麻醉與治療方法 患者入室后,常規(guī)監(jiān)測(cè)生命體征[心率(HR)、無創(chuàng)血壓(NIBP)、血氧飽和度(SpO2)],建立靜脈通道。全身麻醉誘導(dǎo):咪達(dá)唑侖0.03 mg/kg,舒芬太尼0.4 μg/kg,依托咪酯0.3 mg/kg,順式阿曲庫(kù)銨0.15 mg/kg。麻醉誘導(dǎo)后行右頸內(nèi)靜脈、左橈動(dòng)脈穿刺置管,實(shí)時(shí)監(jiān)測(cè)血流動(dòng)力學(xué)。D組:將Dex稀釋為4 μg/mL,麻醉誘導(dǎo)后,予Dex 1 μg/kg負(fù)荷劑量泵注,10 min輸注結(jié)束,之后再改為0.4 μg/(kg·h)進(jìn)行維持,直到肝門阻斷前。C組:注入等容量生理鹽水。麻醉維持:七氟醚(0.6~1.3 MAC)+瑞芬太尼(3~4 ng/mL),Nacrotrend麻醉深度數(shù)值維持在64~37,按需追加肌松劑順式阿曲庫(kù)銨。
1.3 標(biāo)本的采集和測(cè)定指標(biāo) 分別于麻醉前(T1)、最后一次肝門開放即刻(T2)、再灌注后1 h(T3)、6 h(T4)、24 h(T5)、48 h(T6)抽取靜脈血3 mL送本院檢驗(yàn)科行天門冬氨酸氨基轉(zhuǎn)移酶(AST)、丙氨酸氨基轉(zhuǎn)移酶(ALT)、總膽紅素(TBIL)測(cè)定。
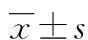
2 結(jié) 果
2.1 兩組患者一般情況等比較 兩組患者一般情況、術(shù)中出血量、肝門阻斷時(shí)間、手術(shù)時(shí)間的差異均無統(tǒng)計(jì)學(xué)意義。兩組患者在各時(shí)間點(diǎn)的平均動(dòng)脈壓(MAP)、HR、中心靜脈壓(CVP)差異無統(tǒng)計(jì)學(xué)意義,見表1。

表1 兩組患者術(shù)中血流動(dòng)力學(xué)指標(biāo)的比較

表2 兩組患者不同時(shí)間點(diǎn)各項(xiàng)指標(biāo)的比較
*:P<0.05,與T1時(shí)比較,;#:P<0.05,與C組比較。
2.2 兩組患者的血漿ALT、AST、TBIL變化T1時(shí),D組與C組的ALT、AST、TBIL活性差異無統(tǒng)計(jì)學(xué)意義。與T1相比,T2~T6時(shí)兩組的ALT、AST活性均明顯增強(qiáng)(P<0.05),T4~T6的TBIL活性明顯增強(qiáng)(P<0.05);與C組相比,T2~T6時(shí)D組的ALT和AST及T4~T6的TBIL活性明顯降低(P<0.05),見表2。
3 討 論
手術(shù)切除是目前治療原發(fā)性肝癌的首選方法和最有效的措施。研究表明,術(shù)中大量出血是造成肝切除術(shù)后病死率和并發(fā)癥增高以及肝癌患者術(shù)后生存率降低的重要獨(dú)立因素[5]。有效控制肝切除術(shù)中出血對(duì)提高肝癌患者的治療效果有顯著意義。隨著外科微創(chuàng)技術(shù)的不斷發(fā)展和外科醫(yī)生技術(shù)的提高,經(jīng)腹腔鏡行肝臟腫瘤切除術(shù)已日漸成熟。由于其切口小,目前仍主要應(yīng)用肝門阻斷的方法來控制出血[6]。而繼發(fā)于肝門阻斷的肝臟缺血再灌注損傷(HIRI)是圍術(shù)期常遇到的問題[7],臨床上主要表現(xiàn)為氨基轉(zhuǎn)移酶和總膽紅素的增高。本試驗(yàn)中,兩組患者在T2~T6時(shí)間點(diǎn)的ALT、AST、TBIL的血漿濃度均升高。現(xiàn)認(rèn)為,HIRI的發(fā)生主要是通過鈣離子超載、氧化應(yīng)激、Kuffer細(xì)胞釋放炎性細(xì)胞因子等引起,其中氧化應(yīng)激與炎性反應(yīng)在HIRI過程中起著非常重要的作用[8-9]。因此,清除(或減少)氧自由基及相關(guān)炎癥因子可減輕肝臟缺血再灌注后的肝功能損傷。
Dex是一種新型高選擇性α2腎上腺素受體激動(dòng)劑,可全面作用于α2A、α2B、α2C3個(gè)亞型,具有鎮(zhèn)靜、抗焦慮、鎮(zhèn)痛和抗交感反射等藥理學(xué)作用。已有研究證實(shí)了Dex在動(dòng)物體內(nèi)的抗炎效應(yīng)[10]。臨床報(bào)道Dex可減少上肢缺血再灌注循環(huán)中過氧化指標(biāo)丙二醛和次黃嘌呤[11],對(duì)抗缺血再灌注損傷。動(dòng)物研究還證實(shí)Dex有器官保護(hù)作用[12-14]。已有研究[15]發(fā)現(xiàn)Dex可減輕大鼠的肝臟缺血再灌注損傷,并對(duì)遠(yuǎn)端器官有保護(hù)作用。
本研究發(fā)現(xiàn),D組在缺血再灌注后各時(shí)間點(diǎn)(T2~T6)的ALT、AST活性及T4~T6的TBIL活性較C組均明顯降低(P<0.05),這表明Dex能減輕經(jīng)腹腔鏡肝臟腫瘤切除術(shù)中肝門阻斷引起的肝臟缺血再灌注損傷,對(duì)腫瘤切除術(shù)患者的肝功能有保護(hù)作用。
雖然本研究發(fā)現(xiàn),臨床中Dex在肝臟腫瘤切除術(shù)患者肝臟缺血再灌注損傷中有保護(hù)作用,但其具體機(jī)制及對(duì)其他器官功能的是否有保護(hù)作用尚需進(jìn)一步探討。
[1]TeohNC.Hepaticischemiareperfusioninjury:Contemporaryperspectivesonpathogenicmechanismsandbasisforhepatoprotection-thegood,badanddeadly[J].JGastroenterolHepatol,2011,26(Suppl1):180-187.
[2]TaniguchiT,KidaniY,KanakuraH,etal.Effectsofdexmedetomidineonmortalityrateandinflammatoryresponsestoendotoxin-inducedshockinrats[J].CritCareMed,2004,32(6):1322-1326.
[3]KocogluH,OzturkH,OzturkH,etal.Effectofdexmedetomidineonischemia-reperfusioninjuryinratkidney:ahistopathologicstudy[J].RenFail,2009,31(1):70-74.
[4]SahinT,Bege?Z,ToprakHI,etal.Theeffectsofdexmedetomidineonliverischemia-reperfusioninjuryinrats[J].JSurgRes,2013,183(1):385-390.
[5]HellingTS,BlondeauB,WittekBJ.Perioperativefactorsandoutcomeassociatedwithmassivebloodlossduringmajorliverresections[J].HPB(Oxford),2004,6(3):181-185.
[6]晏益核,盧榜裕,蔡小勇,等.肝門血流阻斷在腹腔鏡肝切除術(shù)的應(yīng)用[J].中國(guó)普外基礎(chǔ)與臨床雜志,2012,19(7):704-708.
[7]KluneJR,TsungA.Molecularbiologyofliverischemia/reperfusioninjury:establishedmechanismsandrecentadvancements[J].SurgClinNorthAm,2010,90(4):665-677.
[8]千年松,帝振宇,陶開山.肝臟缺血再灌注損傷的發(fā)生機(jī)制研究進(jìn)展[J].現(xiàn)代腫瘤醫(yī)學(xué),2009,17(8):1589-1592.
[9]Abu-AmaraM,YangSY,TapuriaN,etal.Liverischemia/reperfusioninjury:processesininflammatorynetworks-areview[J].LiverTranspl,2010,16(9):1016-1032.
[10]SezerA,MemisD,UstaU,etal.Theeffectofdexmedetomidineonliverhistopathologyinaratsepsismodel:anexperimentalpilotstudy[J].UlusTravmaAcilCerrahiDerg,2010,16(2):108-112.
[11]YagmurdurH,OzcanN,DokumaciF,etal.Dexmedetomidinereducestheischemia-reperfusioninjurymarkersduringupperextremitysurgerywithtourniquet[J].JHandSurgAm,2008,33(6):941-947.
[12]GuJ,SunP,ZhaoH,etal.Dexmedetomidineprovidesrenoprotectionagainstischemia-reperfusioninjuryinmice[J].CritCare,2011,15(3):R153.
[13]GuJ,ChenJ,XiaP,etal.Dexmedetomidineattenuatesremotelunginjuryinducedbyrenalischemia-reperfusioninmice[J].ActaAnaesthesiolScand,2011,55(10):1272-1278.
[14]YoshitomiO,ChoS,HaraT,etal.Directprotectiveeffectsofdexmedetomidineagainstmyocardialischemia-reperfusioninjuryinanesthetizedpigs[J].Shock,2012,38(1):92-97.
[15]AdnanT,OrhanT,IbrahimA,etal.Theprotectiveeffectsofdexmedetomidineontheliverandremoteorgansagainsthepaticischemiareperfusioninjuryinrats[J].IntJSurg,2013,11(1):96-100.
10.3969/j.issn.1671-8348.2016.31.035
陳貴珍(1984-),碩士,主治醫(yī)師,主要從事疼痛方面的研究。
R735.7
B
1671-8348(2016)31-4420-03
2016-03-24
2016-05-08)

