Minitab軟件在藥品生產質量控制中的應用
王春濤 唐靜 陳偉
(重慶科瑞制藥(集團)有限公司,重慶 400060)
Minitab軟件在藥品生產質量控制中的應用
王春濤 唐靜 陳偉
(重慶科瑞制藥(集團)有限公司,重慶 400060)
目的:探討藥品生產過程的質量控制方法。方法:以甲硝唑芬布芬膠囊為例,收集膠囊充填時的裝量數據,運用M initab軟件制作質量控制圖,監控制造過程,評價過程能力。結果:及時發現了看似穩定的生產過程中的異常,裝量均在內控標準范圍內,但已呈現不良趨勢,且過程能力指數值較低(CPK=0.78);進行在線改進后,過程標準差顯著降低(P<0.05),過程能力值增加(CPK=0.90);持續改進后,過程能力指數明顯提高(CPK=1.12)。結論:基于M initab的質量控制圖及過程能力分析是提高藥品生產穩定性、保證藥品質量的較好方法。
M initab軟件;質量控制圖;過程能力指數;藥品生產質量管理
藥品是用于預防、診斷、治療疾病的特殊商品,其質量直接關系到人們的身體健康甚至生命安全。目前制藥行業對藥品生產質量的管控方法非常有限,缺少對藥品制造過程的質量穩定性進行保證的有效手段,藥品制造企業實施的藥品生產質量管理規范(GMP)只提出了基本要求,并未指出達到這些要求的合適辦法,沒有提供相關數據支持和在數據分析的基礎上解決問題的方法[1]。相反,有些行業已實施了對產品制造過程進行有效控制的比較成熟的質量管理方法,如全面質量管理、統計過程控制、六西格碼管理等,取得了顯著成效[2]。因此,應借鑒其他行業的經驗,并結合藥品生產的特點進行質量改進。本研究從膠囊劑藥品的生產線質量控制入手,運用M initab軟件制作質量控制圖,監控制造過程,評價過程能力,對藥品生產過程的穩定性進行分析和評價。
1 M initab軟件與質量管理
M initab軟件于1972年誕生于美國賓夕法尼亞大學統計系,進入20世紀90年代,伴隨著全球六西格瑪管理浪潮的興起而飛速發展,在工商業領域的質量管理工作中發揮重要作用,現已成為六西格碼管理實施的通用語言。
質量控制圖由美國ShewhartWA博士在1924年首次提出[2]。他認為,各種質量特性值的波動可分為偶然波動和異常波動,偶然波動在生產中一直會存在,是不可避免的,異常波動是外界原因引起的,需重點關注。應用質量控制圖能及時發現異常波動,排除產生異常波動的原因,達到只存在偶然波動沒有異常波動的狀態,即為穩態。過程處于穩定狀態時產品質量才能更好地受控。質量控制圖是統計假設檢驗的一種圖上作業,假設質量特性值在穩態下按正態分布,其分布排列是隨機的。控制圖按照±3σ確定控制界限,質量特性值數據點落在控制限之外的概率為0.27%。根據假設檢驗的小概率原則,一旦有界限之外的數據點出現,就可判斷為異常。考慮到假設檢驗的兩類錯誤,對控制界限內的數據關注其排列變化,若呈現異常傾向時,提示過程可能發生變化,應追查原因、采取對策。鐵健司著作中提出“質量管理始于控制圖,終于控制圖”[3],說明控制圖在質量管理工作中的重要性。
M initab軟件可以方便快捷地制作質量控制圖,對數據自動分析,及時發現過程中的異常,實現對制造過程的有效監控。
2 方法與結果
以膠囊充填時的1項關鍵質量指標“裝量”為例,收集數據,應用質量控制圖進行分析和判斷。
2.1 數據采集
在人員、機器、物料、方法、環境、檢測等條件固定情況下,收集甲硝唑芬布芬膠囊(規格:甲硝唑 0.1 g、芬布芬 75 mg,批號:511010)的充填裝量數據,每10 m in 1次,每次8個樣本為1組。
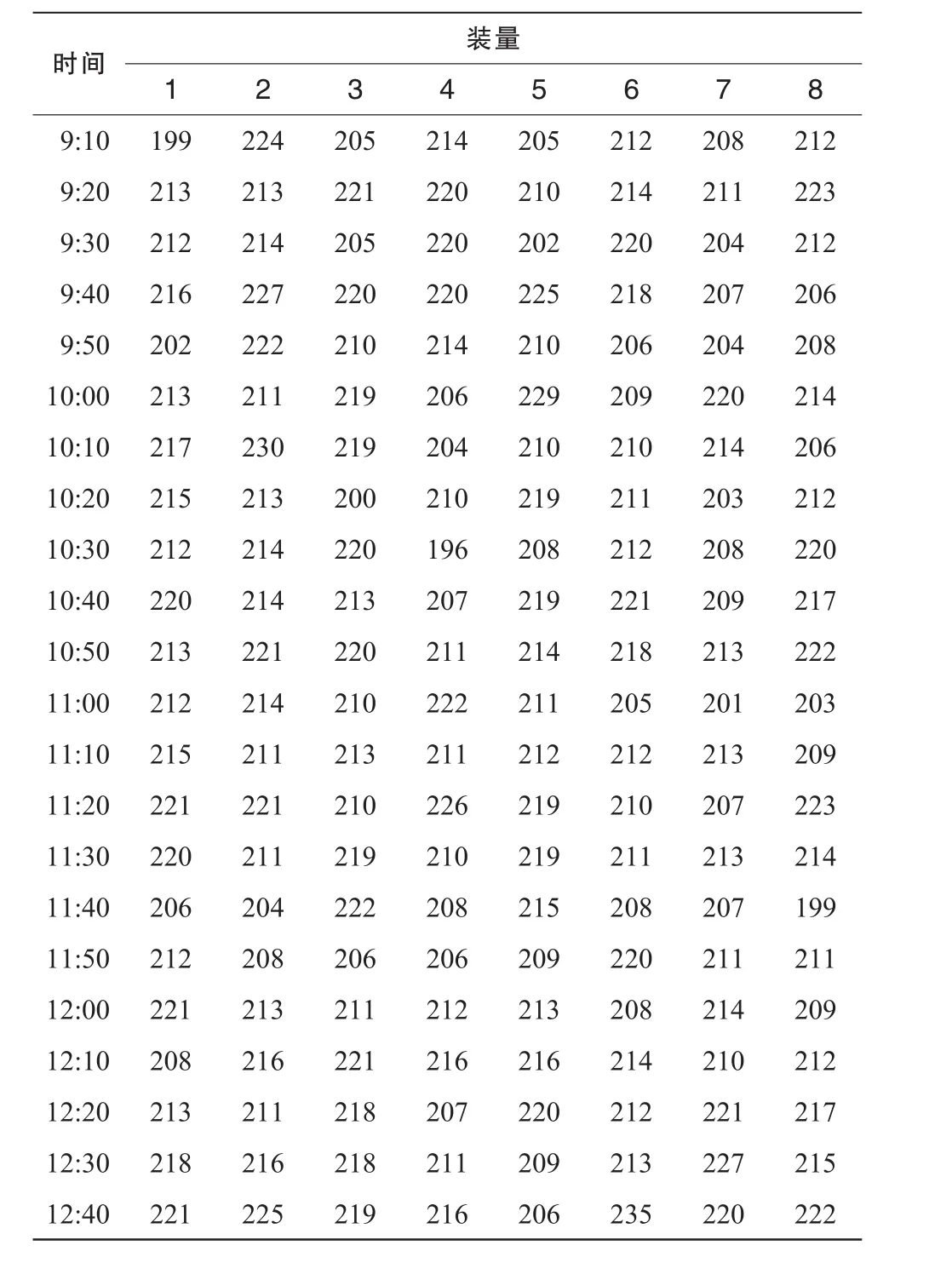
表1 甲硝唑芬布芬膠囊裝量 (mg)
2.2 判斷標準
用M initab軟件制作的質量控制圖,遵守依照統計理論小概率事件原理制定的判異標準[4]:①超出界限;②連續9點落在中心線同一側;③連續6點遞增或遞減;④連續14點上下交錯;⑤連續3點中有2個點距離中心線(同側)大于2個標準差;⑥連續5點中有4個點距離中心線(同側)大于1個標準差;⑦連續15點在距離中心線(任意一側)1個標準差之內;⑧連續8點距離中心線(任一側)大于1個標準差。
同時,運用M initab軟件還能及時對加工過程的穩定性進行評判。CPK是考慮到過程均值與目標值的偏移時的過程能力指數 (Process Capability Index,CP),表示產品滿足規格的能力,傳統統計控制理論根據其大小一般將加工分為 5級[5]:①CPK≥1.67,工序能力過剩;②1.33< CPK<1.67,對精密加工而言工序能力適宜,對一般加工工序能力富裕,可維持現狀;③1<CPK≤1.33,表明對一般加工工序能力尚可,但有缺點發生;④0.67<CPK≤1,工序能力不足;⑤CPK≤0.67,工序能力嚴重不足,不合格品率高,需采取緊急措施。
2.3 制圖
打開M initab軟件,將數據輸入,電腦制圖,見圖1。
M initab軟件制圖自動判斷異常,顯示結果見圖2,同時進行過程能力分析,見圖3。
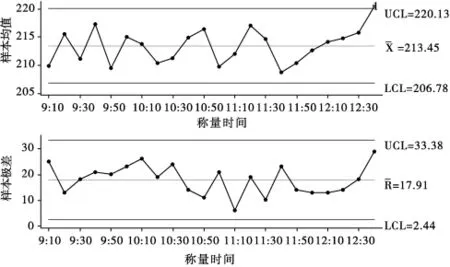
圖1 甲硝唑芬布芬膠囊充填裝量質量控制圖

圖2 Minitab軟件顯示結果
2.4 結果分析
用M initab軟件制作的質量控制圖及過程能力分析結果顯示,雖然裝量均在內控標準范圍內,但已呈現不良趨勢:第22點(12:40采集的數據)違反了規則①和規則③(見圖2),且過程能力指數值較低(CPK=0.78)。在線監控的質量控制圖提出了警告,需要及時查找原因,避免造成更大的損失。
2.5 在線改進
停機查找原因,結果發現充填桿螺絲松動,計量盤不平,壓力上升,藥粉壓實,裝量偏高。重新調整設備,糾正偏差,繼續監控。在線改進后的質量控制圖(圖4)按照2.2標準判斷已無異常。在線改進前后的過程性能對比分析見圖5。
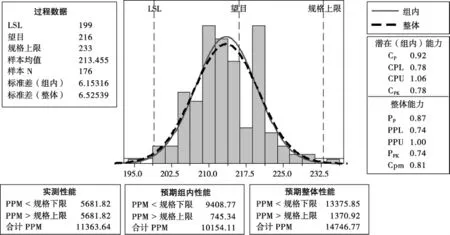
圖3 甲硝唑芬布芬膠囊過程能力分析
運用M initab軟件對改進前后進行對比分析,結果顯示,改進后的過程標準差顯著降低(P<0.05),過程能力值增加(CPK=0.90)。在生產過程中通過計算機軟件監控,及時發現了問題,及時改進,取得明顯效果。
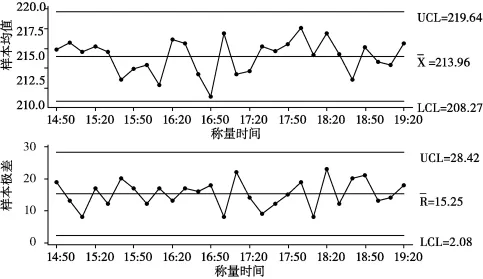
圖4 改進后甲硝唑芬布芬膠囊充填裝量質量控制圖
2.6 持續改進
對于這批產品(批號:511010),雖然在線監控發現問題,通過檢修設備取得效果,但過程能力仍不能令人滿意。于是,生產、質量部門相關人員組成質量控制(QC)小組,改進原輔料處理和配料方法,全面檢修機器設備,更換已磨損的模具,并加強了對生產操作人員的培訓。1個半月后,再次對本產品(批號:522002)進行在線監控,持續改進產品質量,結果見圖6。
結果顯示,全面改進后,甲硝唑芬布芬膠囊生產過程能力明顯提高 (CPK值達到 1.12)。運用M initab軟件能及時發現加工過程的不足,有利于產品質量的持續改進。
2.7 評價
2.7.1 甲硝唑芬布芬膠囊為我公司生產多年的產品,車間自認為工藝成熟,多年來市場也無質量事故,成品檢驗結果均合格。但從統計分析看來,生產過程并不是很穩定,511010批改進前 CPK值為0.78,改進后為0.90,工序能力不足出乎意料,即使后來的批次經過系統改進,CPK值仍只能達到1.12,并非理想狀態,生產穩定性比想象的要差。分析可知,膠囊劑藥品的生產過程影響因素較多,原來看似穩定的過程實際上均有一些異常存在,證明工序能力尚不充足,需進行改善。
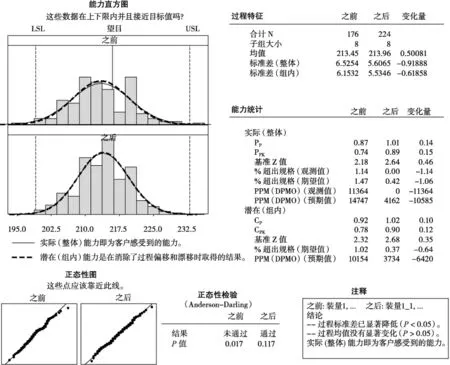
圖5 改進前后甲硝唑芬布芬膠囊過程能力對比分析
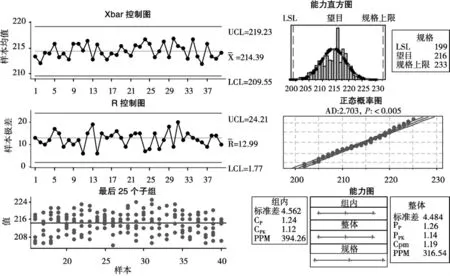
圖6 甲硝唑芬布芬膠囊(522002)過程能力分析六合一圖
同時,本研究也證明了僅靠產品的最終檢驗是遠遠不夠的,產品檢驗合格并不代表質量優異,只有對全過程進行監控管理才能真正地保證產品質量。2.7.2過程能力的欠缺還體現在期望加工目標上,統計結果顯示,過程均值與目標值之間存在顯著差異(P<0.05),也正因過程的欠穩才導致質量不能很好地受控,更證明了過程穩定的重要。
3 結論
3.1 統計過程控制的質量控制圖能更及時準確地發現問題,彌補了制藥行業GMP常規管理的不足
運用基于M initab的質量控制圖具有明顯的優點:①以數據說話,量化、科學、準確;②真正實現在線監控,通過計算機管理,自動分析、自動判斷,不用復雜的計算,不必等到后期處理,能及時發現異常,避免了階段生產結束后才發現問題而造成大量浪費,減少了對常規檢驗的依賴[6];③M initab軟件全球通用,使用范圍廣,制圖規范,界面統一,便于溝通,便于比較;④立即評價出過程能力,判斷過程穩定狀態,為改進提供依據。
3.2 藥品質量控制的及時和準確對用藥安全有重要意義
制造過程不穩會使產品質量波動較大,不利于醫生的準確用藥,藥效無法保證,對于一些特殊的臨界用藥,甚至可能危及生命。僅以本文膠囊劑藥品的裝量控制來說,同樣屬于檢驗合格的藥品,最大裝量與最小裝量相差將近17%,對用藥安全的影響特別是藥效的發揮將會產生的作用可想而知。通過實施定量分析糾正了以往僅憑最終檢驗及印象自以為生產過程穩定的看法,認清了實際情況,更科學合理,也看到了行業之間的差距。同時通過對發現的問題及時糾正而獲得一定的效果,驗證了藥品的制造過程還大有潛力可挖。運用基于M initab軟件的質量控制圖為代表的統計過程控制方法加強藥品生產的穩定性,是制藥行業提升質量管理水平的較好途徑。
[1]張梅.藥品生產企業借鑒TQM完善GMP研究[D].北京:北京交通大學,2007:16-18.
[2]馬逢時,周暐,劉傳冰.六西格碼管理統計指南[M].北京:中國人民大學出版社,2011:368-399.
[3]鐵健司.質量管理統計方法[M].韓福榮,顧力剛,譯.北京:機械工業出版社,2010:112-141.
[4]Gitlowa HS,Oppenheim AJ,Oppenheim R,等.質量管理[M].張杰,譯.北京:機械工業出版社,2008:95-111.
[5]賈新章,李京苑.統計過程控制與評價——CPK、SPC和PPM技術[M].北京:電子工業出版社,2004:37-39.
[6]張貽昌,趙建東,曹正國.統計過程控制在藥品生產質量管理中的重要性[J].中國藥業,2010,19(8):5.
The Application of M initab Software in the Quality Control of Pharmaceutical Production
Wang Chuntao,Tang Jing,ChenWei(Chongqing KeruiPharmaceutical(Group)Co.,Ltd.,Chongqing 400060,China)
Objective:To investigate the quality controlmethods in the pharmaceutical production process.M ethods: Takingmetronidazole fenbufen capsules as an example,the filling quantity data was collected,the quality control chart made by the M initab softwarewas used tomonitor themanufacturing process,evaluate the process capability and analyze the process stability.Results:The abnormality in the processwhich seemed stable was found timely.The filling quantity was in the range of the internal control standards,but adverse trend had presented w ith a low value of process capability index(CPK=0.78).A fter the online improvementwasmade,the process standard deviation significantly reduced(P<0.05)and the process capability value increased (CPK=0.90).A fter the further improvement,process capability index obviously increased (CPK=1.12).Conclusion:The application of M initab software in the analysis of quality control chart and the process capability proved as a suitablemethod to improve the stability of the pharmaceuticalproduction and ensure the drug quality.
M initab Software;Quality Control Chart;Process Capability Index;Quality Managementof Pharmaceutical Production
10.3969/j.issn.1672-5433.2012.11.012
2012-03-06)
王春濤,男,高級工程師。研究方向:藥品質量管理。通訊作者E-mail:271409783@qq.com

