2型糖尿病患者預防骨質疏松所需維生素D水平的研究*
黃征宇 羅雅娟
新余鋼鐵集團有限公司中心醫院 1 代謝內分泌科 2 急診科,江西省新余市 338000
2型糖尿病(T2DM)是一種代謝性疾病,以血糖水平異常升高為特征,可引起多飲、多食、多尿等癥狀,若血糖長時間控制欠佳,還可引起血管、神經等損害,增加相關并發癥風險,降低患者生活質量[1]。骨質疏松屬于代謝性骨病,以骨量丟失、骨脆性增加、骨微組織結構破壞為特征,早期癥狀不明顯,隨著病情的不斷加重,易合并骨折,加重患者身心負擔[2]。而T2DM發生骨質疏松的風險遠高于正常群體,一旦合并骨質疏松后則可進一步增加患者痛苦,影響身心健康。因此,如何防治T2DM患者骨質疏松的發生成為臨床研究的熱點。目前關于T2DM患者體內維生素D的水平變化及與骨質疏松發生的具體關系仍需進一步明確。鑒于此,本研究分析T2DM患者預防骨質疏松所需維生素D水平。現報道如下。
1 資料與方法
1.1 一般資料 選取2020年8月—2022年8月我院收治的50例T2DM患者作為觀察組,另選同期健康體檢者40例作為對照組。經醫學倫理委員會批準。觀察組男26例,女24例;年齡45~65歲,平均年齡(53.65±4.37)歲;體質量指數19~28kg/m2,平均體質量指數(24.36±1.49)kg/m2;病程3~12年,平均病程(6.15±1.25)年。對照組男22例,女18例;年齡45~65歲,平均年齡(54.02±4.42)歲;體質量指數19~28kg/m2,平均體質量指數(24.41±1.53)kg/m2。兩組一般資料相比,差異無統計學意義(P>0.05)。
1.2 選擇標準 納入標準:T2DM符合《中國2型糖尿病防治指南(2020年版)》[3]中診斷;健康體檢者一切正常;精神狀態良好;研究對象及家屬知情同意。排除標準:近3個月使用過鈣劑,使用過糖皮質激素等影響骨代謝藥物;肝腎衰竭;存在嚴重系統性疾病;伴有惡性腫瘤;合并急性糖尿病并發癥。
1.3 方法 所有研究對象均于清晨采集5ml空腹血,以3 000r/min速度離心處理10min,獲得血清后開展檢測。維生素D:選用美國AB SCIEX公司生產的4500MD型高效液相色譜—串聯質譜儀檢測,將適量血清標本加蛋白沉淀劑、內標,之后震蕩混勻處理,再增加萃取溶劑,震蕩后,吸取上清液,以氮氣吹干,定容至100μl,上機檢測,確定25羥基維生素D[25-(OH)D]水平。總Ⅰ型膠原氨基端延長肽(TP1NP):使用電化學發光法測定血清內TP1NP水平,儀器為全自動生化分析儀。所有操作均嚴格按照試劑盒說明及實驗室要求開展,確保獲得的數據真實有效。并依據T2DM患者是否合并骨質疏松分為骨質疏松組及未骨質疏松組,收集兩組基礎資料。
1.4 觀察指標 (1)比較兩組25-(OH)D、TP1NP水平差異。(2)比較骨質疏松及未骨質疏松T2DM患者血清25-(OH)D、TP1NP水平差異。(3)繪制ROC曲線,分析25-(OH)D、TP1NP預測T2DM患者預測骨質疏松的臨床價值。(4)采用Spearman相關性分析25-(OH)D與TP1NP相關性。

2 結果
2.1 血清25-(OH)D、TP1NP水平 觀察組25-(OH)D水平低于對照組,TP1NP高于對照組,差異有統計學意義(P<0.05)。見表1。
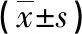
表1 觀察組和對照組血清25-(OH)D、TP1NP水平對比
2.2 合并與未合并骨質疏松患者血清指標變化 50例T2DM患者中19例合并骨質疏松;骨質疏松組25-(OH)D水平低于未骨質疏松組,TP1NP水平高于未骨質疏松組,差異有統計學意義(P<0.05)。見表2。
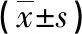
表2 合并與未合并骨質疏松患者血清指標變化對比
2.3 預測骨質疏松發生的價值 繪制ROC曲線分析顯示,25-(OH)D、TP1NP預測骨質疏松發生的曲線下面積分別為:0.902、0.842。見表3、圖1。

圖1 25-(OH)D、TP1NP預測骨質疏松發生的ROC曲線分析

表3 預測骨質疏松發生的價值
2.4 25-(OH)D與TP1NP相關性分析 25-(OH)D水平與TP1NP呈負相關(r=-0.356,P<0.05)。
3 討論
骨質疏松是危害人類身心健康的重要疾病之一,其病因復雜,可涉及年齡、骨代謝異常、內分泌紊亂等多個方面。正常情況下,隨著年齡的不斷增長,人體內性激素水平會逐漸下降,這種生理性變化會對破骨細胞造成刺激,促使其活性增強,還可抑制成骨細胞活性,導致骨量減少[4-6]。同時,在機體衰老的過程中,會降低對于營養物質的吸收能力,使得體內骨形成的相關物質合成減少,亦可降低骨量及骨質,增加骨質疏松風險。而T2DM亦是引起骨質疏松的高危因素,在高血糖的持續刺激下,可引起體內鈣磷代謝異常,使骨質出現脫鈣現象,此時機體會通過降低骨密度來補充血鈣、血磷,以糾正鈣磷代謝,而高糖刺激下促使葡萄糖及其代謝產物出現非酶促糖基化反應,會破壞成骨與破骨細胞間的活性,增加骨質疏松風險[7-8]。T2DM合并骨質疏松后病情則更為復雜,不僅需時刻警惕控糖不佳帶來的并發癥風險,還要擔心骨折隨時發生,導致患者生活質量大幅下降。因此,做好T2DM患者骨質疏松的防治尤為重要。
維生素D是一種脂溶性維生素,與骨質疏松存在密切關系。正常情況下,體內的維生素D可分為外源性及內源性兩大類,其中外源性主要攝取自食物內;內源性則源于真皮層的7-α脫氫膽固醇,在紫外線照射下可轉化為膽鈣化醇;之后經肝臟內25α羥化酶、腎臟內1α羥化酶催化后,形成25-(OH)D和1,25(OH)D,又以25-(OH)D半衰期最長,成為維生素D在人體存在的主要形式,故通過檢測25-(OH)D水平能夠良好評估維生素D狀況。維生素D在骨吸收形成中具有雙向調節作用,維生素D缺乏,會出現典型的骨吸收增加、骨形成減少表現,降低骨礦化,增加骨質疏松發病風險。同時,維生素D水平偏低可反饋性刺激甲狀旁腺激素釋放,抑制成骨細胞功能,進一步增強骨吸收能力,使得骨質疏松發病風險升高[9-11]。而維生素D的水平會受到年齡、胃腸道消化、日照減少等多種因素影響,其水平低下會增加骨質疏松風險,故將維生素D作為骨質疏松防治的參考具有重要意義。TP1NP是一種能夠反映成骨細胞活性的重要指標,能夠體現成骨細胞合成骨膠原的速度,通過監測其變化可了解成骨細胞代謝活力,掌握患者骨形成代謝狀態;正常情況下TP1NP水平異常升高則提示骨質疏松或維生素D缺乏。本研究結果顯示,觀察組25-(OH)D水平低于對照組,TP1NP高于對照組;骨質疏松組25-(OH)D水平低于未骨質疏松組,TP1NP水平高于未骨質疏松組;繪制ROC曲線分析顯示,25-(OH)D、TP1NP預測骨質疏松發生的曲線下面積分別為:0.902、0.842;25-(OH)D水平與TP1NP呈負相關(r=-0.356,P<0.05)。提示T2DM患者體內維生素D水平處于缺乏狀態,且其水平越低骨質疏松風險越高。分析原因為,相較于健康人群,T2DM患者更易出現維生素D缺乏現象,考慮原因在于高血糖狀態下會引起腎臟損傷,使得腎臟途徑的25-(OH)D生成減少,且維生素D水平過低會影響胰島素的分泌,加重T2DM病情,形成惡性循環,使機體維生素D水平持續下降,故T2DM患者更易伴有骨質疏松。臨床需動態監測維生素D水平的變化,及時開展針對性干預措施,降低骨質疏松發生風險。
綜上所述,T2DM患者易合并維生素D缺乏狀態,且維生素D水平能良好預測骨質疏松發生,可以最佳截斷值32.89nmol/L作為參考,做好骨質疏松的防治。

