常規超聲和超聲造影在犬脾臟超聲消融效果評估中的價值
蔡潔璇,孫夢迪,劉 偉,謝浩銘,張旭鑾,萬紹兵,戴靈苓,李河諭,石達友,4,陳義洲,4
(1. 華南農業大學獸醫學院,廣東 廣州 510642 ; 2. 深圳市普羅醫學股份有限公司,廣東 深圳 518000 ;3. 深圳邁瑞動物醫療科技股份有限公司,廣東 深圳 518110 ; 4. 廣東省獸醫臨床重大疾病綜合防控重點實驗室,廣東 廣州 510642)
高強度聚焦超聲(High intensity focused ultrasound,HIFU)消融是唯一一種無創性熱消融技術[1],國內從1997年開始將其應用于臨床治療[2]。HIFU治療具有無創、無出血、疼痛低和恢復快的優點,目前已廣泛應用于人類子宮、肝臟、胰腺、腎臟和前列腺等器官的實體腫瘤以及骨腫瘤的治療[3]。近年來,HIFU也開始用于動物軟組織肉瘤、肝細胞癌和骨肉瘤等的治療[4-7]。人醫在消融治療過程中,常用增強核磁共振成像(Nuclear magnetic resonance imaging,MRI)、增強計算機斷層掃描(Computed tomography,CT)和超聲造影(Contrast-enhanced ultrasound)等方法對HIFU的治療效果進行評估。消融后可用常規超聲(Ultrasound)進行臨床復診檢查[3],以監測病灶消融后的變化。在獸醫臨床上,由于MRI和CT的普及度較超聲低,更常用超聲對HIFU的消融效果進行評估。與MRI和CT相比,超聲具有無輻射、不需麻醉、費用低、操作簡單和可實時監測的優點,但其對消融病灶的顯示能力相對較差。超聲造影在人醫臨床上常用于對肝臟和脾臟等實質器官腫瘤的診斷,有時也用于HIFU的消融效果評估,相對于常規超聲,超聲造影能更清楚的顯示腫瘤病灶和消融灶邊界[8]。目前,關于常規超聲和超聲造影對小動物超聲消融效果的評估研究較少,為進一步比較常規超聲和超聲造影對HIFU消融效果的評估價值,本試驗對實驗犬的脾臟進行HIFU消融后,分別用常規超聲和超聲造影對消融病灶進行檢查,評估2種方法對消融病灶的檢查效果,為今后HIFU治療提供高效、快捷、準確、經濟的評估方法和參考依據。
1 材料與方法
1.1 主要試劑和儀器 Sonovue造影劑,博萊科信誼藥業;Phygene實驗動物脫毛劑,福州飛凈生物科技有限公司。20G留置針,昆山永岳醫療科技有限公司;一次性無菌三通閥,臺州銘安康醫療器械有限公司;PRO VET200獸用聚焦超聲腫瘤治療系統,深圳普羅醫學股份有限公司;Vetus E7獸用便攜式彩色多普勒超聲系統,深圳邁瑞動物醫療科技有限公司。
1.2 實驗動物 6只成年未絕育中華田園犬,雌性4只,雄性2只,平均體重為11.5 kg,正常免疫和驅蟲。消融前對實驗犬進行血常規、血生化和凝血功能等檢查,確定實驗犬處于健康狀態。試驗期間飼喂商品化犬糧,進行常規飼養管理。
1.3 試驗方法 在實驗犬頭靜脈安置20G留置針并連接三通閥,用丙泊酚分別對6只實驗犬進行誘導麻醉,異氟烷維持麻醉。實驗犬仰臥保定,腹部大范圍剃毛后,使用Phygene脫毛劑脫毛、酒精脫脂、真空脫氣完成備皮處理。用常規超聲對脾臟進行全面掃查,在脾尾最厚的部位進行HUFI消融,消融功率為350 W,消融時間為0.1 s,每次消融間隔時間為0.1 s,每個周期消融10次,按照從點到面、從面到體的順序進行。每只實驗犬消融總時間均為30 min,消融深度距離腹壁2~3 cm。消融過程中用常規超聲進行實時監測,當消融完成后,將超聲調到造影模式,顯示常規超聲和超聲造影雙實時同步模式,調節常規超聲總增益為80%,超聲造影總增益為50%,機械指數(Mechanical index,MI)值為0.06。儀器調節完成后立刻用5 mL 生理鹽水配置Sonovue造影劑,配置過程中用力振搖20 s以形成微泡混懸液。按0.5 mL/只的劑量,經留置針注入Sonovue造影劑,再快速推注5 mL生理鹽水。注射造影劑的過程用超聲對消融灶進行實時監測,并保存造影過程的超聲視頻。造影過程中完整掃查脾臟消融灶,評估消融灶的大小、回聲和邊界。在造影雙實時模式下,測量功能支持常規超聲和超聲造影畫面同步,可同步測量消融灶相同位置在常規超聲和超聲造影下的左右徑。為了比較2種檢查方法對消融灶的測量效果,消融灶左右徑采取隨機取樣的方式。消融結束后,分別在消融后即刻(第0天)和消融后第3、7、14、21、28天重復采用常規超聲和超聲造影方法檢查消融灶的變化情況,為了探究消融灶最大上下徑在不同時期的動態變化,超聲探頭在脾臟的長軸方向完整掃查消融灶后,測量消融灶在2種檢查方法中的最大上下徑。保存圖片和測量數據,進行分析。

2 結果
2.1 2種方法檢測HIFU消融后不同時期消融灶影像變化的比較 HIFU消融后即刻(第0天)和第3、7、14、21、28天的常規超聲和超聲造影觀察結果如圖1所示,在常規超聲模式下,消融灶表現為同時存在高回聲、等回聲和低回聲影像,是一種混合回聲結構,周圍未消融的脾臟呈中等回聲,消融灶與正常組織的邊界較模糊,隨著時間的推移,消融灶中的高回聲逐漸變成中低回聲,消融灶邊界區域表現為低回聲;在超聲造影模式下,消融灶表現為邊界清楚的均一低回聲區域,周圍未消融的脾臟表現為增強顯影的高回聲,消融后第3天開始,消融灶的范圍逐漸變小,但回聲影像無變化。
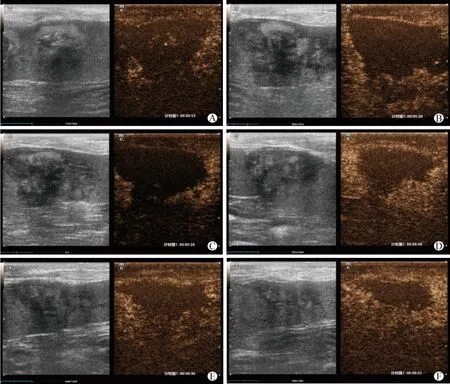
圖1 不同時期HIFU消融灶的常規超聲和超聲造影雙實時同步模式影像比較Fig.1 Comparison of dual real-time synchronous mode images of HIFU ablation focus zones at different time points using conventional ultrasound and contrast-enhanced ultrasoundA:第0天; B:第3天; C:第7天; D:第14天; E:第21天; F:第28天 mt:常規超聲,mc:超聲造影A: Day 0; B: Day 3; C: Day 7; D: Day 14; E: Day 21; F: Day 28mt: Conventional ultrasound; mc: Contrast-enhanced ultrasound
2.2 2種方法檢測HIFU消融后不同時期消融灶左右徑的比較 在HIFU消融后即刻(第0天)和第3、7、14、21、28天進行常規超聲和超聲造影檢查,在雙實時同步模式下測量相同位置消融灶的左右徑,結果如表1所示,超聲造影測量消融后即刻左右徑中位數1.29(1.02,2.12)cm和消融后第3天中位數1.17(0.91,1.52)cm,明顯大于常規超聲測量所得中位數0.91(0.59,1.83)cm和1.09(0.86,1.40)cm,差異有統計學意義(P<0.05),而在消融后第7、14、21、28天測量的左右徑比較中,兩者無統計學差異(P>0.05)。
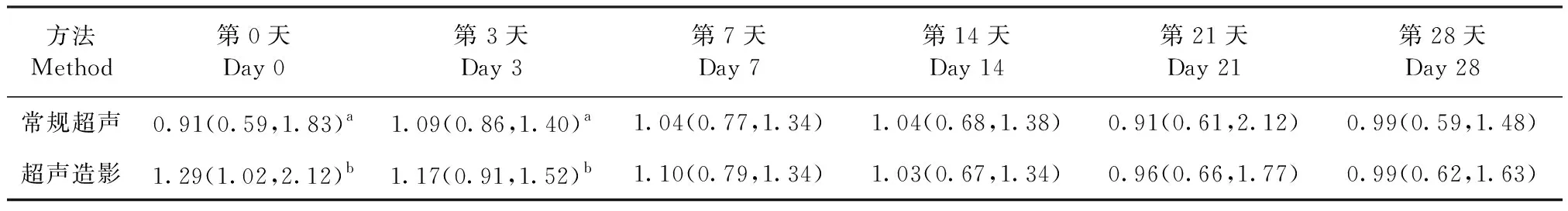
表1 不同時期常規超聲和超聲造影對消融灶左右徑的測量結果Table 1 Measurements of ablation zone left-right diameter by conventional ultrasound and contrast-enhanced ultrasound at different time points [cm,M(P25,P75),n=24]
2.3 2種方法檢測HIFU消融后不同時期消融灶最大上下徑的比較 在HIFU消融后不同時期對消融灶最大上下徑測量的結果如表2所示,2種檢查方法消融后第3天測得的結果均明顯大于消融后即刻(第0天)(P<0.05);消融后第7天測得的消融灶最大上下徑與消融后即刻(第0天)相比無明顯區別(P>0.05)。消融后第14、21和28天,在超聲造影檢查中測得的消融灶最大上下徑與消融后即刻(第0天)相比明顯減小(P<0.05),且呈持續減小的趨勢;而常規超聲檢查中測得的消融灶最大上下徑均比消融后即刻(第0天)小,但差異無統計學意義(P>0.05)。

表2 不同時期常規超聲和超聲造影對消融灶最大上下徑的測量結果Table 2 Measurements of ablation zone maximum cranio-caudal diameter by conventional ultrasound and contrast-enhanced ultrasound at different time points
3 討論
超聲造影是在常規超聲的基礎上注射造影劑,利用造影劑氣體微泡非線性散射與正常組織的線性散射之間的差異,使用二次諧波成像、反脈沖諧波成像和超寬帶非線性成像等成像技術[9],通過抑制正常組織的信號,使得血管與周圍組織、病灶與正常組織之間形成對比,能夠更好地顯示出組織細小的血流信號,是當前的前沿超聲技術。與常規超聲相比較,超聲造影對超聲機器的配置要求更高,且使用的造影劑較昂貴[9,10]。但與增強MRI和增強CT相比較,超聲造影具有費用較低、操作簡單、無輻射、檢查過程不需麻醉和可實時觀察的優點[9,10],因此廣泛應用于人類肝臟和乳腺等腫瘤疾病的診斷。本試驗結果顯示,HIFU消融后,在常規超聲模式下,消融灶影像表現為同時存在高回聲、等回聲和低回聲的混合回聲影像,消融灶邊界較模糊;在超聲造影模式下,消融灶影像表現為無增強、邊界清楚的均一低回聲,周圍未消融的脾臟增強顯影,消融后隨著時間的推移,消融灶的范圍逐漸變小,但回聲影像無變化。結果表明,2種方法均能顯示出消融灶范圍,但超聲造影顯示的消融灶更清晰、邊界和范圍更明顯。
本試驗分別對麻醉前、后實驗犬的脾臟進行測量,未觀察到麻醉前、后實驗犬脾臟大小發生明顯的變化,且左右徑的比較是2種檢查方法在相同時間進行的橫向比較,麻醉前、后脾臟大小差異對比較的結果沒有影響。在HIFU消融后對消融灶的監測中發現,消融后即刻(第0天)和第3天超聲造影測量的消融灶左右徑明顯大于常規超聲的測量結果,差異有統計學意義(P<0.05),而在消融后第7、14、21和28天測量的左右徑比較中,兩者無統計學差異(P>0.05),說明超聲造影能更清楚地顯示消融灶的左右邊界,但在后續的觀察中超聲造影對左右邊界的顯示無明顯優勢,因此可用常規超聲代替超聲造影對消融灶進行長期觀察,從而簡化檢查過程、降低檢查成本。
對HIFU消融后不同時期消融灶最大上下徑測量的結果顯示,2種檢查方法消融后第3天測得的結果均明顯大于消融后即刻(第0天),差異有統計學意義(P<0.05),消融后第7天測得的消融灶最大上下徑與消融后即刻(第0天)相比無明顯區別(P>0.05),說明HIFU消融后3 d,消融灶由于熱量蓄積的作用,靶區周圍的細胞因熱應激在1~2 d內發生細胞凋亡[11-13],實際的消融病變范圍會比消融時顯示的范圍大,因此在臨床實際工作中,必需充分考慮消融的后延效應,消融的范圍需要謹慎規劃,對周圍健康區域采取一定的保護措施,避免后延效應導致周圍健康組織損傷。
綜上所述,在犬脾臟超聲消融效果評估以及術后對消融灶變化的動態監測中,超聲造影比常規超聲更加敏感、更能準確真實地顯示消融灶的位置和范圍。但為簡化檢查過程、降低檢查成本也可用常規超聲對消融灶進行術后動態監測。

