新型冠狀病毒相關兒童急性壞死性腦病2例
李婕,章瑜,嚴志漢
1.溫州醫科大學附屬第二醫院育英兒童醫院 放射科,浙江 溫州 325027;2.寧波市婦女兒童醫院 放射科,浙江 寧波 315012
新型冠狀病毒(SARS-CoV-2)主要侵犯呼吸系統,隨著臨床數據積累,中樞神經系統受累的報道逐漸增多[1],在兒童和成人中類似。研究[2]發現,大部分感染SARS-CoV-2的兒童神經系統癥狀較輕,主要表現為頭痛、頭暈、嗅覺和味覺異常等。然而,也有一部分患兒出現了癲癇、昏迷和腦膜炎甚至壞死性腦病等嚴重神經系統癥狀[3]。其中急性壞死性腦病(acute necrotizing encephalopathy, ANE)是一種繼發于系統性病毒感染的罕見并發癥,目前國內外有關兒童感染SARS-CoV-2后并發ANE的報道甚少[1,3],但一旦發生往往病情進展非常迅速,預后差,大多數患兒可伴有不同程度的神經系統后遺癥,甚至死亡,目前尚無針對ANE的特異性治療方法[4]。本文報告2例SARS-CoV-2相關兒童ANE,以豐富本病臨床數據,為早期診斷ANE和其治療提供參考。
1 病例資料
病例1,患者,女,13歲,因發熱、嘔吐1 d后出現神志不清在樂清市第三人民醫院就診后病情進展,伴四肢強直抽動,隨即轉入溫州醫科大學附屬第二醫院育英兒童醫院。入院查體:體溫37.5 ℃,格拉斯哥評分7分,瞳孔對光反射遲鈍,咽部查體不配合,頸軟,巴氏征(+),四肢肌力下降,克氏征(-),布氏征(-)。輔助檢查:白細胞計數(white blood cell count, WBC)23.83×109/L,中性粒細胞計數(neutrophil count, NEUT)% 91.1%,IL-6 5.60×10-8mg/mL,IL-10 1.54×10-8mg/mL,CRP 20.13 mg/L,均明顯升高。谷草轉氨酶(aspertate aminotransferase, AST)186 IU/L,肌酸激酶 (creatine kinase, CK)232 IU/L,乳酸脫氫酶(lactic dehydrogenase, LDH)607 IU/L,心肌肌鈣蛋白I(cardiac troponin, cTn I)1.96× 10-7mg/mL,氨基端前腦鈉素(N-terminal probrain natriuretic peptide, NT-proBNP)1.94× 10-7mg/mL,降鈣素原(procalcitonin, PCT)4.38×10-5mg/mL,風疹病毒IgG抗體192.00 IU/mL, 巨細胞病毒IgG抗體>500.00 IU/mL,單純皰疹病毒1 型IgG抗體9.57 COI。腦脊液蛋白水平升高。頭顱MRI平掃顯示腦內多發異常信號(圖1):主要為兩側額頂顳葉、半卵圓中心、側腦室旁、基底節區、丘腦、腦干及小腦,臨床符合ANE診斷。診治經過:患兒住院后給予大劑量甲潑尼龍沖擊治療后減量維持抗炎,大劑量丙球封閉抗體,血漿置換3次,輔以降顱壓、抗感染、保肝護胃、靜脈營養等支持治療。激素沖擊治療第14天時患兒神志稍好轉,至第21天時患兒情緒稍穩定,逐漸好轉,住院1個月余后出院。出院1個月后遺留四肢活動不利、智力下降等,至我院康復科進行康復治療,診斷為“ANE恢復期、不完全性癱瘓、邊緣智力可能”。予運動療法、有氧訓練、經顱磁治療等康復治療后,記憶力較前稍有好轉,肢體力量有所改善。出院3個月后肢體活動基本自如,記憶力較前明顯改善。
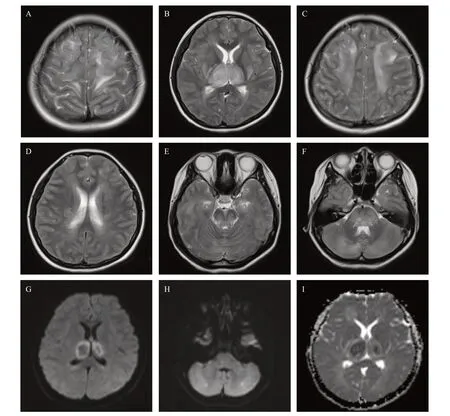
圖1 病例1:13歲女性患者頭顱T2WI、DWI及ADC序列上的表現
病例2,患者,女,2歲,因發熱1 d后出現驚厥于溫州濱海醫院就診后精神差轉至溫州醫科大學附屬第二醫院育英兒童醫院就診。入院查體:體溫38.0 ℃,頸軟,肌力5級,肌張力正常,腦膜刺激征(-),雙側巴氏征(-)。輔助檢查:WBC 46.33× 109/L,NEUT% 76.1%、CRP 16.40 mg/L,明顯升高。AST 98 IU/L、LDH 324 IU/L,NT-proBNP 2.65× 10-7mg/mL,PCT 1.4×10-7mg/mL,風疹病毒IgG抗體90.50 IU/mL,D-D二聚體1.59×10-3mg/mL;腦脊液檢查:氯118.0 mmol/L,余陰性。頭顱MRI平掃檢查顯示腦內多發異常信號(圖2):主要為雙側額頂枕葉、胼胝體、左側基底節區、雙側丘腦及腦干,臨床符合ANE診斷。診治經過:患兒入院后給予甲潑尼龍沖擊治療后減量維持抗炎,同時予大劑量靜脈丙球封閉抗體,期間抗感染、保肝護胃、心肌營養等支持治療同時進行。至激素沖擊治療第3天時患兒能自發睜眼,刺激下能哭,至第9天時神志好轉,住院半月余后出院。出院時遺留語言表達欠佳、肢體無力、站立不穩等障礙,出院1周后肢體乏力有所改善,出院1個月復查腦電圖顯示正常,肢體活動基本自如。
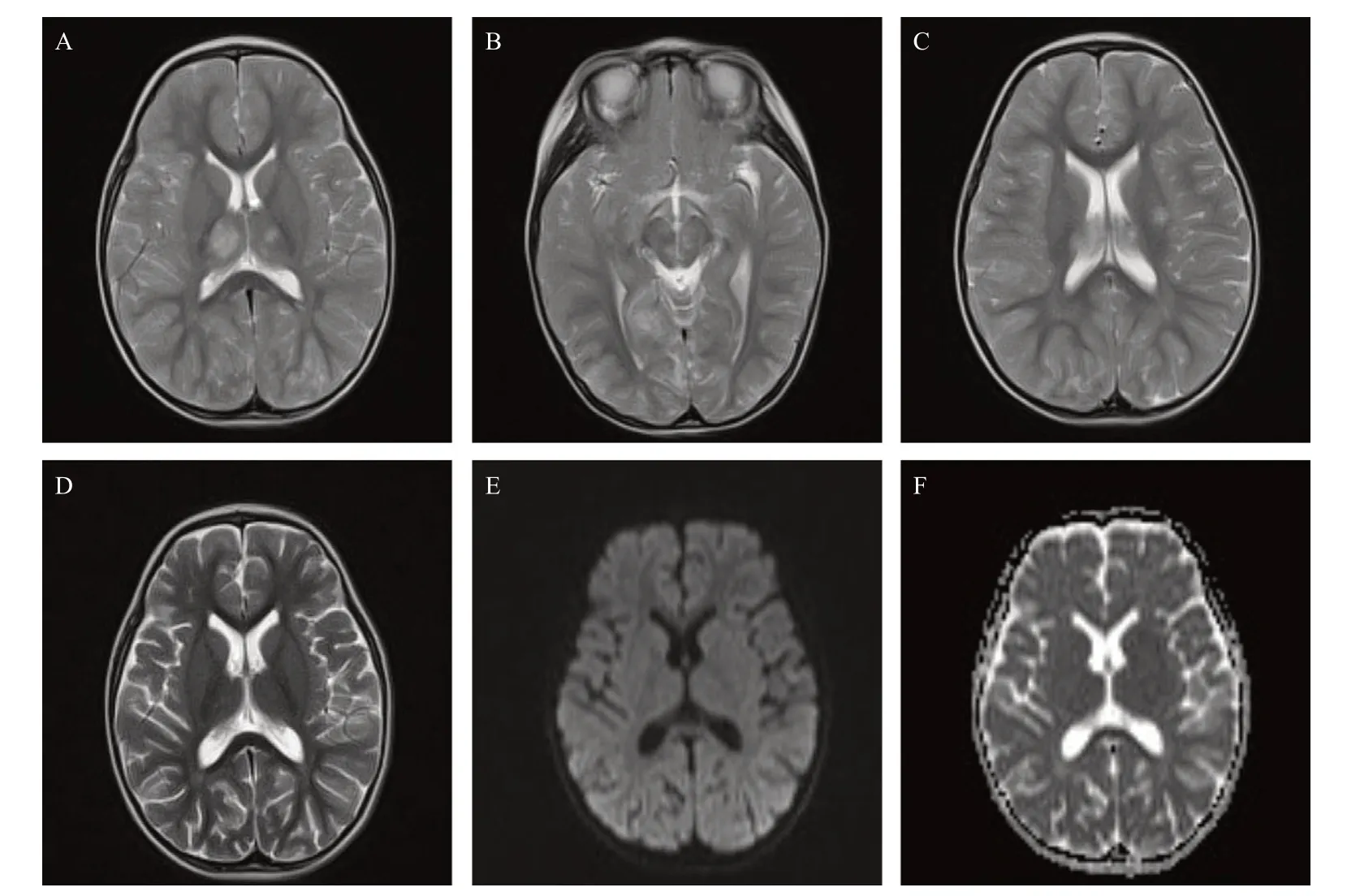
圖2 病例2:2歲女性患者治療前后頭顱MRI對比
2 討論
本文以2022 年12 月至2023 年1月溫州醫科大學附屬第二醫院育英兒童醫院收治的2例感染SARSCoV-2的ANE患兒為研究對象。2例患兒SARS-CoV-2核酸檢測均為陽性且均行1.5T MRI或CT頭顱平掃檢查。納入的診斷標準采用MIZUGUCHI等[5]提出,由NEILSON等[6-7]補充的診斷標準:①病毒所致發熱性疾病1~3 d后快速出現意識障礙或驚厥等急性腦病癥狀。②家族中有相似神經系統感染癥狀者。③復發性腦病伴發熱者。④頭顱影像學檢查(CT或MRI)提示對稱性、多發性病灶,必需部位是雙側丘腦;支持部位包括側腦室周圍白質、內囊、殼核、腦干、小腦。⑤腦脊液中無細胞數升高,蛋白水平升高常見。⑥血清轉氨酶不同程度升高,血氨正常。⑦排除其他疾病,如腦內感染性、代謝性、中毒性、線粒體病、自身免疫性疾病。
在過去的3 年,新型冠狀病毒肺炎(corona virus disease 2019, COVID-19)在全球范圍內大流行,除了顯著的呼吸道表現外,還可能導致各種神經系統并發癥,包括頭痛、味覺和嗅覺改變、腦病、腦血管疾病、肌病、精神疾病和眼部疾病等[8],成人和兒童類似。由SARS-CoV-2感染引起的兒童ANE作為其中一種罕見的腦病,目前僅有國外少數病例報道。
ANE是一種急性爆發性重癥腦病,病程進展迅速,預后差。臨床上以高熱、驚厥、意識障礙(迅速進展至昏迷)和多器官功能衰竭為主要表現。ANE主要繼發于病毒感染,常見的包括甲型流感、乙型流感、H1N1流感、人類皰疹病毒、水痘、輪狀病毒、風疹病毒等,以流感病毒和人類皰疹病毒6為主[9]。本研究依據診斷標準確診的2 例ANE患兒與常見的病毒感染引起的ANE類似,均為前驅感染后出現高熱,并迅速出現意識障礙或驚厥等急性腦病癥狀。2例患兒血液學檢查均有WBC升高,以NEUT上升顯著,CRP、IL亦升高明顯。在許丹等[10]報道的10例其他病毒引起的ANE患兒病例中,所有患兒的WBC和超敏CRP均未明顯升高,這與本研究不一致;但LAZARTERANTES等[11]報道的1例COVID-19相關的ANE患兒也存在WBC升高,我們考慮是由于SARS-CoV-2感染快速進展后合并其他的細菌感染所致。由于感染,其中1例患兒D-D二聚體升高,2例患兒部分Torch抗體升高。ZHOU等[12]報道指出,入院時D-D二聚體升高 (>1 μg/L)是成人COVID-19患者死亡的風險因素。在一組COVID-19兒童患者中也報道了D-D二聚體升高。此外,D-D二聚體水平升高在嬰兒(0至1歲)中比其他年齡組更常見,這可能表明嬰兒比年齡較大的兒童受到COVID-19的影響更嚴重[13]。2例患兒血生化檢查肝酶、NT-proBNP均有升高,提示多臟器損害。其中1例患兒腦脊液蛋白水平升高,其余指標無明顯異常。這些表現與先前文獻報道一致[14]。另外,本組1 例患兒PCT明顯升高,1 例輕度升高。在我國臺灣省13例COVID-19患兒合并腦炎報道[15]中,提示PCT明顯升高,張濤等[16]報道的中國醫科大學附屬盛京醫院的13例ANE患兒也顯示PCT普遍升高,提示COVID-19感染并發腦病或腦炎可以引起PCT升高,但是否可以用PCT的檢測值來評估腦病的嚴重程度還需要進一步研究。
COVID-19 并發ANE的發病機制尚不完全明確。有研究[12]認為,SARS-CoV-2 通過與血管緊張素轉換酶受體結合進入人體細胞,因此表達該受體的細胞最容易受到損傷,比如神經元和神經膠質細胞,以及腦內的內皮和動脈平滑肌細胞,進入機制可能是通過內皮細胞或篩板和嗅球進行血源性播散[17]。然而,中樞神經系統受累也可能是由于類似于噬血細胞性淋巴組織細胞增多癥的“細胞因子風暴”機制[18],即先前的系統性感染引發的強烈全身免疫反應,產生大量炎性細胞因子,使血腦屏障受損,隨后出現水腫、出血及壞死,從而影響了神經系統的功能。此外,研究[19-20]表明ANE有遺傳易感性,RANBP2基因突變與急性壞死性腦病I型相關,更多的證據表明,RanBP2與不同的病毒相互作用以調節病毒感染。因此,目前將ANE分為散發性/孤立性ANE及家族性/復發性ANE,而大部分病例為散發 性[21]。
神經影像學檢查是診斷ANE的重要手段,其特征性影像學表現為多灶性、對稱性腦損害[14]。在MRI上表現為多發性T2WI高信號病灶,主要累及側腦室旁白質、丘腦、殼核、小腦和腦干被蓋,偶見脊髓受累。ANE可見雙側丘腦ADC序列特征性“同心圓結構”、“三色模式”或“靶樣征”:最外層滲出為高信號,反映血管源性水腫,中間層反映細胞毒性水腫為低信號,中心區反映血管周圍出血、神經元壞死為高信號,提示血腦屏障破壞[22]。本組2例患兒均出現了雙側丘腦ADC序列“同心圓樣”異常信號。另有文獻[11]指出,MRI病變的范圍與預后不良相關,特別是累及腦干時,病灶內如果有出血或組織缺損的通常提示預后不良。SARS-CoV-2感染伴神經系統表現的兒童患者最常見的MRI表現包括胼胝體壓部信號改變,包括胼胝體壓部T2高信號病變伴或不伴擴散受限,最有可能繼發于多系統炎癥綜合征,累及胼胝體膝部和半卵圓中心也有報道。
SARS-CoV-2導致的兒童ANE目前尚缺乏有效的特異性治療手段,主要以對癥支持治療為主,由于ANE主要發病機制考慮為“細胞因子風暴”,因此,治療主要用激素沖擊、免疫球蛋白以及血漿置換等免疫調節療法。本研究的2例患兒均早期運用糖皮質激素及人免疫球蛋白治療,1例行血漿置換治療,余治療差異不大。有研究[23]表明,起病24 h內或者早期應用抗生素能使患者有更好的預后,本研究中的2例患兒在早期激素沖擊和丙種球蛋白治療下最終好轉出院,但目前激素使用劑量、療程及是否聯用未有共識,需要擴大樣本量開展對照試驗進一步研究。此外,亞低溫技術(深部體溫35 ℃)治療ANE也有較好的療效,對兒童的預后結局比較重要,尤其是在發病12 h內采用后效果更加顯著[24-25]。早期運用連續性腎臟替代治療(continuous renal replacement therapy, CRRT)于ANE患兒直至意識清醒,出院后隨訪的1年中沒有顯示認知障礙,因此認為及時和持續的CRRT可能有助于ANE取得更好的療效和預后[26]。
ANE多數預后不良,文獻報道病死率為30%~70%,存活者多遺留不同程度的神經系統后遺癥[27]。本研究的2例患兒,隨訪1例出院后1周大致恢復同健康兒童,有1例留有神經系統后遺癥,表現為不完全性癱瘓及智力下降。年齡<2歲、血清天冬氨酸轉移酶顯著升高、腦脊液蛋白顯著升高以及腦干受累通常預示預后不良[4]。朱紅敏等[28]報道的41例ANE,有7例(17.1%)死亡,存活的34例平均隨訪2年(7個月至5.7年),都出現了神經功能障礙,其中輕度8例(23.5%)、中度12例(35.3%)、重度14例(41.2%)。CLEUZIOU等[29]報道的12 家法國醫院兒童重癥監護室的41例流感相關性腦病(influenzaassociated encephalopathy, IAE)中,1/3為ANE,最后死亡7 例(17%),留有神經系統后遺癥20 例(49%),留有嚴重殘疾11例(27%)。可見ANE致殘率極高,因此,幸存患兒后遺癥的康復治療也需引起重視。有研究[4]認為,ANE患兒的神經系統后遺癥可能隨時間推移逐漸減輕甚至消失,遺留神經系統后遺癥的患兒積極進行康復治療可能會逐步改善生存質量。本研究中的病例1患兒采用的康復治療方法主要有運動療法、有氧訓練、作業訓練、生物反饋治療、踩車訓練、單人艙治療、經顱磁治療、言語認知訓練等相應的功能恢復治療手段,在兩次康復治療后,言語、運動和認知功能恢復較好。目前對ANE患兒后期康復治療手段及效果研究較少,將來可以展開更多的研究。
綜上所述,ANE是一種罕見的神經系統危重癥,SARS-CoV-2感染可引起ANE的發生,死亡和傷殘率較高,因此臨床醫師應加強對該病的早期識別能力。當患兒前期感染后迅速出現腦病表現,且影像學有特征的對稱性多發病灶或丘腦“同心圓樣”結構改變,我們應當考慮ANE的可能,并積極予以免疫治療,有助于獲得更好的預后。本研究的局限性在于樣本量過小,且樣本均來自同一地區,將來可以運用腦功能結構成像技術對患兒進行長期隨訪,縱向觀察患兒的細微腦功能結構變化,并且加強對康復治療的研究也是未來的方向。

