MR擴散峰度成像定量參數對不同亞型乳腺癌患者新輔助化療預后的評估價值
張崇杰,楊玨紅,王俊波,郝曉寧,蔡文軍
(1.運城市中心醫院醫學影像科,山西 運城 044000;2.萬榮縣人民醫院影像科,山西 運城 044200)
在對乳腺癌患者的治療中,新輔助化療可通過對病灶部位的有效縮短,進一步降低乳腺癌患者的臨床分期,對于手術切除率的提升具有積極意義[1-2]。但部分患者經過輔助性化療后,其病灶部位的腫瘤體積并未得到有效控制,嚴重影響患者的預后。所以在對患者的治療中,通過有效的臨床影像學指標及時對患者的治療效果進行預測及評估具有積極意義[3]。擴散峰度成像是在傳統的擴散張量成像的基礎上發展而來的新型診斷手段,不僅可以對于組織內的非高斯分布水分子的擴散運動進行分析,同時對于腫瘤組織內的水分子運動進行真實反應[4]。本研究擬分析MR擴散峰度成像定量參數對不同亞型乳腺癌患者新輔助化療預后的評估價值。
1 資料與方法
1.1 一般資料
選取2017年1月至2021年12月運城市中心醫院收治的行新輔助化療方案治療的120例乳腺癌患者作為研究對象,年齡(56.46±5.12)歲,體質量指數(BMI)為(24.83±2.12)kg/m2;TNM分期:Ⅱ期患者44例,Ⅲ期患者76例。Luminal A型患者55例,人表皮生長因子受體2(HER-2)陽性患者36例,三陰性患者29例。納入標準:(1)所有患者均符合腦乳腺癌診斷標準[5],并經過病理學確認;(2)患者均未進行過放化療治療,檢查時間與手術時間的間隔在20 d內。排除標準:患有嚴重心臟或腎臟功能障礙患者,與本研究藥物不耐受患者及伴有其他腫瘤患者。本研究獲醫院倫理委員會審批。
1.2 方法
治療方案:所有患者均采取新輔助化療方案。在化療的第1天,采用多西他賽注射液(齊魯制藥有限公司)80 mg/m2進行靜脈滴注,鹽酸表柔比星注射液[輝瑞制藥(無錫)有限公司]70 mg/m2進行靜脈注射。注射用環磷酰胺(江蘇盛迪醫藥有限公司)6 000 mg/m2進行靜脈注射。每21 d作為1個周期,共計治療3個周期。
化療前分別對所有患者進行MR檢查,本研究中采用的MR儀器主要是由西門子醫療系統有限公司提供。檢查過程中,囑患者采取仰臥位,使患者乳房自然下垂進入乳腺線圈內,在檢查過程中,重復時間設定為4 200 ms,回波時間為70.8 ms,矩陣設定為256*256,視野設定為30*30 cm,層數設定為18,層厚設定為4 mm,層距設定為1.0 mm,激勵次數設定為6次。在對患者的MR擴散峰度成像過程中,在b=0 s/mm2,b=1 000 s/mm2,b=2 000 s/mm2條件下,分別對患者進行掃描,掃描時間設定為4.5 min。同時在取得的影像學圖像分別在工作站中進行上傳,選擇病灶部位較大的層面,使用軟件自動對感興趣區域進行勾畫,分別對平均擴散峰度(MK)及平均擴散系數(MD)進行比較。
1.3 觀察指標
(1)比較不同分子分型患者的一般資料:分別對Luminal A組、HER-2組及三陰性組患者的年齡、BMI、TNM分期進行比較。(2)不同分子分型患者的核磁共振擴散峰度成像參數比較。分別對Luminal A組、HER-2組及三陰性組患者的MK、MD進行比較。(3)不同治療效果患者的MR擴散峰度成像參數比較。根據化療后的病理表現[6],可將患者分為完全緩解(pathological complete regress,pCR)組和非pCR組,其中pCR組患者52例,非pCR組患者68例,比較兩組患者的MK、MD之間的差異。(4)MK、MD對治療效果完全緩解的預測效果。采取并聯方式,分析單獨檢測及聯合檢測對乳腺癌患者完全緩解的預測效能。(5)ROC曲線分析。采用ROC曲線分析,研究單獨檢測及聯合檢測對乳腺癌患者完全緩解的曲線下面積(AUC)之間的差異。
1.4 統計學分析
2 結果
2.1 不同分子分型患者的一般資料比較
Luminal A組、HER-2組及三陰性組患者的年齡、BMI及TNM分期之間比較,差異均無統計學意義(P>0.05)。見表1。
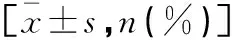
表1 不同分子分型患者的一般資料比較
2.2 不同分子分型患者的MR擴散峰度成像參數比較
化療前,不同分子分型患者的MR擴散峰度成像參數比較,差異均無統計學意義(P>0.05)。化療后,三組患者的MK、MD均下降(P<0.05),且Luminal A組>HER-2組>三陰性組(P<0.05)。見表2。
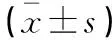
表2 不同分子分型患者的MR擴散峰度成像參數比較
2.3 不同治療效果患者的MR擴散峰度成像參數比較
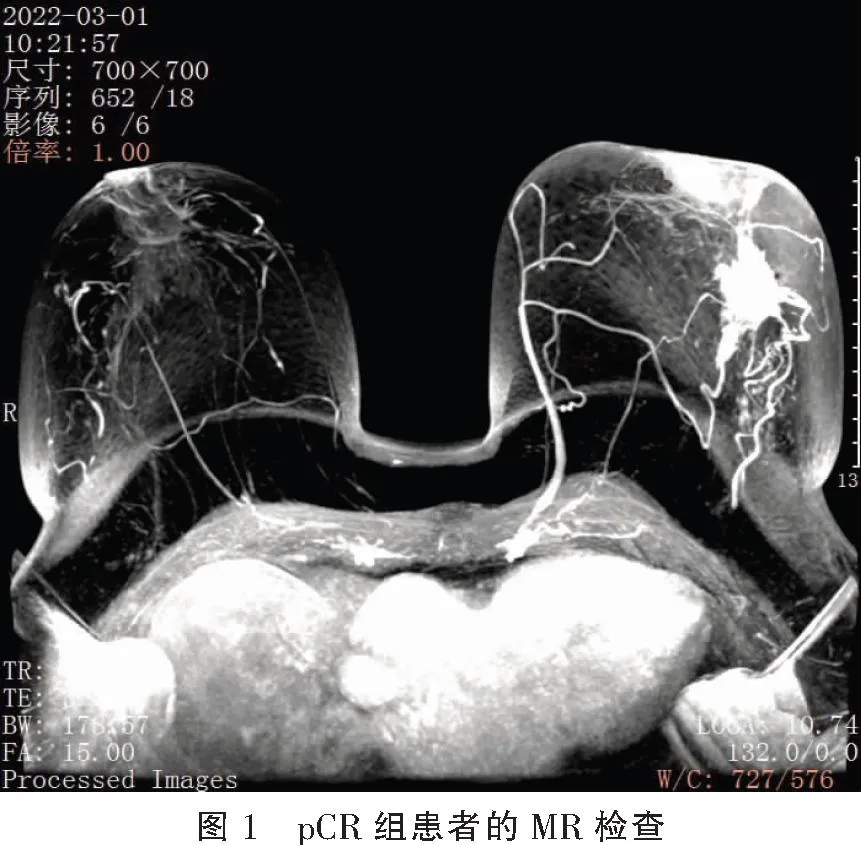
化療前,不同治療效果的MR擴散峰度成像參數比較,無統計學差異(P>0.05)。化療后,pCR組及非pCR組患者的MK、MD均下降,且pCR組低于非pCR組(P<0.05)。見表3、圖1及圖2。
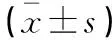
表3 不同治療效果患者的MR擴散峰度成像參數比較
2.4 MK、MD對治療效果完全緩解的預測效果比較
MK、MD聯合檢測對治療效果完全緩解的預測敏感度高于單獨檢測(P<0.05)。見表4。
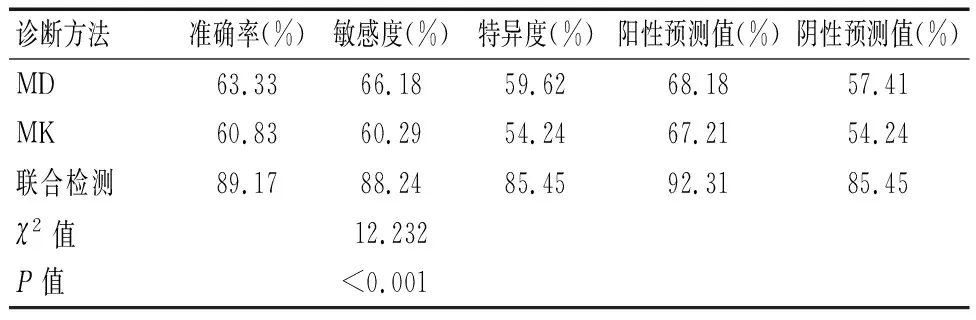
表4 MK、MD對治療效果完全緩解的預測效果比較
2.5 MK、MD及二者聯合檢測對治療效果完全緩解的診斷效能
通過ROC曲線分析,MK、MD及二者聯合檢測對治療效果完全緩解的AUC分別為0.778、0.792、0.832,且二者聯合檢測的AUC最大。見表5。
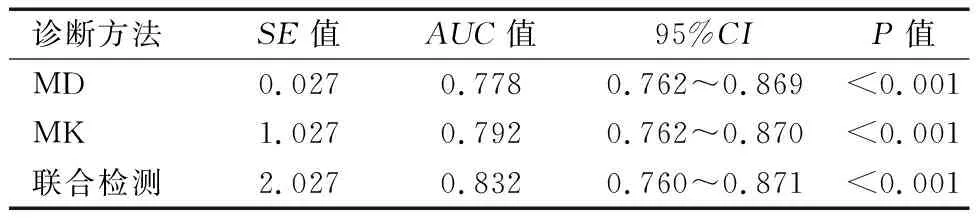
表5 MK、MD及二者聯合檢測對治療效果完全緩解的診斷效能
3 討論
在對乳腺癌患者的治療中,采用新輔助化療手段進行治療,可有效縮小患者的病灶,進一步控制或者消滅局部病灶,有效提升手術效果。但既往研究[7]指出,乳腺癌患者在經過新輔助化療后,其腫瘤密度并未得到有效的改善,甚至腫瘤組織發生進展,對于患者的預后具有不良影響[8]。本研究中,通過對患者的治療效果進行分析,完全緩解患者的比例達到60%以上,依然有30%以上的人群效果未達到治療目的。所以在對患者的治療中,通過對患者的預后進行有效評估,及時對患者的治療方案進行調整,改善患者的生命質量,對于患者的預后具有積極意義[9]。
在對患者MR檢查中,通過對局部病灶部位腫瘤組織中水分子擴散的方向及擴散程度進行分析,進一步對組織的微觀結構變化、擴散峰度成像、水分子的擴散程度及擴散方向進行量化分析[10]。在本研究中,MK主要是峰度在所有方向上的平均值,對于病灶部位的腫瘤及正常組織微結構的復雜程度具有指導意義。而MD是在各個方向上水分子的彌散程度[11-12],可以對患者組織內的水含量進行分析。通過對不同分子亞型及治療效果的MK及MD的分析,其差異有統計學意義[13]。分析認為,在乳腺癌患者的疾病進展中,由于腫瘤細胞的增生多呈現無序增生,導致局部病灶部位新生血管的增生較為畸形,同時局部內皮細胞功能的下降,也是造成局部正常組織纖維化及結締化的重要因素[14]。在腫瘤細胞的不斷進展中,隨著纖維化程度的升高,局部病灶部位的整體密度呈現上升趨勢,而水分子的整體含量下降。同時在腫瘤細胞對不同方向的組織浸潤過程中,其新生血管的迂曲等,造成局部水分子向不同方向的運動不協調,最終造成患者的MD及MK的異常改變[15]。而在聯合檢測效能的分析中,通過對患者的MD及MK的聯合檢測,其對治療完全緩解的預測效能較好。提示通過對患者病灶部位的腫瘤組織的水分子含量及水分子在各個方向的運動情況進行綜合分析,可有效預測患者的治療效果[16-17],與吳磊[18]通過對乳腺癌患者采取新輔助化療治療中采取MRI擴散峰度成像進行分析,具有顯著的治療效果預測價值相一致。
綜上,MR擴散峰度成像定量參數的聯合檢測,可以對不同亞型乳腺癌患者新輔助化療的治療效果進行有效預測。

