膿毒癥合并急性腎損傷患者炎癥因子、血流動力學變化與腎功能轉歸的關系
亢志琴,黃靜,楊美霞
(山西白求恩醫院,1急診內科,2急診外科,山西 太原 030000)
膿毒癥指宿主對感染的免疫反應失調引起的危及生命的器官功能障礙,是ICU常見的急危重癥[1-2]。腎臟是膿毒癥最易累及的靶器官,急性腎損傷(Acute kidney injury,AKI)是指機體在短時間內出現腎功能急速下降的臨床綜合征,是膿毒癥最常見、最嚴重的并發癥,發生率高達膿毒癥患者的66%,不僅增加患者痛苦、增加治療難度,還極大程度增加患者死亡風險[3]。目前統計顯示,全球范圍內每年約1300萬人患AKI,約170萬人死于AKI及相關并發癥嚴重威脅人民的生命安全,早期分析患者腎功能轉歸對指導治療方案、改善患者預后至關重要[4]。目前臨床評估腎功能及評價預后指標多為肌酐及尿量,但影響其的因素較多,在評價腎功能轉歸情況具有一定局限性。近年研究發現,炎癥因子及血流動力學改變可影響膿毒癥合并AKI患者腎功能變化[5-6],與患者腎功能轉歸方面存在一定聯系。本研究選擇膿毒癥合并AKI患者為觀察對象,旨在分析膿毒癥合并AKI患者炎癥因子、血流動力學變化與腎功能轉歸的關系。
1 資料與方法
1.1 一般資料
選擇2021年1月至2022年12月于山西白求恩醫院收治的膿毒癥合并AKI患者120例為觀察對象,納入標準:(1)患者均符合國際關于膿毒癥的診斷標準[7];(2)患者符合國際改善全球腎臟病預后組織(KDIGO)所制定的AKI診斷標準[8];(3)臨床資料完整無流失。排除標準:(1)為哺乳期或妊娠期婦女;(2)合并惡性血液病;(3)1個月內應用免疫抑制劑;(4)合并重要器官嚴重功能障礙。根據28 d腎小球濾過率(Glomerular filtration rate,eGFR)水平分為A組(28 d eGFR≥90 mL·min-1·1.73 m-2,n=36)、B組(15 mL·min-1·1.73 m-2≤28 d eGFR<90 mL·min-1·1.73 m-2,n=66)、C組(28 d eGFR<15 mL·min-1·1.73 m-2,n=18)。其中A組男性20例,女性16例,年齡(71.25±5.85)歲;B組男性36例,女性30例,年齡(70.86±4.04)歲;C組男性10例,女性8例,年齡(71.07±5.23)歲。各組年齡、性別等資料比較,差異無統計學意義(P>0.05)。本研究均經醫院倫理會批準同意。
1.2 觀察指標
實驗室指標:采集各組受檢者入急診2 h內的靜脈血,3 000 r/min離心10 min,于-40 ℃環境中低溫保存,避免反復凍融。采用酶聯免疫吸附法檢測患者白細胞介素6(IL-6)、腫瘤壞死因子α(TNF-α)、降鈣素原(PCT)]水平。
血流動力學評價:采用心電監護儀檢測并記錄各組患者平均動脈壓(MAP)、心率(HR)、心排出量(CO),計算心臟指數(CI)值,CI=CO(L/min)/體表面積(m2)。
1.3 統計學分析
2 結果
2.1 各組患者血清炎癥指標比較
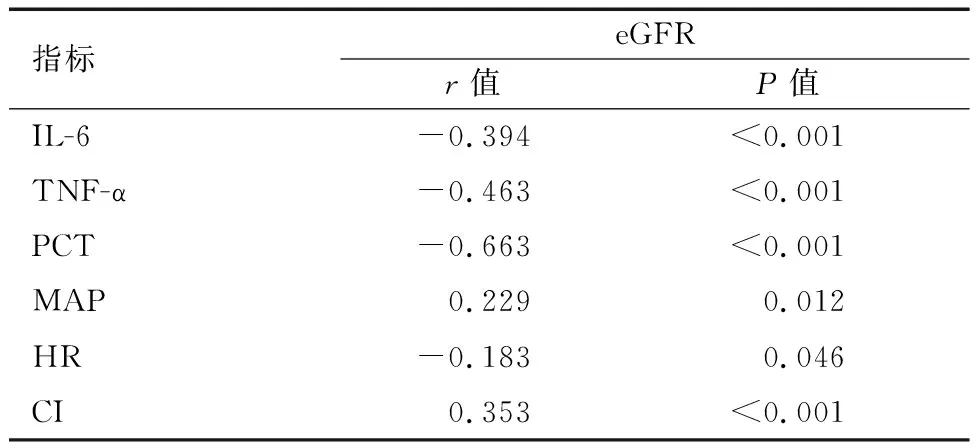
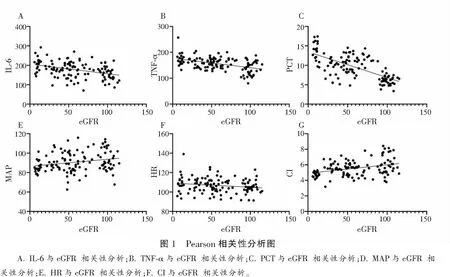
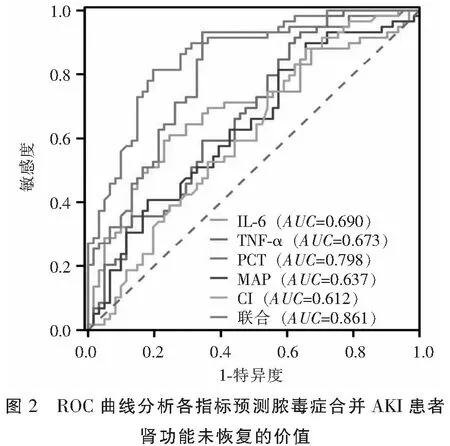
各組患者血清IL-6、TNF-α、PCT水平比較:A組 表1 各組患者血清炎癥指標比較 各組患者HR水平無統計學差異(P>0.05)。B組、C組患者CI水平低于A組,C組患者MAP、CI水平低于B組,差異有統計學意義(P<0.05)。見表2。 表2 各組患者血流動力學指標比較 Pearson相關性分析顯示,IL-6、TNF-α、PCT、HR與膿毒癥合并AKI患者28 d eGFR水平負相關(r=-0.394、-0.463、-0.663、-0.183,P<0.05);MAP、CI與膿毒癥合并AKI患者28d eGFR水平正相關(r=0.229、0.353,P<0.05)。見表3及圖1。 表3 膿毒癥合并AKI患者炎癥因子、血流動力學與腎功能轉歸的相關性分析 ROC曲線顯示,IL-6、TNF-α、PCT、MAP 、CI在預測膿毒癥合并AKI患者腎功能未恢復的曲線下面積(AUC)分別為0.690、0.673、0.798、0.637、0.612,多項指標聯合預測膿毒癥合并AKI患者腎功能未恢復的AUC為0.861(P<0.05)。見表4及圖2。 表4 ROC曲線分析各指標預測膿毒癥合并AKI患者腎功能未恢復的價值 膿毒癥是由宿主對感染的反應失調引起的器官功能障礙,感染最常見的器官之一是腎臟,導致AKI的發生,增加了患慢性伴隨性疾病的風險,此外膿毒癥AKI常見于危重患者,與慢性腎臟病、心血管事件和死亡風險增加等不良結局密切相關。目前,研究[9]發現,膿毒癥合并AKI患者死亡率比膿毒癥無AKI患者高3~5倍,早期預測膿毒癥合并AKI患者腎功能轉歸情況并給予針對性干預有助于改善患者預后。 目前臨床多選擇血清肌酐和尿量用于AKI診斷和分期。但血清肌酐和尿量的變化在實際腎損傷后發生相對較晚,因此不能提供AKI的早期或及時檢測。此外,血清肌酐和尿量受到多種因素的影響,例如脫水、膳食蛋白質攝入、肌肉質量、利尿劑等,因此在預測腎功能轉歸情況存在一定滯后性[10-11]。PCT是由116個氨基酸殘基組成的糖蛋白質,是由甲狀腺C細胞生成的降鈣素的前體蛋白,臨床多選擇PCT作為反應細菌感染的敏感指標,反應全身炎癥反應的活躍程度,膿毒癥感染后,PCT水平急速升高,且PCT水平越高說明膿毒癥病情越嚴重,對腎功能損傷情況越顯著,因此可能影響腎功能轉歸[12-13]。IL-6作為一種前炎性細胞因子,可參與機體應激反應及免疫調節過程,當膿毒癥導致機體全身炎癥反應時,IL-6水平升高參與以單核巨噬細胞系統激活為主的早期炎癥反應,導致腎功能損傷,影響腎臟疾病的發生、發展及轉歸[14]。TNF-α是腎臟損傷因素之一,可通過炎癥反應誘導動脈粥樣硬化,導致腎功能損傷,而腎功能損傷可出現機體液體潴留、機械張力增加情況,加重炎癥反應,形成惡性循環,因此TNF-α的高表達對腎功能轉歸造成不利影響。本研究中,B組、C組患者血清IL-6、TNF-α、PCT水平高于A組,C組患者血清IL-6、TNF-α、PCT水平高于B組。說明膿毒癥合并AKI患者血清IL-6、TNF-α、PCT水平變化與腎功能轉歸情況存在一定聯系,與王佳等[15]研究結果類似,該研究發現,血清NGAL、PCT水平的升高與膿毒癥合并AKI患者腎功能轉歸不良有關,早期監測其水平變化有助于預測患者預后情況。 膿毒癥發生后,機體可出現不同程度的外周血管收縮舒張功能異常情況,導致機體血流分布異常,從而出現血流動力學改變。CI反應機體心功能變化,CI水平越高說明機體處于高循環狀態,不僅增加心臟負擔,誘導心力衰竭等心臟病,還可能增加因心源性休克、急性心力衰竭導致的AKI,加重膿毒癥病情[16-17]。MAP水平變化可反映機體血液循環及供應狀態,是評價人體狀態的指標之一,MAP水平較低,機體腎臟的血液供應越低,腎臟組織缺血缺氧情況越嚴重,對腎功能轉歸造成不利影響[18-19]。本研究中,B組、C組患者CI水平高于A組,C組患者MAP、CI水平高于B組。說明膿毒癥合并AKI患者血流動力學改變與腎功能轉歸存在一定聯系,另外Pearson相關性分析顯示,IL-6、TNF-α、PCT與膿毒癥合并AKI患者28d eGFR水平負相關;MAP、CI與膿毒癥合并AKI患者28d eGFR水平正相關。ROC曲線顯示,IL-6、TNF-α、PCT、MAP、CI、多項指標聯合診斷在預測膿毒癥合并AKI患者腎功能未恢復的AUC分別為0.690、0.673、0.798、0.637、0.612、0.861。說明膿毒癥合并AKI患者炎癥因子及血流動力學變化與腎功能轉歸存在密切聯系,早期監測其水平變化有助于預測腎功能未恢復風險,多項指標聯合診斷效果更佳,有助于醫師早期預測膿毒癥合并AKI患者預后情況,對指導治療方案、改善患者預后情況具有重要意義。 綜上,IL-6、TNF-α、PCT、MAP、CI與膿毒癥合并AKI患者腎功能轉歸不良相關,早期監測有助于預測膿毒癥合并AKI患者預后情況,監測其水平變化可提高臨床預測預后的準確性,對臨床實踐具有一定指導意義,可幫助指導治療方案幫助提高治療效果,降低住院費用及病死率。
2.2 各組患者血流動力學指標比較
2.3 膿毒癥合并AKI患者炎癥因子、血流動力學與腎功能轉歸的相關性分析
2.4 ROC曲線分析各指標預測膿毒癥合并AKI患者腎功能未恢復的價值

3 討論

