北極甜蝦廢棄物多肽鉬螯合物的抗氧化性研究
◎ 劉雪凌,于 翠,亢 娜,林 貝,周莉莉
(燕京理工學院,河北 三河 065201)
微量金屬螯合物可以補充人體微量必需礦物質。現階段,市面上有無機鹽金屬礦物質補充劑、有機金屬礦物質補充劑、氨基酸(蛋白質或多肽)金屬礦物質補充劑等[1]。以北極甜蝦蝦殼為原料制備多肽鉬螯合物,可以在降低環境污染的同時,利用蝦殼生產高附加值產品,最大化利用蝦類廢棄物。
1 材料與方法
1.1 材料與試劑
北極甜蝦蝦殼,山東榮信水產食品集團股份有限公司提供;木瓜蛋白酶(800 μ/mg,生化試劑),山東卡貝因生物科技有限公司;無水乙醇(分析純),山東德彥化工有限公司;磷酸氫二鈉(分析純),廊坊市金海化工有限公司;三氧化鉬(分析純),天津市光復精細化工研究所;氫氧化鈉(分析純),天津市永大化學試劑有限公司;鹽酸羥胺(分析純),重慶市茂榮化工貿易有限公司;DPPH·(1,1-二苯基-2-三硝基苯肼)(分析純),北京百奧萊博科技有限公司;ABTS[2,2-聯氮-二(3-乙基-苯并噻唑-6-磺酸)二銨鹽](分析純),酷爾化學科技有限公司;過硫酸鉀(分析純),河南銘之鑫化工產品有限公司;鄰二氮菲(分析純),隨州佳科生物工程有限公司;硫酸亞鐵(分析純),濟南裕景成林經貿有限公司。
1.2 儀器與設備
FA1004B電子分析天平,上海佑科儀器有限公司;電熱恒溫鼓風干燥機,滄州晶碩試驗儀器有限公司;pH計,煙臺凱米斯儀器有限公司;HH-6恒溫水浴鍋,江蘇省金壇市榮華儀器制造有限公司;DT5-6低速臺式離心機,北京時代北利離心機有限公司;UV-1601紫外分光光度計,北京北分瑞利分析儀器(集團)公司。
1.3 實驗方法
1.3.1 北極甜蝦蝦殼多肽的制備
將提前烘干、粉碎的北極甜蝦蝦殼取適量,用無水乙醇脫色,過濾,濾渣用去離子水洗滌2~3次后,加入10%[酶的質量(mg)/溶劑體積(mL)]的木瓜蛋白酶溶液,在50 ℃、pH為4的條件下,制取蝦殼多肽。利用旋轉蒸發儀進行離心分離,取上清液放進烘箱進行烘干,即得蝦殼多肽[2]。
1.3.2 北極甜蝦蝦殼多肽鉬螯合物的制備
在蝦殼多肽中按照北極甜蝦蝦殼多肽與三氧化鉬質量比為1∶5,加入被氫氧化鈉溶解的三氧化鉬,螯合反應溫度為55 ℃,螯合反應pH為6,螯合反應時間為120 min。用90%以上的乙醇進行沉淀,靜置3 h,抽濾、干燥,即得北極甜蝦蝦殼多肽鉬螯合物[3]。
1.3.3 北極甜蝦蝦殼多肽鉬螯合物的抗氧化性研究
取適量北極甜蝦蝦殼多肽鉬螯合物,對DPPH·、ABTS、·OH 3種自由基進行清除效果實驗。整個研究探索了多肽鉬螯合物濃度、反應時間、反應溫度,對北極甜蝦蝦殼多肽鉬螯合物抗氧化性的影響[4]。
(1)對DPPH·清除率的計算
用C2H6O(AR)配制0.1 mmol/L的DPPH溶液,陰暗處保存。將2.0 mL北極甜蝦蝦殼多肽溶液與2.0 mL該溶液混合。在強吸收波長處測吸光度(A1),空白組為2.0 mL無水乙醇加上2.0 mL的蒸餾水,測定其吸光度(A2),對照組為2.0 mL DPPH溶液加上2.0 mL的蒸餾水代替樣品,測定其吸光度(A3),用2 mL蒸餾水和2 mL無水乙醇混合做對照[5]。公式計算如下。
(2)對ABTS清除率的計算
將1滴北極甜蝦蝦殼多肽溶液與ABTS工作液均勻混合,在陰暗處靜置6 min。在734 nm波長處測吸光度,測定3次[5]。按以下公式進行清除率的計算。
式中,A0為不加樣品,加入ABTS的吸光度;Ai為北極甜蝦蝦殼多肽與ABTS反應的吸光度。
(3)對·OH清除率的計算
取鄰二氮菲溶液20滴至于試管中,依次加入緩沖液(pH為7.4)40滴、蒸餾水20滴、 硫酸亞鐵溶液10滴,充分搖勻,加 H2O24滴,溫度人體常溫即可,恒溫水浴鍋中45 min,于536 nm處測其吸光度,其值稱AD[7]。同前步,將其中用20滴蒸餾水代替H2O2測得的吸光度稱AB。再用試樣液1 mL代替第一步中的蒸餾水,測得的吸光度稱As。
·OH自由基清除率計算公式如下:
2 結果與討論
2.1 濃度對自由基清除率的影響
濃度對自由基清除率的影響見圖1。從圖1可以看出,不同多肽鉬螯合物濃度對3種自由基的清除率均有影響,隨著濃度的增加,對自由基的清除率也會增加。通過比較可知,多肽鉬螯合物清除ABTS所需濃度最低。

圖1 濃度對自由基清除率的影響圖
2.1.1 多肽鉬螯合物濃度對DPPH·清除率的影響
隨著多肽鉬螯合物的濃度增加,其與DPPH自由基的結合率越高,清除率逐漸上升,直至濃度達到6 mg/mL時,清除率幾乎保持不變,表明已將DPPH自由基全部消耗,說明抗氧化性隨著多肽鉬螯合物濃度的增加而增加,在6 mg/mL時達到飽和狀態。
2.1.2 多肽鉬螯合物濃度對ABTS清除率的影響
隨著多肽鉬螯合物濃度的增加,其清除率逐漸增加直至不變。在0.5 mg/mL濃度以下,由于反應的逐步進行,越來越多的ABTS自由基被多肽鉬螯合物還原,直至濃度高于0.5 mg/mL后,ABTS自由基全部被還原,清除率保持恒定,說明在0.5 mg/mL時反應已達到飽和狀態。
2.1.3 多肽鉬螯合物濃度對·OH清除率的影響
隨著多肽鉬螯合物濃度的增加,該清除能力不斷加強。當濃度為9 mg/mL時,對·OH清除效果最好,高達91.9%。
2.2 反應溫度對自由基清除率的影響
溫度對自由基清除率的影響見圖2。從圖2可以看出,不同溫度對3種自由基的清除率的影響規律相似,均是先升高后降低。通過比較可知,多肽鉬螯合物清除DPPH·所需最適溫度最低,其次是·OH,最后為ABTS。

圖2 反應溫度對自由基清除率的影響圖
2.2.1 多肽鉬螯合物反應溫度對DPPH·清除率的影響
圖2表明,清除率隨著溫度的增加而減小。導致清除率降低的原因可能是溫度升高引起多肽鉬螯合物結構改變,其多肽鏈越長該物質熱穩性越差。由圖2可見,此多肽鉬螯合物在5 ℃清除效果最好。
2.2.2 多肽鉬螯合物反應溫度對ABTS清除率的影響
隨著溫度升高,清除率不斷升高,40 ℃時達到清除率頂點值94.64%。40 ℃以后,清除率隨著溫度逐漸下跌,到50 ℃逐漸平穩。可知,溫度為40 ℃為此反應的最佳溫度。
2.2.3 多肽鉬螯合物反應溫度對·OH清除率的影響
當反應溫度增加時,對·OH清除率不斷攀升,30 ℃時,清除率達到最高點,高于30 ℃時,對·OH自由基的清除率逐步回跌。說明多肽鉬螯合物在30 ℃時對·OH清除效果最好。
2.3 反應時間對自由基清除率的影響
反應時間對自由基清除率的影響見圖3。從圖3可以看出,不同溫度對3種自由基的清除率的影響不同,對ABTS、·OH的清除率均是先升高后降低,而對于DPPH·的清除率則達到一定時間后趨于穩定。通過比較可知,多肽鉬螯合物清除ABTS所需時間最短。
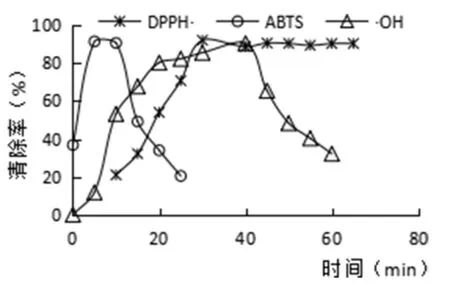
圖3 反應時間對自由基清除率的影響圖
2.3.1 多肽鉬螯合物反應時間對DPPH·清除率的影響
多肽鉬螯合對DPPH·清除率隨著反應時間的增加而增加,在30 min后幾乎不變。因此,最佳清除反應時間為30 min。
2.3.2 多肽鉬螯合物反應時間對ABTS清除率的影響
隨著反應時間的增加,多肽鉬螯合物對ABTS自由基的清除率先增加后減小。反應5~10 min清除率達到穩定,為最佳反應時間。
2.3.3 多肽鉬螯合物反應時間對·OH清除率的影響
當0 min時,羥自由基(·OH)清除率不到1%,可知此反應很緩慢。清除率隨著時間推移而增高。40~50 min,羥自由基(·OH)清除率有所下降。反應時間為40 min時,對·OH的清除率為90.15%,為最大值。
3 結語
本研究利用北極甜蝦廢棄物進行多肽鉬螯合物的制備,通過對其抗氧化性的研究探索,得知北極甜蝦多肽鉬螯合物具有一定的抗氧化性,不同自由基等氧化物的抗氧化條件不同,其抗氧化能力不同。今后的抗氧化性研究,應該結合多肽鉬螯合物的制備工藝,不僅需要用螯合率作為比較指標,還需要增加抗氧化性指標,以提高該多肽鉬螯合物的應用價值。

