卡瑞利珠單抗聯合mFOLFIRI方案對結腸癌的療效及其對血管新生指標及惡性細胞增殖活性的影響
孟元普 裴 哲 周 博
結腸癌是消化科常見癌癥之一,早期癥狀不明顯,據報道,75%以上患者確診時已屬于晚期,錯失最佳手術時機[1]。mFOLFIRI方案是不可切除的晚期結腸癌一線治療方案,但部分患者發生化療耐藥,導致預后不良[2]。卡瑞利珠單抗是一種人源化單克隆抗體,與PD-1受體結合,阻斷PD-1/PD-L1結合而激活T細胞,產生持續抗腫瘤效應[3]。血管新生與結腸癌腫瘤生長、轉移密切相關,血管內皮生長因子(VEGF)、VEGF受體-2(VEGFR-2)、血管生成素-2(Ang-2)等血管生長因子在此過程中發揮重要作用[4]。另研究證實,磷脂酰肌醇3-激酶(PI3K)/絲氨酸-蘇氨酸蛋白激酶(Akt)通路過度激活與腫瘤細胞惡性增殖有關[5]。基于此,本研究嘗試探討卡瑞利珠單抗聯合mFOLFIRI方案治療結腸癌對血管新生指標及惡性細胞增殖活性影響。
1 資料與方法
1.1 一般資料
選取2019年12月至2020年12月我院結腸癌患者106例進行前瞻性研究,采用簡單隨機化法分為觀察組(n=53)、對照組(n=53)。兩組性別、年齡、體質量指數(BMI)、病變位置、病理類型、腫瘤大小、轉移部位比較,差異無統計學意義(P>0.05),見表1。

表1 兩組一般資料比較
納入標準:①經病理或細胞學診斷為結腸癌,屬晚期結腸癌(Ⅳ期);②均為初治;③KPS積分≥60分;④至少有一個可測量病灶;⑤患者及家屬知情同意,簽署同意書。排除標準:①合并其它惡性腫瘤;②合并嚴重高血壓、心功能不全及肝腎功能明顯異常;③嚴重感染;④精神障礙;⑤正在參加其他藥物臨床試驗;⑥妊娠婦女。
1.2 方法
對照組采用mFOLFIRI方案治療,伊立替康(江蘇恒瑞醫藥股份有限公司,國藥準字H20040711)180 mg/m2,第1 d、第8 d,靜滴;亞葉酸鈣(齊魯制藥有限公司,國藥準字H20184093)100 mg/m2,第1~5 d,5-氟尿嘧啶前靜滴;5-氟尿嘧啶(西南藥業股份有限公司,國藥準字H50020128)400 mg/m2,第1~5 d,靜脈注射。3周為1個周期,治療2個周期。觀察組于對照組基礎上給予卡瑞利珠單抗(蘇州盛迪亞生物醫藥有限公司,國藥準字S20190027),200 mg,靜滴,1次/3周,應用2次。
1.3 觀察指標與檢測方法
(1)療效。依據實體瘤療效評價標準[6],目標病灶完全消失并維持4周以上為完全緩解(CR);基線病灶長徑總和縮小>30%,并維持4周以上為部分緩解(PR);基線病灶長徑總和增加>20%或出現新病灶為疾病進展(PD);介于PR、PD之間為疾病穩定(SD)。將CR、PR、SD計入疾病控制率。(2)不良反應發生率,參照常見不良反應事件評價標準4.0版[7]及皮膚及皮下組織疾病分級標準[8](皮膚毛細血管增生癥)。(3)治療前后血清腫瘤標志物[癌胚抗原(CEA)、結腸癌特異性抗原-2(CCSA-2)、糖類抗原199(CA199)]水平。采集空腹肘靜脈血3 ml,離心(時間15 min,半徑8 cm,轉速3500 r/min),取血清,采用酶聯免疫吸附試驗測定CEA、CCSA-2、CA199,均使用美國Abcam公司試劑盒。(4)治療前后血清血管新生指標(VEGF、VEGFR-2、Ang-2)水平。VEGF、VEGFR-2、Ang-2均采用酶聯免疫吸附試驗測定,使用上海紀寧生物制劑公司試劑盒。(5)惡性細胞增殖活性[治療前后血清PI3K、Akt水平]。PI3K、Akt采用酶聯免疫吸附試驗測定,使用上海廣瑞生物科技有限公司試劑盒。(6)生活質量狀況。治療后KPS評分增加≥10分為提高;治療后KPS評分減少≥10分為降低;治療后KPS評分變化<10為穩定。
1.4 統計學方法
應用統計學軟件SPSS 25.0處理數據,計數資料以例數描述,采用χ2檢驗,計量資料采取Bartlett方差齊性檢驗與Kolmogorov-Smirnov正態性檢驗,均確認具備方差齊性且近似服從正態布,以平均數±標準差描述,兩組間比較采用獨立樣本t檢驗,組內對比采用配對t檢驗。均采用雙側檢驗,α=0.05。
2 結果
2.1 療效
觀察組疾病控制率(88.68%)高于對照組(73.58%)(P<0.05)。見表2。

表2 兩組療效對比(例,%)
2.2 不良反應
兩組不良反應發生率比較無顯著性差異(P>0.05)。見表3。

表3 兩組不良反應情況對比(例,%)
2.3 腫瘤標志物
治療前兩組血清CEA、CCSA-2、CA199水平比較,差異無統計學意義(P>0.05);治療后兩組血清CEA、CCSA-2、CA199水平低于治療前,且觀察組低于對照組(P<0.05)。見表4。
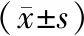
表4 兩組血清腫瘤標志物水平對比
2.4 血管新生指標
治療前兩組血清VEGF、VEGFR-2、Ang-2水平比較,差異無統計學意義(P>0.05);治療后兩組血清VEGF、VEGFR-2、Ang-2水平低于治療前,且觀察組低于對照組(P<0.05)。見表5。

表5 兩組血管新生指標對比
2.5 PI3K、Akt
治療前兩組血清PI3K、Akt水平比較,差異無統計學意義(P>0.05);治療后兩組血清PI3K、Akt水平低于治療前,且觀察組低于對照組(P<0.05),見表6。

表6 兩組血清PI3K、Akt水平對比
2.6 生活質量
觀察組生活質量提高穩定率(83.02%)高于對照組(64.15%)(P<0.05),見表7。

表7 兩組生活質量對比(例,%)
3 討論
結腸癌在我國發病率較高且逐年上升,化療是晚期結腸癌主要治療手段。研究證實,以伊立替康為主的mFOLFIRI方案(含伊立替康、氟尿嘧啶、亞葉酸鈣)對晚期結直腸癌有較好療效,毒副反應可耐受,已廣泛用于晚期結腸癌的一線或二線治療[9]。但在與腫瘤抗爭過程中,腫瘤細胞可產生原發或繼發性耐藥,導致化療失敗。為進一步提高結腸癌治療效果,需積極探索新的有效藥物。
腫瘤免疫逃逸是結腸癌發生發展的重要機制之一,其中免疫檢查點是關鍵環節之一。PD-1/PD-L1軸是生理免疫穩態的關鍵決定因素。免疫細胞,尤其T細胞表面的PD-1結合抗原呈遞細胞表面的PD-L1后產生抑制信號,避免免疫細胞在外源體侵入或機體感染時產生過度免疫應答。卡瑞利珠單抗是人源化IgG4κ型抗PD-1單克隆抗體,通過結合PD-1,阻斷PD-1/PD-L1通路,激活T細胞而發揮抗腫瘤效應[10]。目前,卡瑞利珠單抗已在多種實體瘤中開展了臨床試驗,吳克林等[11]研究顯示,老年非小細胞肺癌患者化療基礎上聯合卡瑞利珠單抗,可進一步降低血清腫瘤標志物水平,總有效率由35.00%增至55.00%。袁國盛等[12]研究表明,卡瑞利珠單抗聯合阿帕替尼治療中晚期肝癌患者,可有效延長生存期,且耐受性良好。本研究發現,卡瑞利珠單抗輔助治療結腸癌患者,疾病控制率由73.58%增至88.68%,且不良反應可控,是安全有效的治療方案。黃健等[13]研究顯示,結腸癌組織PD-1、PD-L1蛋白表達水平高于癌旁組織,且與TNM分期、浸潤深度、淋巴結轉移、分化程度、脈管侵犯等病理特征具有顯著相關性。因此,卡瑞利珠單抗應用于結腸癌患者,或可通過阻斷PD-1/PD-L1通路,增強機體對腫瘤抗原的免疫應答,呈現抗腫瘤活性。本研究顯示,治療后觀察組腫瘤標志物CEA、CCSA-2、CA199水平低于對照組(P<0.05),提示卡瑞利珠單抗對結腸癌的良好療效。
還有研究提出,卡瑞利珠單抗存在通過激動VEGFR2而引起血管內皮細胞活化并驅動血管瘤發展,誘發毛細血管增生癥的風險,其主要發生在體表皮膚,且3~6個月后相關癥狀會逐漸消失,并無遠期影響[14]。本研究觀察組患者盡管出現2例皮膚毛細血管增生癥,但整體治療效果良好,且治療后觀察組血清VEGF、VEGFR-2、Ang-2水平低于對照組(P<0.05)。VEGF是最強大血管生長因子,具有促進有絲分裂、調節血管通透性等功能,是腫瘤生長、浸潤的生物學標志;VEGFR-2是VEGF細胞膜受體,與VEGF結合后引發抗凋亡級聯反應,進而促進腫瘤血管內皮細胞增殖及血管形成[15]。Ang-2表達是腫瘤血管新生起始的強化因素,研究認為,Ang-2和VEGF協同作用于結腸癌血管生成[16]。上述研究提示,加用卡瑞利珠單抗或能通過降低VEGF、VEGFR-2、Ang-2水平發揮抗腫瘤血管新生的目的。分析主要是因結腸癌血管新生受VEGF、VEGFR-2、Ang-2等多個因子調控,而報道中卡瑞利珠單抗僅對體表VEGFR-2存在微弱激活作用,同時還有研究顯示,卡瑞利珠單抗能通過PD-1/PD-L1軸激活免疫細胞功能,調節免疫系統重編程并作用于腫瘤血管,促使其正常化,抑制VEGF、VEGFR-2、Ang-2等細胞因子異常生成,繼而發揮抗腫瘤血管新生作用。
此外,PI3K/Akt信號通路是重要的腫瘤惡性生物學行為調控通路,其能通過抑制細胞凋亡、下調腫瘤抑制蛋白p53表達而導致惡性細胞無限增殖,與結腸癌細胞增殖活性關系密切[17]。目前,以PI3K/Akt信號通路為靶點的靶向治療已成為腫瘤學研究熱點,石雪萍等[18]研究顯示,人參皂苷Rh2能通過調控PI3 K/AKT/GSK-3β信號通路誘導結腸癌細胞凋亡。本研究結果顯示,隨治療進行結腸癌患者血清PI3K、Akt水平降低,且觀察組降低更顯著,客觀說明卡瑞利珠單抗能進一步降低上述因子水平,發揮抗結腸癌細胞增殖作用。此機制結合現有研究分析可能是:B淋巴細胞刺激因子可激活PI3K/Akt信號通路[19],而通常情況B淋巴細胞、T淋巴細胞處于動態平衡,當加用卡瑞利珠單抗通過PD-1/PD-L1軸強效激活T淋巴細胞時,B淋巴細胞含量相對降低,間接調控血清PI3K、Akt水平[20]。但本研究作為臨床觀察研究,首次通過PI3K/Akt信號通路觀察加用卡瑞利珠單抗對結腸癌細胞增殖活性的影響,其具體機制尚未完全明確,仍需后期更多研究繼續探討。
綜上可知,卡瑞利珠單抗聯合mFOLFIRI方案治療結腸癌患者,可降低血管生長因子VEGF、VEGFR-2、Ang-2水平,抑制PI3K/Akt通路,降低惡性細胞增殖活性,療效顯著,且安全性高。

