子宮內膜癌患者宮腔鏡電切術治療后復發的危險因素分析
袁超群 馮艷曉 吳樂策
子宮內膜癌為臨床常見惡性腫瘤,好發于圍絕經期及絕經后女性,可引起陰道出血、月經紊亂等癥狀,嚴重降低患者生存質量,且近年來逐漸呈年輕化趨勢,備受臨床關注[1-2]。臨床隨訪發現,子宮內膜癌經手術后存在較高復發風險,不僅增加患者身心痛苦,還增大經濟負擔,故如何預防復發也是臨床對抗腫瘤的重點及難點。若能及早發現相關危險因素并加以干預,則對防治子宮內膜癌術后復發具有重要意義。鑒于此,本研究旨在分析宮腔鏡電切術治療子宮內膜癌后復發相關危險因素,為臨床防治策略制定提供重要參考。
1 資料與方法
1.1 一般資料
回顧性分析2018年10月至2020年10月于我院行宮腔鏡電切術治療的96例子宮內膜癌患者臨床資料。納入標準:均經病理檢查確診為子宮內膜癌;伴有陰道不規則出血癥狀;精神狀態正常;臨床資料完整;患者及家屬知情同意。排除標準:術前存在放化療史;伴有免疫、血液等系統疾病;合并其他惡性腫瘤;心肺功能難以耐受手術;存在嚴重感染性疾病。
1.2 方法
所有患者入院后均完善相關檢查,并予以宮腔鏡電切術治療:先使用10~12號擴宮棒打開患者宮口,在以1.5%甘氨酸溶液進行子宮充盈處理,膨宮壓力維持70 mmHg左右;待完全充盈后將10 mm電切鏡導入,仔細觀察病灶及周圍組織情況;之后依據情況選取5 mm電切割環以100 W的輸出功率切割子宮內膜病灶組織,切割深度為病灶下2~3 mm深度的子宮淺肌層;完成切割后止血退出宮腔鏡,術后常規抗感染等處理。所有患者術后進行長期隨訪,督促按時復查。術后復發標準為術后6個月內發現腫瘤復發或遠處轉移。術后依據復發情況將96例患者分為復發組和未復發組,收集兩組患者年齡、體質量指數、病理分期、病理分級、肌層浸潤深度、病理類型、腹腔細胞學檢查、基礎疾病史、腫瘤直徑等一般資料。先進行單因素分析,之后將具有統計學差異的變量納入多因素Logistic回歸模型,采用逐步回歸篩選變量,最終獲取宮腔鏡電切術治療子宮內膜癌患者后復發的獨立影響因素。
1.3 觀察指標
分析子宮內膜癌患者宮腔鏡電切術治療后復發相關危險因素。
1.4 統計學方法
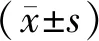
2 結果
2.1 術后復發情況
96例子宮內膜癌患者,術后出現復發23例,術后復發率為23.96%(23/96)。
2.2 影響子宮內膜癌術后復發的危險因素分析
兩組淋巴結轉移、病理分級、肌層浸潤深度、術后聯合激素類藥物情況及腫瘤直徑相比,差異有統計學意義(P<0.05)。見表1。
2.3 影響子宮內膜癌術后復發的多因素分析
有淋巴結轉移、病理分級G3、肌層浸潤深度≥1/2、術后未聯合激素類藥物及腫瘤直徑>2 cm是子宮內膜癌患者術后復發的高危因素(P<0.05,且OR>1)。見表2。
3 討論
子宮內膜癌發病機制復雜,臨床認為激素水平紊亂是誘發本病的重要因素,當患者體內無孕激素對抗時,雌激素可對子宮內膜造成持續刺激,促使子宮內膜長期處于過度增生狀態,進而增大子宮內膜癌風險[3]。此外,肥胖、糖尿病、遺傳等均與子宮內膜癌發病存在密切關系。宮腔鏡電切術是子宮內膜癌重要治療術式,具有創傷小、術后恢復快等特點,術中精細操作可最大程度減輕子宮內膜損傷,保留患者子宮功能,以改善患者生存質量[4-5]。但術后高復發成為困擾臨床的重點難題,若能早期明確危險因素,則有助于提高子宮內膜癌整體預后。
目前,臨床認為淋巴結轉移是術后復發的高危因素,子宮內膜癌最常見的轉移途徑則為淋巴結轉移,腫瘤細胞隨著淋巴液循環可被帶到匯流區淋巴結,并能以此為中心生長出同樣腫瘤組織,故一旦患者合并淋巴結轉移,則會增加手術清除難度,術后復發風險大[6-7]。本研究多因素分析發現,淋巴結轉移為術后復發高危因素,故術前精確診斷及術中完全清除病灶尤為重要。本研究多因素分析顯示,病理分級G3、肌層浸潤深度≥1/2、術后未聯合激素類藥物及腫瘤直徑>2 cm也是子宮內膜癌患者術后復發的高危因素。分析原因為,腫瘤病理分級G3期惡性程度高,肌層浸潤深度≥1/2、腫瘤直徑>2 cm則提示腫瘤組織對周圍正常組織侵襲較為嚴重,該類群體術后可能存在較高腫瘤細胞殘留風險,若不及時采取對應措施,則術后易出現復發[8]。術后未聯合激素類藥物也是影響術后復發的重要因素,子宮內膜癌為雌激素依賴性腫瘤,當體內雌激素水平較高時,可加快腫瘤組織增殖分化。因此,術后需及時輔以激素治療,如應用地屈孕酮等孕激素制劑,可直接作用于子宮內膜,拮抗雌激素活性,從而阻止子宮內膜增生,抑制腫瘤生長,進而降低術后復發風險[9]。
綜上所述,宮腔鏡電切術治療子宮內膜癌術后存在較高復發風險,臨床應重點關注合并有淋巴結轉移、病理分級G3、肌層浸潤深度≥1/2、腫瘤直徑>2 cm群體,并于術后積極進行激素輔助治療,以減少子宮內膜癌復發。

