經劍突肋緣下入路、胸腔鏡側胸入路在前縱隔腫瘤切除手術中的應用效果及術后疼痛和恢復情況分析
王 杰 盧家彬 楊世卿
前縱膈腫瘤多為良性,在患者符合手術適應癥的情況下,一般行手術切除病灶,以解除患者臨床癥狀。傳統開胸手術在胸骨正中做切口,以獲得良好的術野,充分顯露腫瘤界限,便于腫瘤的完全切除,但開胸手術創口大,術中出血量多,術后疼痛明顯,切口瘢痕明顯[1]。胸腔鏡手術創口小,能有效減少術中出血量,患者術后恢復快,與開胸手術相比,具有微創性優勢[2]。本文對比分別采用經劍突肋緣下入路、胸腔鏡側胸入路的前縱膈腫瘤切除術患者臨床資料,分析以上入路對患者術后疼痛及并發癥的影響,為臨床前縱膈腫瘤切除術的手術入路的選擇提供參考。
1 資料與方法
1.1 研究對象
將2017年01月至2021年01月間行前縱膈腫瘤切除術的95例患者納為研究對象,根據患者手術方式及入路,將其分為兩組,包括劍突組(經劍突肋緣下入路,n=44),側胸組(胸腔鏡側胸入路,n=51)。(1)納入標準:患者經胸部CT檢查明確為前縱膈腫瘤,檢查提示腫瘤病灶局限,與周圍組織界限清晰,可一次性切除;患者凝血功能、血生化、肺功能等均符合手術要求,可耐受手術;由資歷相當的主治醫生完成手術治療。(2)排除腫瘤較大,累及肺葉者;合并精神障礙者;合并其他惡性腫瘤者。
1.2 方法
1.2.1 劍突組手術方法 患者取仰臥位,行胸腔鏡劍突下入路前縱膈腫瘤切除術。行單腔氣管插管麻醉,常規消毒輔巾,于劍突下2~3 cm做一橫行切口,切口長度約為2 cm,作為觀察孔,術者手指緊貼劍突后,向上鈍性分離胸骨后間隙,分別在左右鎖骨中線肋弓下緣作0.5 cm切口,置入直徑為5 mm的Trocar,放入抓鉗與超聲刀,觀察孔內置入10 mm的Trocar,并置入30°胸腔鏡,充入CO2,建立人工氣腹。推開肺組織,顯露無名靜脈、膈神經以及心包之間的組織,利用超聲刀切開縱膈胸膜,沿縱膈胸膜自下而上切除心包旁、膈肌上方、雙側膈神經至無名靜脈之間區域的前縱膈脂肪組織,切斷胸腺靜脈,再行全胸腺切除,后將標本取出,期間注意仔細辨認并保護上腔靜脈、無名靜脈及膈神經。術后在觀察孔內放置引流管,縫合創面。
1.2.2 側胸組手術方法 患者取平臥位,雙腔氣管插管麻醉,取健側90°側臥位,將患側上肢上舉固定,常規消毒輔巾,根據術前影像學資料選擇手術側。在術側腋中線與腋前線之間的第6或7肋間切開一長為1 cm的切口,置入10 mm Trocar,并置入30°胸腔鏡,于腋前線第三或第四肋間切開一3~4 cm切口,作為操作孔,置入切口保護套,健側行單肺通氣,利用超聲刀逐步分離粘連,鈦夾夾斷滋養血管,常規全胸腺及其周圍脂肪切除。術后在觀察孔內置入引流管,縫合創面。
1.3 觀察指標
比較兩組手術相關指標,包括手術時間、術中出血量、術后引流量、術后住院時間、術后第一次下床活動時間。
比較兩組術后傷口疼痛程度及止痛藥使用情況。采用視覺模擬評分量表(VAS)評估兩組術后切口疼痛程度,VSA得分0~10分,其中0~3分為輕度疼痛、4~6分為中度疼痛、7~9分為重度疼痛,10分別為劇痛。VAS評分為7~10者給予肌注鹽酸哌替啶,4~6分者給予口服雙氯芬酸鈉,2~3分者給予口服塞來昔布,1分者無需應用止痛藥物。
比較兩組術后24 h血清疼痛應激指標:術后24 h,采集患者外周靜脈血,3000 r/min高速離心5 min,分離上層血清,采用酶聯免疫吸附法檢測患者疼痛應激指標,包括5-羥色胺(5-HT)、促腎上腺皮質激素(ATCH)以及前列腺素E2(PGE2)。試劑盒均購自南京森貝伽生物技術有限公司,嚴格按照試劑盒相關說明進行操作。
比較兩組術后并發癥,包括肺部感染、切口愈合不佳、胸腔積液、呼吸功能不全。
1.4 統計學方法
2 結果
2.1 兩組一般資料比較
兩組患者性別比例、年齡、BMI、腫瘤最大直徑、基礎性疾病以及術后病理類型比較,均無顯著性差異(P>0.05),見表1。

表1 兩組一般資料比較
2.2 兩組圍術期相關指標比較
劍突組與側胸組手術時間及術中出血量比較無顯著性差異(P>0.05),劍突組術后引流量、術后拔管時間、術后住院時間、術后第一次下床活動時間均顯著優于側胸組(P<0.05),見表2。
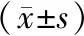
表2 兩組圍術期相關指標比較
2.3 兩組術后疼痛VAS評分及止痛藥物使用情況
術后12 h、24 h及72 h,兩組患者疼痛VAS評分均隨術后時間的推移呈依次下降趨勢(P<0.05),劍突組術后各時間段VAS評分均顯著低于側胸組同時間段水平(P<0.05),其術后止痛藥使用時間顯著短于側胸組(P<0.05),見表3~4。
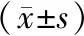
表3 兩組術后疼痛VAS評分
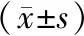
表4 兩組術后止痛藥物使用情況
2.4 兩組術后血清應激指標比較
兩組患者術后12 h、24 h及72 h,其血清應激指標5-HT、ATCH及PGE2水平均隨時間推移呈依次下降趨勢(P<0.05),而劍突組術后各時間段血清5-HT、ATCH及PGE2水平均顯著低于側胸組(P<0.05),見表5。
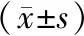
表5 兩組術后血清應激指標比較
2.5 兩組術后并發癥比較
劍突組與側胸組術后并發癥發生率比較無顯著性差異(P>0.05),見表6。

表6 兩組術后并發癥比較(例,%)
3 討論
早期前縱膈腫瘤可能無明顯異常表現,但隨著縱膈腫瘤體積的不斷增大,以及腫瘤生長部位,患者可能出現呼吸困難,胸腔積液,心悸甚至肌無力表現。前縱膈腫瘤一般為良性,故手術切除病灶是治療前縱膈腫瘤最常見的方式。傳統開胸手術常以縱劈胸骨作為手術入路,開胸手術的優勢在于可獲得廣闊清晰的手術視野,術者可輕松掌握腫瘤及其周圍毗鄰的解剖關系,進而完整地切除腫瘤,解除腫瘤相關臨床癥狀[3]。雖然開胸手術可有效保障腫瘤完全切除,但手術創傷性大,對于年老體弱,或機體承受能力差者并不適用。且隨著臨床醫療條件及技術的提高,患者對微創治療的需求也越來越強烈。胸腔鏡下前縱膈腫瘤切除較開胸手術而言,手術創口更小,術中出血量更少,患者術后疼痛程度更低,且術后恢復更快[4]。
但由于胸腔鏡下縱膈腫瘤切除的手術切口必然經過肋間,故無論是幾孔操作,均可能損傷肌肉及肋間神經,進而引起術后急性或慢性疼痛,影響術后恢復[5]。
胸腔鏡下前縱膈腫瘤切除術的手術入路是目前臨床研究的重點。本文對比胸腔鏡下劍突下肋緣入路及胸腔鏡側胸入路兩種入路方式在前縱膈腫瘤切除中的效果發現,劍突下肋緣入路及側胸入路在手術耗時、術中出血量中無明顯差異,但劍突下肋緣入路患者術后引流量更少,術后拔管時間、住院時間及第一次下床活動時間均明顯縮短,且術后72 h內疼痛程度更低。說明與胸腔鏡側胸入路相比,劍突下肋緣入路更利于患者術后恢復。側胸入路是臨床上最常使用的入路方式,但經側胸入路難以完全顯露膈神經、對側胸腺以及腫瘤周圍脂肪組織,不利于腫瘤的徹底切除,此外,側胸入路需行單肺通氣,進而增加肺部感染風險[6]。
謝澤華等[7]對比經劍突下與經右胸胸腔鏡下胸腺擴大切除術在重癥肌無力中的治療效果發現,經劍突下入路腫瘤切除更徹底,術后疼痛程度更低,患者術后恢復更快。于永濤等[8]研究發現,胸腔經劍突下切口入路與單側肋間切口入路相比,能有效減少老年縱膈腫瘤患者術中出血量,減輕患者術后疼痛程度。以上研究均與本文研究結論相似,證實經劍突下肋緣入路更具微創性優勢。
經劍突下肋緣入路無需在胸口做切口,進而避免對肋間神經及肌肉造成的損傷,最大程度上減輕術后疼痛,減少止痛藥物使用劑量及時間[9]。經劍突下肋緣入路能充分暴露手術術野,顯露腫瘤及其周邊解剖結構,利于腫瘤的徹底切除,并允許術者對雙側胸腔的探查,進而處理雙側病變[10],本文研究發現,經劍突下肋緣下入路者術后疼痛程度更低,止痛藥物使用時間更短,且術后72 h內血清應激指標5-HT、ATCH及PGE2水平均低于側胸組,提示經劍突下肋緣入路的安全性與微創性。
但經劍突下肋緣入路也存在明顯的局限性,該入路并不適用于處理胸膜及肺尖病變,且在左側胸腔內進行手術操作時,可能因手術器械壓迫心臟造成術后心律失常。故要求醫生熟練手術操作,掌握手術技巧,以避免以上情況。
綜上所述,胸腔鏡下經劍突下肋緣入路與側胸入路相比,在減輕患者術后疼痛,縮短患者術后恢復時間中更具優勢。

