非體外循環冠狀動脈搭橋術后發生心搏驟停的危險因素分析
劉 歡,陸小虎,劉 翔,王曉偉
(南京醫科大學第一附屬醫院心臟大血管外科,南京 210029)
冠狀動脈搭橋手術作為一種高風險手術操作,是冠心病治療的主要方法之一,其手術方式包括常規體外循環心臟停搏下冠狀動脈搭橋術(conventional coronary artery bypass,CCAB)及非體外循環下冠狀動脈搭橋術(off-pump coronary artery bypass,OPCAB)。雖然手術技術及相關設備不斷成熟,但是由于我國老齡化程度加重,術前有效藥物的應用也間接導致冠心病患者手術時機延遲,仍有一部分患者面臨術后發生嚴重并發癥甚至死亡的風險。研究表明,相對于CCAB,OPCAB可顯著降低患者圍手術期并發癥發生率及死亡率,且同樣適用于伴有左心功能不全的患者[1-2]。但臨床研究中,作者觀察到部分接受OPCAB的患者術后出現心搏驟停(cardiac arrest,CA),導致恢復期延長,并發癥發生率升高甚至死亡。目前關于OPCAB患者術后發生CA的相關臨床研究較為罕見,本研究旨在分析OPCAB術后發生CA的相關危險因素,為臨床治療提供參考。
1 資料與方法
1.1 一般資料
采用回顧性研究,選取2018年1月至2020年12月于本院心臟大血管外科接受OPCAB治療且在術后發生CA的患者25例(研究組),采用1∶4配對的方法,在同期接受OPCAB患者中選取未發生CA的100例為對照組(性別相同,年齡±2歲)。CA被定義為一種病理生理狀態,包括室速/室顫、心搏停止及無脈性電活動。接受OPCAB的患者在重癥監護室(ICU)接受嚴密監護及綜合治療時突發1次或多次CA即納入研究組。排除標準:(1)因術后短期內急性出血誘發的CA;(2)術后短期內因急性心肌梗死誘發的CA;(3)患者病情較重家屬放棄搶救導致的CA。本研究經本院倫理委員會批準。
1.2 方法
1.2.1觀察指標
通過查閱病歷資料,收集患者術前及手術相關臨床資料,比較研究組和對照組年齡、性別、美國紐約心臟病協會(NYHA)心功能分級、高血壓史、糖尿病史、心絞痛史、心梗史、冠狀動脈介入治療(PCI)史、吸煙史、飲酒史、腦梗死史、腎功能不全、頸內動脈狹窄、外周血管病變、冠狀動脈病變情況;術前心臟超聲檢查指標,包括左心房直徑(LAD)、左心室舒張末期直徑(LVDd)、左心室射血分數(LVEF)、合并左室舒張功能減退及室壁運動障礙情況;手術相關指標,包括手術時間、搭橋數目、搭橋方式。
1.2.2手術方法
所有手術均采用平臥位,常規靜脈吸入復合麻醉及氣管插管,開胸后以1 mg/kg行肝素化,常規取左側乳內動脈、大隱靜脈備橋血管,全靜脈搭橋僅取大隱靜脈,多動脈搭橋另取橈動脈備血管橋。常規先行左乳內動脈與前降支靶血管吻合,再吻合其他血管。依據患者升主動脈鈣化程度,采用側壁鉗或近端吻合器行大隱靜脈、橈動脈與升主動脈吻合,后再由近及遠行剩余病變靶血管的端側或序貫吻合。再血管化完成后使用冠狀動脈流量儀明確吻合效果,魚精蛋白中和肝素,止血、關胸。
1.2.3術后管理
所有患者術后均在插管狀態下入ICU行進一步治療,維持血流動力學和內環境穩定,定時檢測心肌標志物,監測生命體征及引流量。患者術后若突發CA,立即采用心肺復蘇(CPR)治療,同時積極明確病因,及時予以對癥處理,包括采用急診開胸探查、主動脈內球囊反搏(IABP)植入及體外膜肺氧合(ECMO)支持治療。
1.3 統計學處理
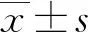
2 結 果
2.1 兩組臨床資料和手術情況比較
研究組室壁運動障礙發生率及術前LAD、LVDd均高于對照組,術前LVEF低于對照組,差異均有統計學意義(P<0.05);其余指標兩組間比較,差異均無統計學意義(P>0.05),見表1。

表1 兩組臨床資料和手術情況比較

續表1 兩組臨床資料和手術情況比較
2.2 OPCAB后發生CA危險因素的logistic多元回歸分析
將單因素分析中差異有統計學意義的變量納入logistic多元回歸分析,結果顯示,LVDd高[OR=1.141,95%CI(1.017,1.280),P=0.025]是OPCAB術后發生CA的獨立危險因素,而LVEF高[OR=0.942,95%CI(0.890,0.998),P=0.043]是保護因素。
3 討 論
據報道冠狀動脈搭橋術后發生CA的概率約3.4%[3]。CA是一種嚴重影響患者預后的并發癥,甚至可導致患者死亡。一旦出現CA,通過CPR可及時恢復心臟機電功能,可能避免心肌和冠狀動脈循環的不可逆性損傷。冠狀動脈搭橋術后發生CA可能與圍手術期心肌梗死相關,而后者常與手術技術及患者自身血管條件相關。當移植血管出現如血栓、吻合口狹窄、血管扭轉、痙攣,以及靶血管條件差會導致橋血管低流量、高阻力等問題,均可能誘發CA。同時術中再血管化不完全、心肌保護不佳、再灌注損傷及冠狀動脈微栓塞等原因也可能導致心肌梗死發生,通過手術技術的改進和完善、標準化的術中操作可以降低其發生率[4]。本研究因術中操作干擾因素多,不具有預測價值,已排除因術后急性心肌梗死導致的CA病例。另一方面,心功能不全也有可能誘發CA[5]。本研究結果表明,術前室壁運動障礙發生率、LAD、LVDd及LVEF在研究組和對照組間均有明顯差異,且logistic多元回歸分析結果顯示術前LVDd高是OPCAB后發生CA的獨立危險因素,而LVEF高是保護因素。這些指標均與患者術前心功能相關,進一步印證OPCAB后發生CA可能與心功能不全相關。
相較于CCAB,OPCAB避免了體外循環操作帶來的手術創傷和炎癥反應,逐漸成為冠狀動脈外科主流手術方式之一。施行CCAB時靜止的心臟和無血的操作視野可使再血管化操作更為確切[6],但OPCAB可降低新發房顫、心肌梗死、急性腎損傷、低心排血量、腦血管事件等并發癥發生率,并且能縮短氣管插管時間及ICU治療時間[7-8]。研究顯示,冠狀動脈搭橋術后死亡率隨LVEF降低出現明顯升高[9],對于低LVEF冠心病患者采用創傷更小的OPCAB方式更具有優勢,其對左心室功能影響更小[10]。諸多研究表明,OPCAB可安全用于左心室功能不全的冠心病患者,相對于正常心功能患者可獲得同等的搭橋質量和完全再血管化率[11]。但相較于LVEF正常患者,即使采用OPCAB方式,低LVEF患者仍面臨更高的心血管事件發生率和死亡率。
低LVEF作為CABG后重要的危險因素已被廣泛研究,LVDd作為在心功能評估時與射血分數同時獲取的指標,卻較少被用于風險評估中。事實上LVEF和左心室擴張程度密切相關,有研究表明低LVEF伴嚴重左心室擴張的患者相較于低LVEF伴正常或輕度左心室擴張的患者發生心源性猝死的風險明顯增加[12],左心室擴大高血壓人群中室性心律失常的發生率約為左心室正常者的5倍[13]。類似的,在冠狀動脈外科手術相關研究中也發現,CABG后左心室尺寸的改善和LVEF可以預測患者中期死亡率[14];也有學者認為,單純通過LVEF指標對CABG的手術風險與結果預測并不準確,應聯合左心室尺寸與LVEF進行綜合評估[15]。本研究結果也表明,LVDd和LVEF這兩項指標在患者術前評估中具有重要價值。
本研究不足在于病例數較少,相關影響因素納入不夠全面,后續仍需納入更多病例行更全面的前瞻性觀察研究。OPCAB手術對于需要外科治療的冠心病患者具有創傷小、恢復快、并發癥少等優點,但需要全面的術前評估,嚴格掌握手術適應證。尤其對于低LVEF合并左心室嚴重擴張的患者,應慎重選擇OPCAB,術后需要密切監護,維持水、電解質及酸堿平衡,預防CA發生,降低并發癥及死亡風險。

