達沙替尼聯合α-干擾素致嚴重的溶血性貧血分析*
桑 花,毛 琳,張紫嬋,劉 紅,周 鷺**
1 南通大學附屬醫院血液科,南通 226001;2 上海市寶山區吳淞中心醫院(復旦大學附屬中山醫院吳淞醫院)藥劑科,上海 201900
溶血性貧血(Hemolytic anemia,HA)是一種異質性疾病。由于異常的免疫反應攻擊自身的紅細胞,導致管內和管外的溶血,通常為原發性。繼發性HA 與感染、自身免疫性疾病、淋巴細胞增殖性疾病以及多種藥物有關。HA 發生的核心的病理機制是免疫耐受的異常和自身抗體的產生[1]。
慢性粒細胞性白血病(Chronic myeloid leukemia,CML)是一種克隆性的造血干細胞疾病。它的核心機制是獲得性的9 號和22 號染色體易位形成了BCR-ABL1 融合基因[2]。CML 的貧血可能與多種因素有關[3];但是CML 合并HA 非常少見。
達沙替尼,是一種小分子的酪氨酸激酶抑制劑(Tyrosine kinase inhibitor,TKI),通過抑制BCRABL1 來治療CML 和費城染色體(Philadelphia chromosome,ph 染色體)陽性的急性淋巴細胞白血病。它還能抑制一些脫靶激酶,例如c-KIT、TEC、SRC 等,其中一些激酶具有免疫功能[4]。研究表明,達沙替尼在體內能明顯降低Treg 水平,增強腫瘤抗原特異性的T 細胞反應。干擾素(Interferon-alpha,IFN-α)是一種免疫調節劑,它能夠下調BCR-ABL1的基因表達,激活多種轉錄因子,從而調節細胞增殖、成熟和凋亡[5]。除此之外,它還能通過免疫系統誘導CML 細胞的識別和清除[6]。
近年來TKI 聯合IFN-α 治療CML 慢性期患者獲得更深度的緩解[7];聯合治療還能夠清除T315I 突變[8]。因此2020 年歐洲白血病網(European Leukemia Net,ELN)指南推薦TKI 聯合IFN-α 作為CML 的一線治療[9]方案;但是聯合治療也可能會帶來許多副作用。
本研究報道了1 例少年CML 患者在達沙替尼聯合IFN-α 治療后發生了罕見的HA。此例可能為TKI 聯合IFN-α 治療CML 提供確切的臨床安全性警示。
1 病例摘要
患者,男,11 歲,因乏力伴腹脹1 周于2004 年至南通大學附屬醫院門診。查體示巨脾。血常規示白細胞125×109/L,其中中性粒細胞80%,血紅蛋白120 g·L-1,血小板950×109/L。骨髓涂片和流式檢測提示:慢性粒細胞白血病慢性期。染色體示46,xy,t(9,22)。PCR 檢測到BCR-ABL1(p210)融合基因。診斷為慢性粒細胞性白血病慢性期(Chronic phase,CP)。既往史無特殊。
由于經濟原因,初始治療選擇間斷使用羥基脲和IFN-α。2016 年5 月,患者病情進入加速期。骨髓涂片提示原始細胞為13%,嗜堿性粒細胞為16%。患者開始服用尼羅替尼0.4 g bid。4 個月后,BCRABL1 表達水平從100%(IS)降至20.64%(IS)。然而,轉氨酶升至630 U·L-1。在經過護肝治療和尼羅替尼減量之后沒有明顯改善。因此從2016 年11 月開始,換用達沙替尼0.1 g qd。一個月后,轉氨酶水平基本恢復正常。然而,BCR-ABL1 表達水平從20.64%(IS)升至23.64%(IS)。達沙替尼的劑量從0.1 g qd 升至0.14 g qd。3 個月后,BCR-ABL1 表達水平從23.64%(IS)降至2.78%(IS);但是6 個月后再次升至14.9%(IS)。基因檢測未檢測到ABL 激酶區的突變。2017 年10 月達沙替尼的劑量進一步升至0.15 g qd。遺憾的是,BCR-ABL1 表達水平沒有下降反而繼續上升至22.1%(IS)。再次進行基因檢測,仍未找到ABL 激酶區的突變(見圖1)。血常規提示,在換用達沙替尼后該患者的淋巴細胞數量逐漸上升,血小板逐漸下降。在達沙替尼治療期間,患者感到乏力;但沒有胸悶氣急的表現。
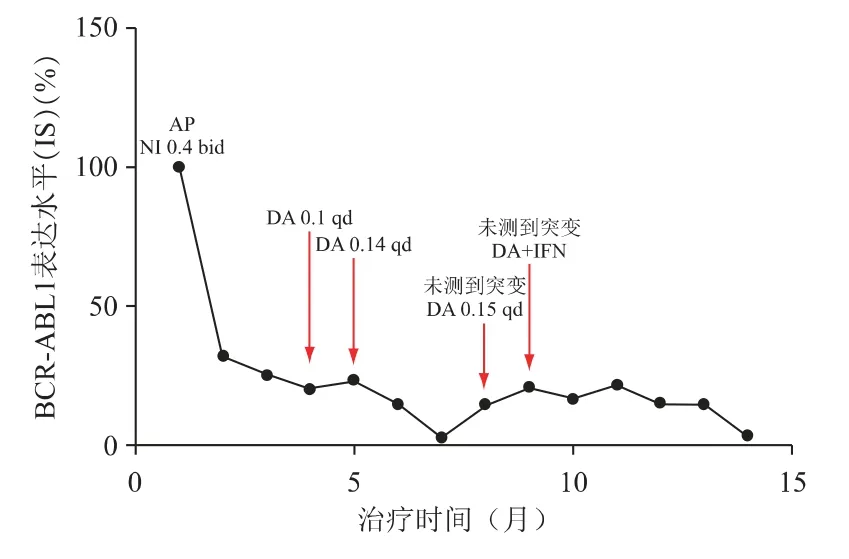
圖1 患者TKI 開始治療后的BCR-ABL1融合基因表達水平
2018 年2 月,在達沙替尼0.14 g qd 治療的基礎上,臨床給予患者加用每天IFN-α 300 萬單位、每月連用7 天的方案。6 個月后,該患者的BCRABL1 表達從22.1%(IS)降至3.46%(IS)。然而,從2019 年3 月開始患者出現了嚴重的血性胸水,血紅蛋白明顯下降,伴隨著間接膽紅素和網織紅細胞明顯升高。此狀符合溶血性貧血的表現(見圖2)。
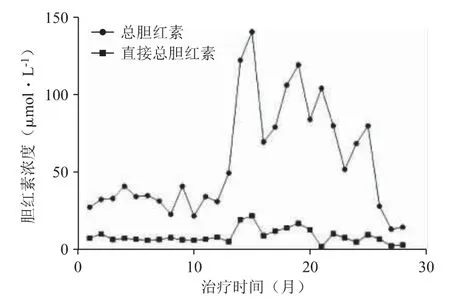
圖2 在使用達沙替尼聯合干擾素治療后患者總膽紅素和直接膽紅素的濃度水平
臨床立刻停止了上述聯合治療,并加用潑尼松50mg qd 免疫抑制治療。半個月后,該患者的間接膽紅素從102.8mmol·L-1降至60.3mmol·L-1。在停止聯合治療后4 個月,該患者的間接膽紅素降至正常水平。
2 討論
CML 是一種老年性疾病[10]。兒童和青少年非常少見;占兒童和青少年白血病的2%~3%[11]。本例患者在11 歲發生CML,具有較為侵襲性的臨床和生物學表現,治療效果欠滿意,符合兒童、青少年型CML 的特點[12]。該患者整個治療過程中未發現ABL1 激酶區的突變,其耐藥可能與BCR-ABL1 內含子的突變或者非BCR-ABL1 區域的突變有關。
溶血性貧血診斷標準包括:①血紅蛋白水平達貧血標準;②至少符合以下一條:網織紅細胞百分比>4%或絕對值>120×109/L;結合珠蛋白<100mg·L-1;總膽紅素≥17.1 μmol·L-1(以非結合膽紅素升高為主)。該患者貧血,正常細胞型,網織紅細胞明顯增高,乳酸脫氫酶增高,膽紅素增高,以間接膽紅素增高為主,符合溶血性貧血的診斷標準。
CML 合并HA 非常少見。Hamamyh T 等[13]回顧了1952 年至2018 年共54 例CML 合并HA 的病例報告:幾乎所有合并HA 的患者均為CML 慢性期的患者;這些患者可以分為移植和非移植患者兩類。對于非移植患者,多數都與干擾素的使用有關。這與本案例相似。本例患者在達沙替尼聯合干擾素-α治療1 年余發生了溶血性貧血,停用后溶血癥狀消失;并且該患者在2016 年開始使用TKI 之前,有長達12 年的間斷使用干擾素-α 單藥的病史,并沒有發生溶血。根據Karch 和Lasagna 評價方法,故認為該患者的溶血與達沙替尼聯合干擾素-α 治療很可能有關。
達沙替尼的常見副作用包括液體潴留、腹瀉、頭痛、皮疹、肌肉骨骼疼痛、惡心、疲勞、肌痛、嘔吐和肌肉炎癥等;其中胸水是其最為特征性的副作用。干擾素最常見的副作用是發熱、疲勞等反應,其它可能存在的不良反應有輕度的骨髓抑制、頭痛、肌痛、關節痛、食欲不振、惡心和脫發等。達沙替尼聯合干擾素導致溶血性貧血的不良反應鮮有報道。本案例的發生可能與兩藥聯用后對機體T 細胞免疫的異常激活有關。因此,該患者不適宜達沙替尼和干擾素聯合用藥。該案例提示:對于達沙替尼聯合干擾素治療CML(CP),需要密切監測患者的血常規、肝功能、網織紅細胞水平,以便及時發現HA。一旦發生,需立即停藥,嚴重的情況可以使用激素治療。
多藥耐藥且找不到明確的BCR-ABL1激酶區突變的CML 患者的治療,是目前的臨床治療的難點。新一代的TKI 制劑,臨床試驗或者異基因造血干細胞移植都是可選擇的治療方案。除此之外,TKI聯合干擾素-α 的治療可能會對部分患者有效;但是兩藥聯用可能會帶來許多副作用,需要引起臨床的重視。

