瑞馬唑侖聯合舒芬太尼抑制無痛人工流產術擴張宮頸體動研究
陳秋紅,劉博文,楊文明,胥露露
南昌大學第一附屬醫院,江西 南昌 330006
人工流產術是婦科常見的終止早期妊娠的方法,術中需置入窺陰器、擴張宮頸、刮吸子宮內膜等操作,對患者身心均可造成嚴重的創傷。隨著舒適化醫療理念不斷深入,無痛診療技術的日漸成熟,越來越多的患者更傾向于在無痛狀態下完成人工流產術。目前,丙泊酚廣泛運用于無痛人工流產術麻醉,但其注射痛明顯,呼吸、循環抑制作用較強[1]。瑞馬唑侖(CNS7056)是一種超短效新型鎮靜藥物,具有安全、高效的鎮靜效果,且對呼吸循環影響輕微,幾乎沒有注射痛等特點[2]。因此,本研究采用瑞馬唑侖聯合舒芬太尼麻醉方案用于無痛人工流產術,測定抑制擴張宮頸體動反應瑞馬唑侖的ED50及95%CI,為臨床用藥提供參考。
1 資料與方法
1.1 一般資料
本研究選取2021 年11 月至2022 年2 月南昌大學第一附屬醫院自愿要求行無痛人工流產術患者53 例,分為無分娩史患者組(N1 組,n=29)和有自然分娩史患者組(N2 組,n=24)。兩組患者組內有體動反應和無體動反應、患者年齡、體質量指數(BMI)、妊娠天數和手術時間均差異無統計學意義,見表1。
表1 兩組患者一般情況比較()

表1 兩組患者一般情況比較()
注:與同組內有體動反應比較,aP>0.05。
1.2 選取標準
(1)納入標準:①美國麻醉醫師協會(ASA)分級為I~Ⅱ級;②符合《婦產科疾病診斷標準》[4]中妊娠的相關診斷標準;③輔助檢查提示宮內早孕,符合人工流產手術適應證;④不存在麻醉相關禁忌證;⑤患者及家屬均知情研究目的并簽署麻醉知情同意書。(2)排除標準:①對苯二氮類藥物及相關成分過敏者;②精神分裂癥或嚴重抑郁狀態患者;③BMI>30 kg/m2、阻塞性睡眠呼吸暫停低通氣綜合征(OSAHS)患者;④近2 周有急性上呼吸道感染,哮喘急性發作期;⑤存在嚴重婦科疾病或異位妊娠患者;⑥合并重要臟器嚴重功能障礙者。
1.3 研究方法
所有患者術前常規禁食8 h、禁飲2 h,均不予術前用藥。入室后取膀胱截石位,開放外周靜脈通道,鼻導管吸氧3 L/min,連接心電監護監測心電圖(ECG)、無創血壓(NBP)、血氧飽和度(SpO2)等生命體征。緩慢推注枸櫞酸舒芬太尼注射液(江蘇恩華藥業股份有限公司,國藥準字H20203650,規格:1 mL∶50 μg)0.1 μg/kg,隨后靜脈注射序貫法對應劑量的注射用甲苯磺酸瑞馬唑侖(江蘇恒瑞醫藥股份有限公司生產,國藥準字H20190034,規格:36 mg/支),60 s 內推注完畢,2 min 后開始手術。若麻醉期間收縮壓(SBP)≤80 mm Hg 或低于基礎值20%,靜脈注射麻黃堿6 mg;若心率(HR)≤50 次/min,靜脈注射阿托品0.5 mg;當SpO2≤90%或呼吸頻率(RR)≤10 次/min,則予輔助通氣。
1.4 觀察指標
觀察和記錄所有患者入室時(T0)、麻醉誘導后2 min(T1)、擴張宮頸結束時(T2)及手術結束時(T3)各時間點的平均血壓(MAP)、HR、SpO2等血流動力學指標及Ramsay 鎮靜評分。記錄所有患者靜脈注射痛、術中知曉、惡心嘔吐等不良反應發生情況。
1.5 序貫方法
采用改良Dixon 序貫法,根據預實驗及一系列研究結果[5-7]選擇瑞馬唑侖的起始劑量為0.2 mg/kg,按0.05 mg/kg 梯度等差值增減,擴張宮頸時出現體動反應則為陽性反應則下一例患者的瑞馬唑侖劑量增加1 個梯度,若出現陰性反應則下一例減少1 個梯度。陽性反應標準:患者有任意肢體運動,皺眉或Ramsay 評分<5 級。Ramsay 鎮靜評分標準。1 級:清醒,焦慮、不安或煩躁;2 級:清醒,患者合作、定向力良好或安靜;3 級:清醒,患者僅對命令有反應;4 級:睡眠,患者對叩眉或強烈刺激快速反應;5 級:睡眠,患者對叩眉或者強烈刺激反應遲鈍;6 級:睡眠,患者對叩眉或者強烈刺激無反應[8]。若手術過程中出現影響操作的體動反應,酌量給予丙泊酚乳狀注射液(阿斯利康制藥有限公司生產,批 號X20014A,規格:20 mL∶200 mg)25~50 mg鎮靜補救,直至滿足手術需求,當出現8 個拐點時,研究終止。
1.6 統計學方法
采用SPSS 17.0 統計學軟件進行數據分析。計量資料以表示。組間比較采用獨立樣本t檢驗,組內比較采用重復測量方差分析。采用概率單位Probit 回歸分析法計算ED50及95%CI,用GraphPad Prism 5 軟件制作序貫試驗圖。P<0.05 為差異有統計學意義。
2 研究結果
2.1 不同時間點患者血流動力學變化及鎮靜評分的比較
同一組內有體動反應患者與無體動反應患者相比較,T1 時刻Ramsay 鎮靜評分均明顯要低,差異有統計學意義(P<0.01);與T0 比較:N2 組中有體動反應患者T1、T2 時刻MAP 均明顯降低(P<0.05),T3 時HR 明顯下降(P<0.05),但下降幅度均在安全范圍內;N1 組中有體動反應患者T2 時SpO2明顯降低(P<0.05),但無需干預;所有患者T1、T2、T3 時刻Ramsay 鎮靜評分明顯升高(P<0.01),差異有統計學意義。見表2。
表2 血流動力學及鎮靜評分在不同時間點的變化情況()
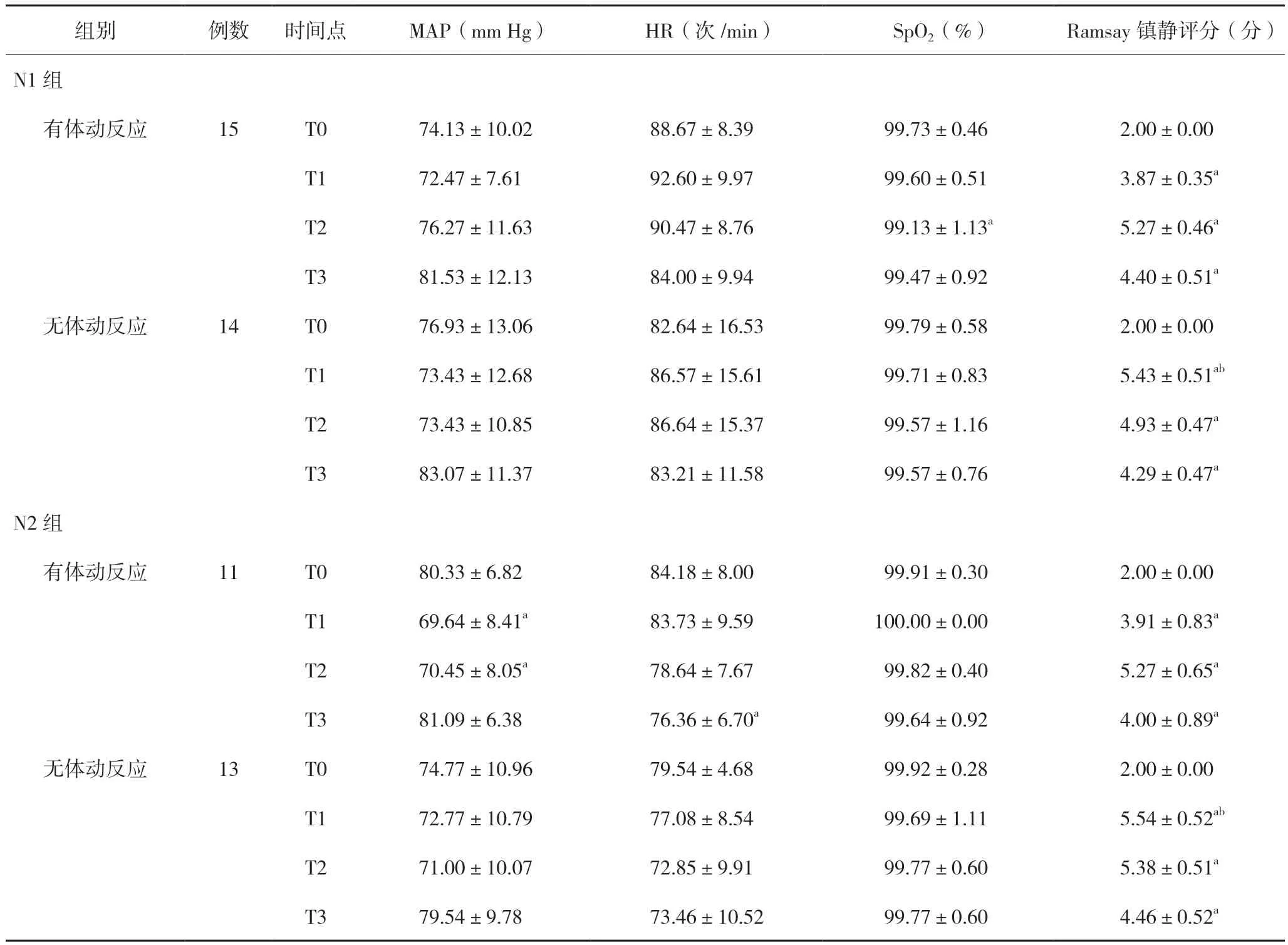
表2 血流動力學及鎮靜評分在不同時間點的變化情況()
注:組內各時間點與T0比較,aP<0.05;同組有體動反應患者與無體動反應患者比較,bP<0.05。
2.2 不良反應記錄
所有患者未見明顯注射痛、胸壁強直、術中知曉、頭暈頭痛等不良反應;與術前基礎值T0 比較,N1 組給藥后有1 例血壓下降超過基礎值20%;1例有呃逆;1 例有嘔吐反應。N2 組有1 例患者術中SpO2降至93%,自行恢復至正常水平;2 例出現呃逆;1 例出現嘔吐反應。
2.3 瑞馬唑侖聯合舒芬太尼抑制無痛人工流產術擴張宮頸體動反應的ED50、95% CI
本研究N1 組完成8 個折返時,陽性反應患者15 例,陰性反應患者14 例。瑞馬唑侖抑制無分娩史患者行無痛人工流產術擴張宮頸體動的ED50為0.21 mg/kg,95%CI0.17~0.25 mg/kg(見圖1)。
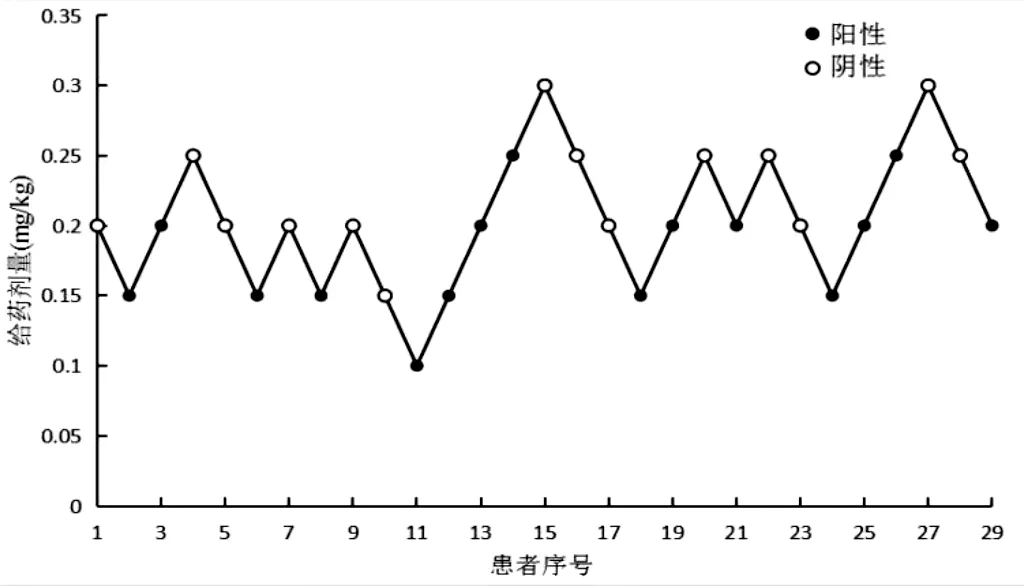
圖1 無分娩史29例改良序貫試驗圖
N2 組完成8 個折返時,陽性反應患者11 例,陰性反應患者13 例。瑞馬唑侖抑制有分娩史患者行無痛人工流產術擴張宮頸體動的ED50為0.14 mg/kg(95%CI0.11~0.17 mg/kg)(見圖2)。
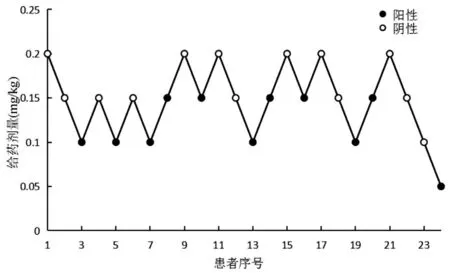
圖2 有分娩史24例改良序貫試驗圖
3 討論
無痛人工流產術常用于意外妊娠的補救,也用于因疾病不宜繼續妊娠、預防先天性畸形或遺傳性疾病而需終止妊娠者。手術時間較短,但術中部分手術操作可引起機體強烈不適感,甚至導致嚴重并發癥[9]。其中,擴張宮頸通過刺激宮頸體旁神經叢而引起患者劇烈疼痛和不適,患者疼痛敏感性和患者宮頸松弛度密切相關,而宮頸的松弛程度又和患者既往是否有自然分娩史緊密相連。所以,本研究將患者分為無分娩史組和有自然分娩史組進行研究,以提高研究結果的精確度。從手術開始至進行擴張宮頸操作的時間間隔約為60 s,該過程中往往不需額外追加藥物。因此,可以根據擴張宮頸時患者是否有體動來反映麻醉藥物用量是否足夠[10]。
瑞馬唑侖是一種新型超短效苯二氮類藥物,它作用于中樞γ-氨基丁酸(GABAa)受體的GABA位點,使氯離子通道開放,氯離子通透性和內流增加,引起神經細胞膜超極化從而產生鎮靜催眠作用[11]。瑞馬唑侖可通過體內的非特異性血漿酯酶迅速水解為唑侖丙酸(CNS7054),而瑞馬唑侖對GABAa 受體的親和力是唑侖丙酸的320~410 倍,所以瑞馬唑侖的代謝產物幾乎不具有藥理活性[12-14],因此,瑞馬唑侖具有起效快,代謝迅速,長時間輸注無蓄積作用,不依賴肝腎代謝,能被氟馬西尼特異性拮抗等藥理特性,尤其適用于快節奏的手術室外無痛診療麻醉[15]。目前已有研究證實,瑞馬唑侖用于無痛人工流產術麻醉安全性較高,相較于丙泊酚具有無注射痛、血流動力學穩定、蘇醒質量佳、不良反應發生率低等優勢[5-6]。因此,本研究擬探討瑞馬唑侖聯合舒芬太尼應用于無痛人工流產術麻醉,并測定抑制擴張宮頸時體動的瑞馬唑侖的ED50。
改良序貫法是臨床研究藥物ED50最常用的經典方法之一[16-17]。本研究結合預試驗研究結果和相關研究報道[5-7],選定瑞馬唑侖起始劑量為0.2 mg/kg,相鄰患者按劑量梯度為0.05 mg/kg 等差值增減,兩組均直至出現8 個折返則終止研究。
預實驗研究發現,單純使用瑞馬唑侖雖鎮靜良好,但術中體動明顯,麻醉深度不能滿足手術需求,考慮原因在于瑞馬唑侖具有鎮靜而無鎮痛作用,尚不能抑制擴張宮頸、宮內操作等刺激引起的疼痛不適,所以臨床上常復合鎮痛藥應用于無痛人工流產術,因此,本研究采用瑞馬唑侖聯合舒芬太尼麻醉方案,根據兩者協同作用,可減弱手術應激反應,提高患者的耐受性。研究結果發現,既往有分娩史患者瑞馬唑侖的ED50明顯小于無分娩史患者,原因在于有分娩史患者宮頸口和宮頸管直徑相比于無分娩史患者均較寬,吸具可順利通過宮頸管,減少擴張宮頸的需要,故有分娩史患者使用藥物劑量低于未生育患者。另一原因也在于無分娩史患者對疼痛較敏感,術中出現疼痛視覺模擬評分(VAS)>5 分的風險較有分娩史患者高出25%,所以無分娩史患者需較深的麻醉深度以抑制疼痛應激反應,所需的瑞馬唑侖劑量相應增大,這與本研究結果也相一致。研究還發現瑞馬唑侖聯合舒芬太尼麻醉方案鎮靜效果良好,患者血流動力學穩定,53 例患者中僅1 例患者血壓下降幅度超過20%,1 例患者SpO2下降到93%,自行恢復到正常水平,臨床安全性較高,這與臨床前期研究結果相一致。
綜上所述,瑞馬唑侖聯合0.1 μg/kg 舒芬太尼用于無痛人工流產術麻醉時安全有效,無分娩史患者和有分娩史患者抑制擴張宮頸體動的瑞馬唑侖ED50分別為0.21 mg/kg(95%CI0.17~0.25 mg/kg)和0.14 mg/kg(95%CI0.11~0.17 mg/kg),且有分娩史患者ED50 明顯小于無分娩史患者,所以無痛人工流產術麻醉誘導時應根據患者既往生育史酌情用藥,為臨床合理用藥提供參考。

