依托泊苷方案對兒童急性髓系白血病的療效及預后影響因素分析
胡海輝
急性髓系白血病(AML)是一種來源于骨髓的惡性異質性白血病,其惡性程度較高,病死率為70%~80%,且病情盡快發展極快[1-2]。如不能及時治療,其生存時間不足半年。AML可發生與任何年齡,無性別差異,其中兒童病患較常見。AML患兒在初診時體內一般會有20%以上的白血病細胞,經有效治療后,機體內的白血病細胞減少到5% 以下,無浸潤性骨髓現象,血象也基本恢復正常[3-5]。目前治療AML方案和藥物較多,依托泊苷方案較常用。目前依托泊苷方案中主要以米托蒽醌、依托泊苷、阿糖胞苷藥物為主,其臨床獲得認可,有利于預后。但AML患兒治療預后與諸多因素有關,不僅僅包括治療方案,還有其他因素如免疫力、年齡等。分析影響AML患兒預后顯著尤為重要。本文對醫院2017年6月~2019年6月診治的AML患兒作為依托泊苷方案治療對象,分析其治療效果和預后因素,現報告如下。
1 資料與方法
1.1 一般資料
選擇醫院2017年6月~2019年6月診治的AML患兒69例作為研究對象。納入標準:①符合《兒科學》中關于AML診斷標準;②7~15歲患兒;③病案信息完整;④溝通能力正常;⑤家屬和患兒配合。排除標準:①急性早幼粒細胞患兒;②自體干細胞或異體干細胞移植患兒;③骨髓癌患兒;④對治療藥物過敏的患兒;⑤自閉癥患兒;⑥病理性黃疸患兒。根據治療方案不同分為對照組和治療組,分別為33例和36例。對照組男性18例,女性17例,年齡7~15歲,平均(11.97±1.05)歲。治療組,男性19例,女性17例,年齡8~14歲,平均(11.91±1.04)歲。兩組患兒年齡和性別差異比較無統計學意義(P>0.05),具有可比性。
1.2 方法
治療方法:對照組患兒接受姑息治療,羥基脲、輸血等治療,連續治療14 d。治療組患兒接受依托泊苷方案治療,米托蒽醌針5 mg(m2·d),連續治療3 d;依托泊苷針1000 mg(m2·d),連續治療5 d;阿糖胞苷針1000 mg·m2·d,連續治療14 d。
基礎信息:使用問卷調查方法調查患兒的性別、染色體核型、CD34細胞表達情況、白細胞(WBC)水平、病因、Charlson合并癥指數(charlson complication index,CCI)評分、血小板計數(PLT)水平、乳酸脫氫酶(LDH)值、骨髓原始細胞比例、治療方案。
染色體核型參考熒光原位雜交(FISH)法檢測,分為低危核型、標危核型和高危核型。在治療前抽取患兒肘靜脈血8 ml,離心處理后使用全自動生化分析儀檢測WBC、PLT、LDH。使用免疫組化法檢CD34細胞表達情況。使用定量RT-PCR法檢測骨髓原始細胞比例。采用Charlson合并癥指數(charlson complication index,CCI)對患兒合并癥進行評價。
臨床療效:參考《血液學診斷與療效》標準對患兒治療效果進行評定,主要評價指標是完全緩解。隨訪1年統計兩組患兒生存時間,作為評價臨床療效的指標之一。
1.3 評價指標
比較兩組患兒臨床療效,分析影響患兒預后的單因素和多因素。
1.4 統計學方法
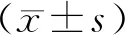
2 結果
2.1 兩組患兒臨床療效比較
治療組(36例)患兒中完全緩解30例(83.33%)。對照組(33例)患兒中完全緩解23例(69.70%)。治療組患兒生存時間(10.57±0.29)個月,對照組患兒(8.95±0.23)個月。治療組患兒完全緩解率和生存時間均大于對照組(P<0.05),見圖1。
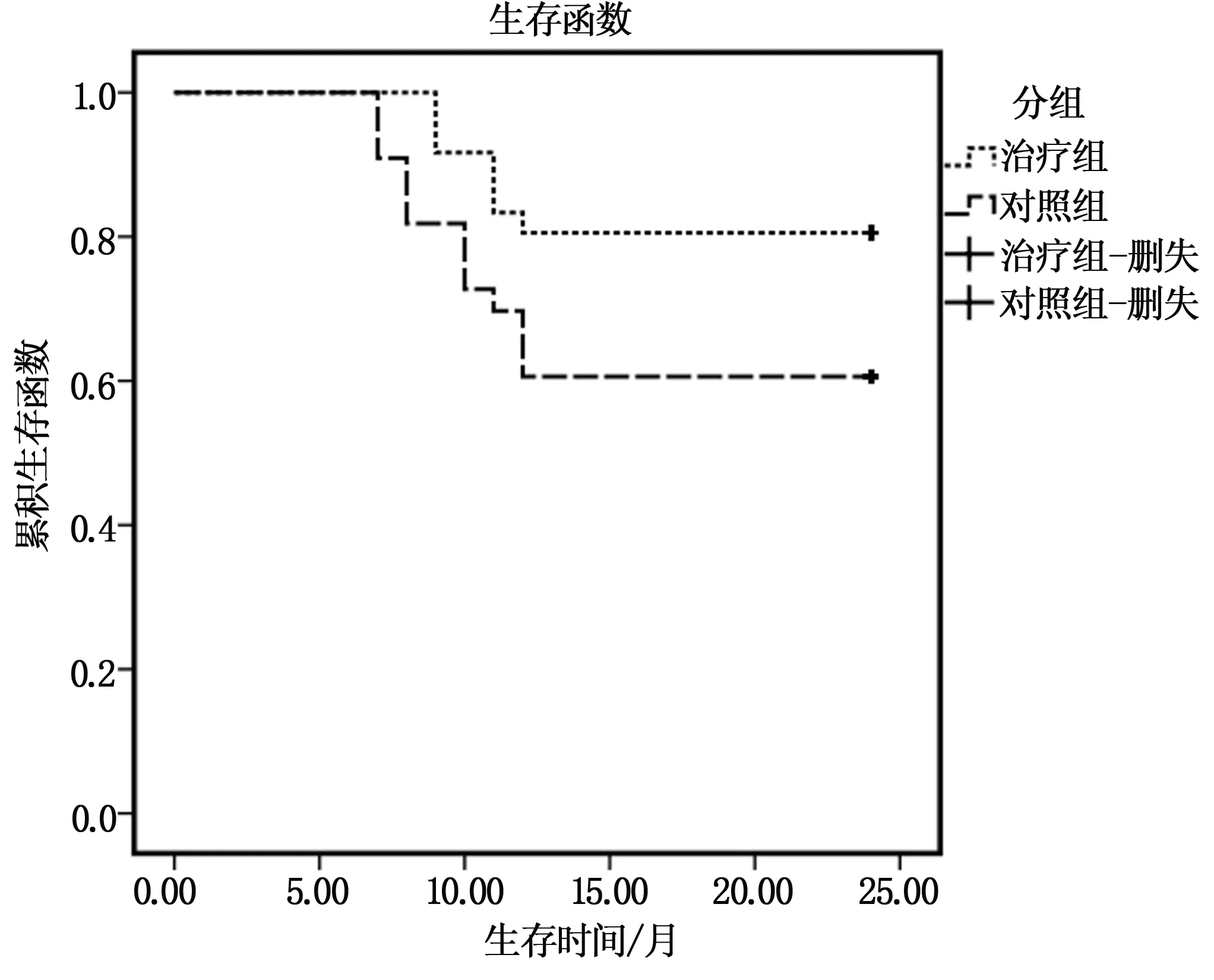
圖1 生存曲線圖
2.2 影響AML患兒預后單因素分析
經2.1結果可知,完全緩解53例,未完全緩解16例。經單因素分析發現,CCI評分、WBC、染色體核型、治療方案差異比較有統計學意義(P<0.05),而性別、年齡、CD34細胞表達情況、病因、PLT水平、LDH值、骨髓原始細胞比例情況差異比較無統計學意義(P>0.05),見表1。
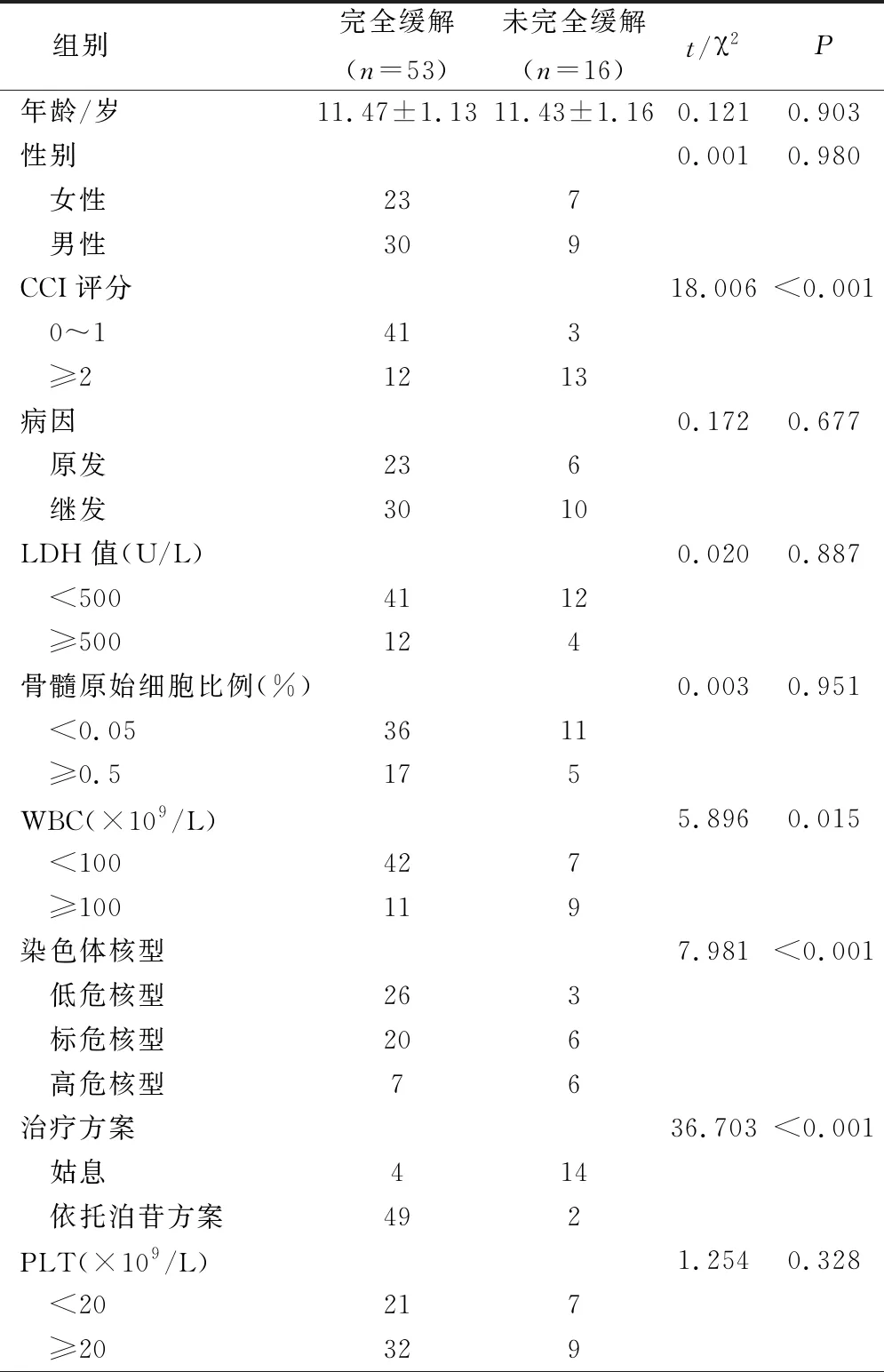
表1 影響AML患兒預后單因素分析/例
2.3 影響AML患兒預后因素Logistic分析
將表1中有統計學意義的因素“CCI評分、WBC、染色體核型、治療方案”進行賦值并作為自變量(X)(表2),將其納入Logistic中,因變量(y)為是否完全緩解,結果顯示CCI評分≥2分(OR=2.125,95%CI=1.382~3.678)、WBC≥100×109/L(OR=2.270, 95%CI=1.409~4.118)、高危核型染色體核型(OR=6.317,95%CI=1.762~20.127)是影響AML患兒預后的獨立危險因素(P<0.05),見表3。

表2 賦值表
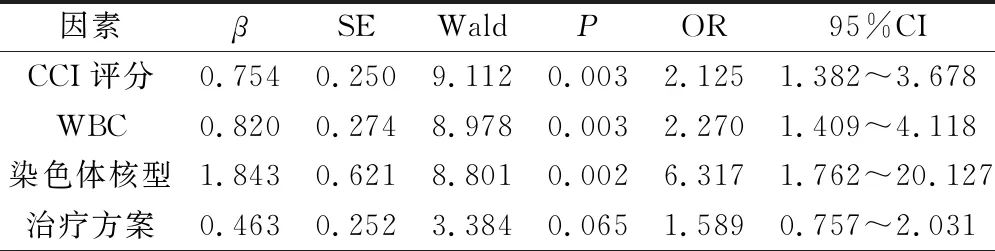
表3 影響AML患兒預后因素Logistic分析
3 討論
米托蒽醌、依托泊苷、阿糖胞苷藥物共同組成了依托泊苷治療方案。依托泊苷是一種氨基醌類藥物,是細胞周期非特異性廣譜抗腫瘤藥物,現已廣泛用于實體瘤和復發難治性白血病的治療,與米托蒽醌、阿糖胞苷藥物無較差性耐藥[6-7]。米托蒽醌嵌插型抗癌藥物,可用于治療惡性腫瘤。阿糖胞苷是治療白血病常用藥物之一。三藥聯合使用可用過代謝產生自由基,殺傷腫瘤細胞,且能協同起到抗腫瘤的療效。白血病是一種異質性惡性克隆疾病,是造血干細胞突變引起的造血系統的惡性腫瘤。臨床主要表現為異常細胞在骨髓及其他造血組織中惡性增殖[8-10]。隨著疾病發展,惡性細胞會浸潤導其他組織,導致骨髓中正常造血功能受到抑制。AML是白血病中常見惡性腫瘤,是一種分化受阻于髓系干細胞的一種異質性白血病,其特點較明確,是惡性克隆性白血病干細胞無顯著增殖并且顯著損傷免疫細胞[11-12]。AML臨床主要表現為白細胞和血小板增多或減少。AML生存期較短,生存率較低,60歲以上 的患者治愈率不足20%,小于60歲的患者其治愈率為35%~40%。最近幾年隨著治療方法發展,新技術和新藥的出現,其治療效果獲得較大提升。以往研究認為[13],AML療效和很多因素有關,且影響預后的因素相互關聯、相互影響,包括臨床特點、形態學和免疫學等等。預后因素之間的相互影響是指預后好的指標與其他預后不好的因素結合也會導致預后因素不好[14]。最近幾年大量關于預后指標出現,使得AML治療越來越根據預后危險因素進行分層治療,有利于患者康復。
本文研究結果顯示,接受依托泊苷治療方案治療的治療組患兒的完全緩解率和生存時間較單純接受姑息治療的對照組患兒優佳。依托泊苷治療方案具有廣譜抗腫瘤作用,能阻止細胞進入分裂期,作用于S1和S2期細胞,從而保證患兒安全度過骨髓抑制期,進而提升了完全緩解率,延長了患兒生存時間。CCI評分≥2分、WBC≥100×109/L、高危核型染色體核型是影響AML患兒預后的獨立危險因素。CCI評分主要是對合并癥進行評定,2分及以上預示死亡風險大。CCI評分≥2分是影響AML預后獨立危險因素很可能與患兒常合并心、肝、肺等重要器官功能障礙有關。嚴重性的合并癥會導致機體對藥物清除力降低的同時影響機體抵抗力。WBC是評價機體炎癥反應重要指標,WBC≥100×109/L說明出診時患兒機體外周血白細胞水平顯著升高。WBC≥100×109/L時可能會出現高白細胞綜合征,增加血液粘度,導致血栓形成,進而促使患兒出現呼吸困難和缺氧等狀態,極容易誘導患者在治療期間出現顱內出血和肺功能障礙,進而影響治療預后,促使患兒早期死亡[15]。染色體核型是與AML預后的相關重要因素,約有60%的患者伴有染色體核型異常。染色體核型在AML預后中起到非常重要意義。細胞遺傳學通過染色體核型分析將AML患兒分為低危核型、標危核型、高危核型例數分別是26例、20例和7例。預后相同的核型的患兒在分子生物水平和治療過程中具有高度異質性。高危核型惡性化程度嚴重,患兒在接受治療中很難獲益。
綜上所述,依托泊苷方案治療兒童急性髓系白血病能明顯延長患兒生存時間,提升預后。臨床在治療前要重視觀察CCI評分≥2分、WBC≥100×109/L、高危核型染色體核型患兒,制定個性化治療方案,以提升預后。

