5種營養篩查量表對腫瘤患者營養不良的診斷價值
——網狀Meta分析
張楠 傅譽 顏萍
(新疆醫科大學護理學院,新疆 烏魯木齊 830000)
腫瘤患者是最易患營養不良的群體之一,其中至少20%患者的死因與營養不良有關[1]。營養不良及機體高消耗狀態直接影響腫瘤患者的治療效果,甚至預后[2]。營養篩查是解決患者營養不良問題的基礎,也是營養支持療法的第一步[2]。目前,臨床上已用于營養不良篩查的工具有主觀綜合評價法 (subjective global assessment,SGA)、患者主觀綜合評價法 (patient-generated subjective global assessment,PG-SGA)、簡略版患者主觀綜合評價法 (patient-generated subjective global assessment short form,PG-SGA SF)、營養不良通用篩查工具 (malnutrition universal screening tool,MUST)、營養不良篩查工具 (malnutrition screening tool,MST)、營養風險篩查 (nutritional risk screening,NRS-2002)及營養危險指數(nutritional risk index,NRI)等。SGA和PG-SGA是臨床中應用廣泛并具有良好信效度的惡性腫瘤患者營養不良風險篩查工具。有學者[3-4]在對大腸癌患者敏感篩查工具有效性的研究中,將SGA和PG-SGA作為參考標準進行分析,進一步驗證了這2個量表具有很高的敏感度和特異度。因此,本研究以SGA和PG-SGA作為腫瘤住院患者篩查的標準篩查工具,采用網狀Meta分析方法比較NRS-2002、MST、MUST、NRI和PG-SGA SF 5種常用營養篩查工具對腫瘤患者營養不良篩查的相對有效性,旨在為臨床準確評估腫瘤患者的營養狀況及制定臨床個體化營養支持方案提供依據。
1 資料與方法
1.1文獻納排標準 納入標準:(1)納入對象為經病理證實的惡性腫瘤患者且年齡≥18歲。(2)研究類型為診斷性研究。(3)以SGA或PG-SGA為金標準;篩查工具為NRS-2002、MST、MUST、NRI或PG-SGA SF。(4)結局指標為敏感度、特異度或可通過轉換計算出。(5)語種限定為中、英文。排除標準:(1)非惡性腫瘤患者。(2)參考標準非SGA或PG-SGA、無法提取數據。(3)重復發表、無法獲取全文的論文和會議論文。(4)非中、英文文獻。
1.2文獻檢索 檢索PubMed、Web of Science、MEDLINE、Embase、中國知網、維普數據庫及萬方數據庫,同時查找相關綜述、納入文獻的參考文獻。檢索時限為建庫至2020年10月。所有檢索策略通過多次預檢索后確定,采用主題詞與關鍵詞相結合的方式,中文檢索詞包括“腫瘤、癌癥、營養障礙、營養不良、營養不良風險、篩查工具、評估工具、量表、敏感度、靈敏度、特異度、效度”,英文檢索詞包括“cancer、tumor、nutritional disorders、 malnutrition、nutritional risk、screening tool、assessment tool、questionnaires、sensitivity、specificity、efficiency”。對于中文數據庫檢索出的會議論文資料和學位論文資源,檢索其已發表的期刊論文或納入文獻的參考文獻原文,追查已發表的相關系統評價、Meta分析和納入文獻的參考文獻,以獲取未檢索到的相關信息。
1.3文獻篩選與質量評價 由2位研究者獨立嚴格按照納入及排除標準對檢索出的文獻進行篩選,剔除明顯不符合標準的文獻,對可能相關的文獻閱讀全文后進行分析。若有分歧,則根據篩選標準進行討論或與第3位研究者討論決定。對最終納入的文獻進行資料提取,提取內容包括作者、發表年份、國家、研究對象、年齡、病例數、評估時間、評估工具、參照標準、敏感度和特異度。采用Cochrane協作網推薦的診斷準確性試驗質量評價工具(quality assessment of diagnostic accuracy studies,QUADAS-2)評估納入研究的方法學質量[5],該工具對4個域進行3個等級的評價,4個域為病例選擇、待評價試驗、金標準的選擇、病例流程和進展情況,3個等級為是、否、不清楚。
1.4統計學方法 結果分析建立在將篩查工具的結果轉化為二分類變量的基礎上。采用Stata 16.0軟件進行數據分析,采用mvmeta及network Meta命令進行網狀Meta分析,聯合SURCA命令進行秩次排序。采用校正-比較漏斗圖識別是否存在發表偏移。采用MetaDISc1.4軟件計算綜合受試者工作特征曲線(symmetric receiver operator characteristic curve,SROC) 模型估計曲線下面積。P<0.05為差異有統計學意義。
2 結果
2.1文獻檢索過程及結果 根據檢索策略檢索到相關文獻2 317篇 (中文534篇,英文1 783篇),經嚴格篩選最終納入17篇,其中中文5篇,英文12篇,包含3 454例患者。見圖1。
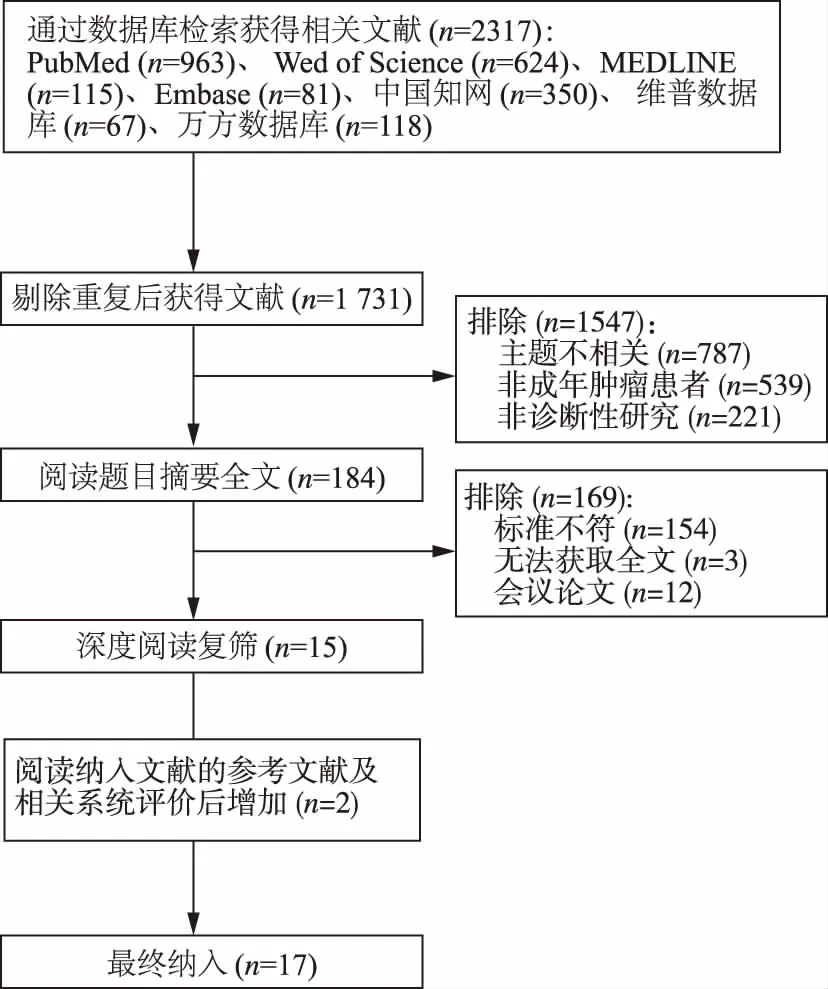
圖1 文獻篩選流程圖
2.2納入文獻的基本特征及質量評價 本文共納入比較的篩查工具共5個:NRS-2002、MST、MUST、NRI、PG-SGA SF。納入研究的基本特征見表1,質量評價見表2。
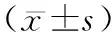
表1 納入研究的基本特征
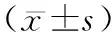
續表1 納入研究的基本特征
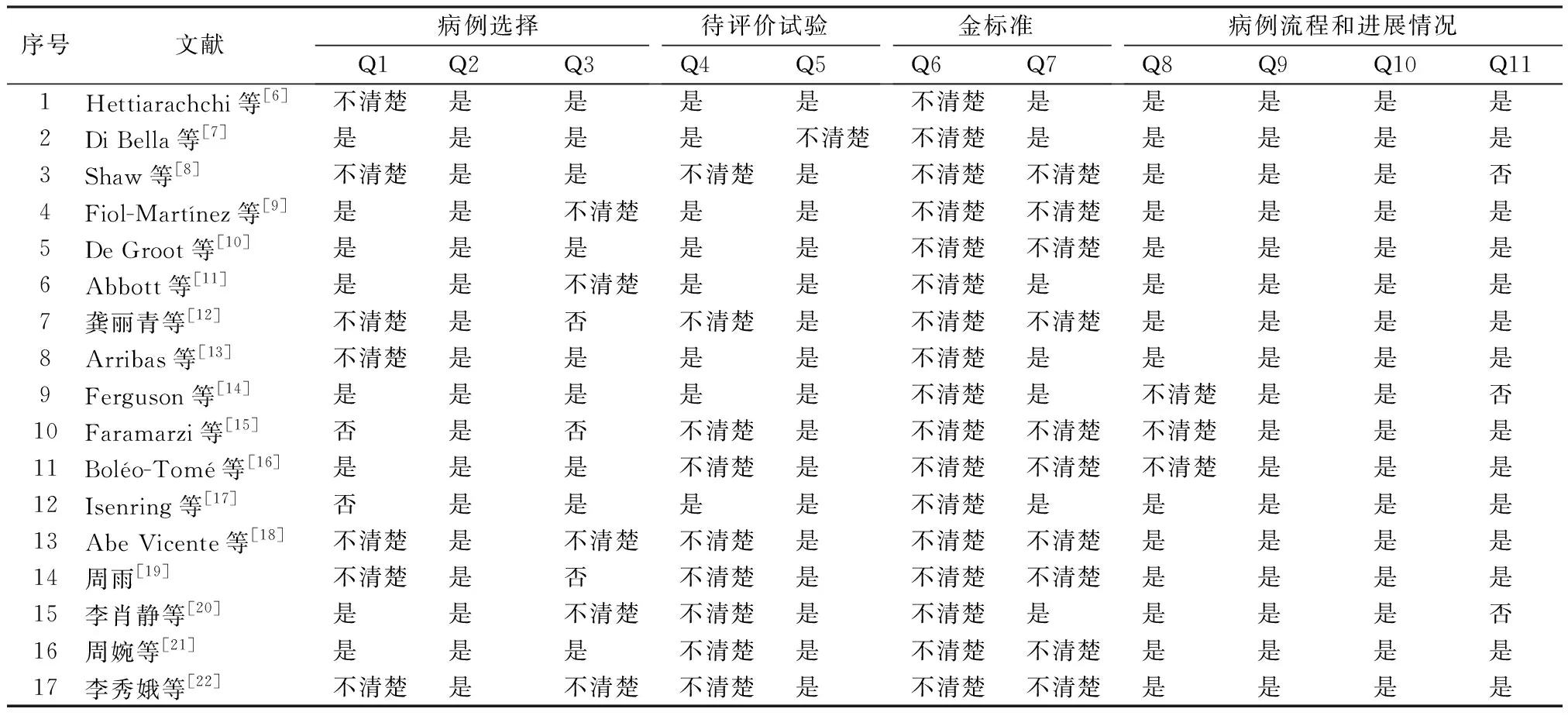
表2 納入研究的質量評價
2.3網狀Meta分析結果
2.3.1證據網絡、一致性檢驗和發表偏移檢測 證據網絡以參考標準為中心,以5個不同營養篩查工具為節點的網狀結構,見圖2。敏感度和特異度的一致性檢驗結果分別為(χ2=7.57,P=0.671;χ2=17.18,P=0.071),提示直接比較和間接比較結果具有一致性。校正-比較漏斗圖的研究分布基本圍繞零位線對稱,形狀為“頂小底大”的漏斗樣,可認為發表偏移較小,見圖3。

圖2 敏感度、特異度網絡證據圖

圖3 敏感度與特異度校正-比較漏斗圖二維碼
2.3.2敏感度 比較納入研究的敏感度,合并點估計值為[ES=0.842,95%CI(0.828,0.855),P<0.001]。7項研究驗證了NRS-2002的敏感度[ES=0.804,95%CI(0.780,0.826),P<0.001];12項研究驗證了MST的敏感度[ES=0.864,95%CI(0.839,0.887),P<0.001];8項研究驗證了MUST的敏感度[ES=0.908,95%CI(0.882,0.930),P<0.001];3項研究驗證了NRI的敏感度[ES=0.832,95%CI(0.769,0.884),P<0.001];5項研究驗證了PG-SGA SF的敏感度[ES=0.957,95%CI(0.935,0.973),P<0.001]。
2.3.3特異度 比較納入研究的特異度,合并點估計值為[ES=0.898,95%CI(0.889,0.906),P<0.001]。7項研究驗證了NRS-2002的特異度[ES=0.907,95%CI(0.888,0.925),P<0.001];12項研究驗證了MST的特異度[ES=0.913,95%CI(0.902,0.924),P<0.001];8項研究驗證了MUST的特異度[ES=0.909,95%CI(0.893,0.923),P<0.001];3項研究驗證了NRI的特異度[ES=0.864,95%CI(0.809,0.909),P<0.001];5項研究驗證了PG-SGA SF的特異度[ES=0.923,95%CI(0.900,0.942),P<0.001]。
2.3.4綜合受試者工作特征曲線 (SROC) SROC曲線兼顧了特異度和敏感度,曲線下面積可表示診斷的準確性,見圖4。NRS-2002的曲線下面積 (area under the curve,AUC)為0.7854;MST的AUC為0.8986;MUST的AUC為0.9027;NRI的AUC為0.7105;PG-SGA SF的AUC為0.9612。

圖4 SROC曲線二維碼
2.3.5排秩及聚類分析排序 擬合一致性模型后,對敏感度排秩,得出MUST和PG-SGA SF的敏感度較高;對特異度排秩,得出MST和PG-SGA SF的特異度較高。采用聚類分析將5種工具分成2類,PG-SGA SF和MUST診斷性能較高為最優推薦,見圖5。
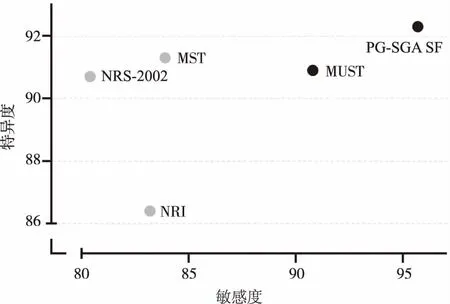
圖5 敏感度、特異度兩結局聚類分析排序
3 討論
3.1PG-SGA SF和MUST診斷性能優于其他3種量表 本研究共納入17篇研究,涉及5種常用的營養不良篩查工具。結果顯示,兼顧敏感度和特異度時,MUST和PG-SGA SF的診斷性能最好。在腫瘤患者中,體質量常常受到體液狀態的影響,患者可能出現體質量增加,同時體質量和脂肪儲存減少,因此腫瘤患者的營養評價不能過度依賴體質量變化,這也與作者前期研究結果相符[23]。我們的研究結果顯示,當用于營養評定/營養不良篩查時,PG-SGA SF或MUST一定程度能達到SGA和PG-SGA的篩查性能,而MST、NRS-2002和NRI則無法達到類似的篩查效果。Gabrielson等[24]在門診化療患者中對比PG-SGA SF與SGA的診斷準確性,得出了PG-SGA SF臨界點≥6分時診斷性能最好的結論。De Groot等學者[10]在門診接受抗癌治療的患者中發現PG-SGA SF臨界值≥5時與SGA的一致性最高,能比MST篩查出更多有營養不良風險的患者。PG-SGA SF很好地避免了體質量變化對營養不良評定的影響,并且還能檢測到營養風險改善的信息(過去2w體質量增加,攝入量比平時多),這些信息對提高營養支持的效果是非常有價值的。本研究中驗證了PG-SGA SF與其他篩查工具相比能夠顯示出更優的診斷性能。另外,與PG-SGA相比,PG-SGA SF內容更精煉,患者完成只需5 min或更短時間。這些研究結果都表明PG-SGA SF在腫瘤患者中具有較高的診斷準確性和可接受性。MUST由英國腸內腸外營養學會[25]于2003年制定,由體質指數、體質量減輕和進食量減少3方面組成。因其操作簡單,能在一定程度上預測預后而使用廣泛,缺點是患者在體質量回顧上可能存在回憶偏倚。
值得注意的是,以往研究中被應用于營養不良篩查的NRS-2002相較于參考標準的篩查能力并不出色,作者分析可能是NRS-2002更適用于營養風險篩查,而營養風險篩查和營養不良篩查是兩個完全不同的概念,營養風險強調與營養因素有關的出現臨床并發癥的風險,而非營養不良的風險[26]。既往對于篩查工具的比較大多停留在發生率/檢出率上,較少關注靈敏度、特異度或約登指數等診斷性試驗真實性的性能指標,這可能是造成本研究結果與其他學者不一致的原因之一。此外,應用營養篩查工具時應注意區分營養不良和營養風險篩查,以降低假陰性率或假陽性率。
3.2局限性 本研究系統比較了常用的5種營養不良篩查工具在腫瘤患者應用中的準確性,但尚存一些局限性。(1)由于原始研究的數量限制,我們無法就癌癥類型或區域間進行亞組分析。不同癌癥之間的異質性可能會隱藏不同篩查工具間真正的差異。(2)受制于納入文獻的質量,尤其是金標準相關的評價指標質量均較低,因此需要設計更完善的大樣本隨機對照研究來進一步證實研究結論。(3)可能存在語言偏倚。
4 小結
與參考標準相比,所有工具的篩查性能各有不同,總體來說,PG-SGA SF和MUST的診斷性能最好。結合PG-SGA SF和MUST具有內容精煉、操作簡便等特性,建議臨床工作者在對腫瘤患者的營養不良篩查時優先選用PG-SGA SF或MUST量表。

