胎兒側腦室和(或)后顱窩池增寬影像學評價與致病性拷貝數變異的差異
趙順標,洪偉峰,王榮躍,夏堅利,許敏,黃德益,趙雅萍,許崇永
1.玉環市人民醫院 放射科,浙江 臺州 317600;2.溫州醫科大學附屬第二醫院育英兒童醫院 放射科,浙江 溫州 325027
胎兒宮內發育監測以及出生缺陷的產前診斷一直是胎兒醫學的研究熱點[1]。側腦室增大(ventriculomegaly, VM)和(或)后顱窩池增寬(posterior cerebral fossa cistern enlargement,PCFCE)是胎兒中樞神經系統(central nervous system, CNS)最常見的產前超聲異常之一。重度VM和(或)PCFCE與患兒的死亡風險和腦發育不良密切相關,應盡早進行干預及治療[1-2]。產前精確診斷及評估VM和(或)PCFCE程度以及是否伴發CNS及其他臟器畸形具有重要價值。胎兒結構異常與染色體拷貝數變異(copy number variants, CNVs)相關,而染色體微陣列分析(chromosome microarray analysis, CMA)技術可檢測傳統核型分析無法發現的基因組微缺失或微重復變異,敏感度極高,逐漸成為超聲和MRI診斷胎兒異常的產前遺傳學一線檢測手段[3]。研究表明[3-4],CNVs在胎兒VM和(或)PCFCE的遺傳學病因中起重要作用,但目前研究結果不一致;本研究主要探討胎兒VM和(或)PCFCE程度與各系統結構畸形及CNVs差異,旨在為胎兒轉歸提供依據。
1 對象和方法
1.1 對象 收集溫州醫科大學附屬第二醫院育英兒童醫院及玉環市人民醫院2015年1月至2020年10月醫院產前胎兒共1 114例。納入標準:①超聲檢查診斷VM和(或)PCFCE胎兒。②其中468例胎兒行MRI及染色體核型分析(16~24周羊水檢測317例;24~38周臍帶血檢測151例)。③440例染色體核型正常胎兒行全基因組高分辨CMA檢測,分為輕中度組[VM和(或)PCFCE寬度10~15 mm]、重度組[VM和(或)PCFCE寬度>15 mm],分析胎兒CNS、泌尿生殖系統、循環系統及消化系統等畸形在不同CNVs(基因組微缺失或微重復)間的差異,評估妊娠結局。排除標準:①未簽署知情同意書;②孕婦幽閉恐懼癥;③帶有心臟起搏器、人工心臟瓣膜及體內鐵磁性異物者;④3個月內早期妊娠;⑤重度高熱孕婦。本研究獲得兩所醫院倫理委員會批準,胎兒父母均簽署知情同意書。
1.2 影像學檢查方法
1.2.1 超聲檢查:采用GE Voluson E8/E10彩色多普勒超聲診斷儀,配有RAB4-8-D凸陣腹部容積探頭和C1-5-D常規腹部探頭,頻率2.0~8.0 MHz和2.0~5.0MHz。圖像采集及測量方法:產前超聲詳細系統檢查胎兒全身各器官與結構,仔細觀察各系統發育情況,有無畸形;經腹部超聲探頭在標準平面測量后顱窩池及側腦室寬度。
1.2.2 MRI檢查:采用德國Siemens Avanto1.5T和Siemens Aera1.5T掃描儀,常規序列采用胎兒軸位、矢狀位及冠狀位掃描,掃描范圍覆蓋整個子宮。采用快速平衡穩態采集序列(FIESTA),重復時間TR 3.5~5.0 ms,TE 1.0~2.0 ms,層厚4.0 mm;單次激發快速自旋回波序列(SSFSE),TR 1 150~1 450 ms,TE 90~135 ms,層厚4.0 mm;由2名具有10年經驗的影像診斷醫師共同分析、閱片,并詳細記錄各系統陽性征象。
1.3 介入性產前穿刺診斷 317例(孕周16~24周)行超聲引導下羊水穿刺術。使用22G PTC針羊膜腔穿刺,抽吸羊水20~30 mL行染色體檢查;151例(24~38周)行超聲引導下臍血穿刺檢測,使用22G PTC針刺入臍帶,抽吸臍血2~3 mL行染色體檢查。
1.4 染色體核型分析和CMA檢查 上述羊水、臍血進行細胞培養,收獲后G顯帶染色制片,在光學顯微鏡下分析3個核型,計數20~30個核分裂相,對于嵌合體則計數50~100個核型。CMA檢測分析440例,其中羊水檢測308例,臍血檢測132例,采用Affymetrix CytoScan 750K芯片分析CNVs,參考OMIM、DECIPHER、DGV、ClinGen等數據庫對CNVs致病性進行判斷、分析。
1.5 出生后發育隨訪 通過電話隨訪咨詢患兒的出生后健康狀況,主要包括患兒的生長發育、大運動、精細運動、聽力、視力及語言發育等情況。
1.6 統計學處理方法 采用SPSS19.0軟件包進行統計學分析;符合正態分布的計量資料用±s表示,用兩獨立樣本t檢驗進行分析;不符合正態分布的計量資料用[M(P25,P75)]表示,用Mann-WhitneyU檢驗或Kruskal-WallisH檢驗進行分析;計數資料用百分比表示,用χ2檢驗或Fisher精確檢驗進行分析。P<0.05為差異有統計學意義。
2 結果
2.1 不同程度VM和(或)PCFCE組染色體核型異常的比較 468例胎兒中,染色體核型異常發生率為5.98%(28/468),其中數目異常11例,結構異常10,數目+結構異常7例,28例均引產,見表1。
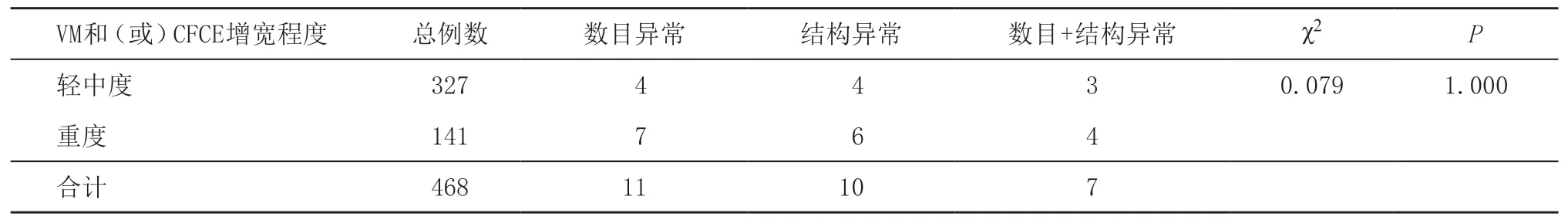
表1 不同程度VM和(或)PCFCE組染色體核型異常的比較(例)
2.2 致病性CNVs在不同程度VM和(或)PCFCE組中的比較 440例染色體核型正常胎兒中,致病性CNVs發生率為8.41%,大小范圍在187 kb~8.93 Mb。重度VM和(或)PCFCE組與輕中度組比,致病性CNVs發生率差異有統計學意義(P=0.012),見表2。
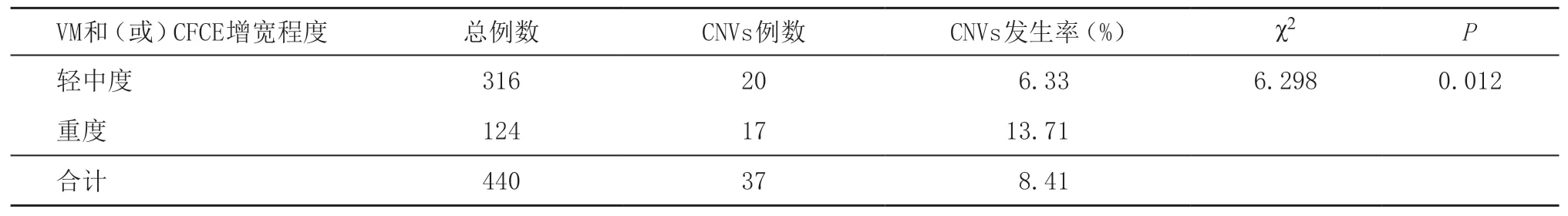
表2 不同程度VM和(或)PCFCE組致病性CNVs的比較
2.3 不同類型VM和(或)PCFCE組致病性CNVs的比較 單純VM、單純PCFCE、VM+PCFCE三組間致病性CNVs發生率差異有統計學意義(P=0.029),見表3。
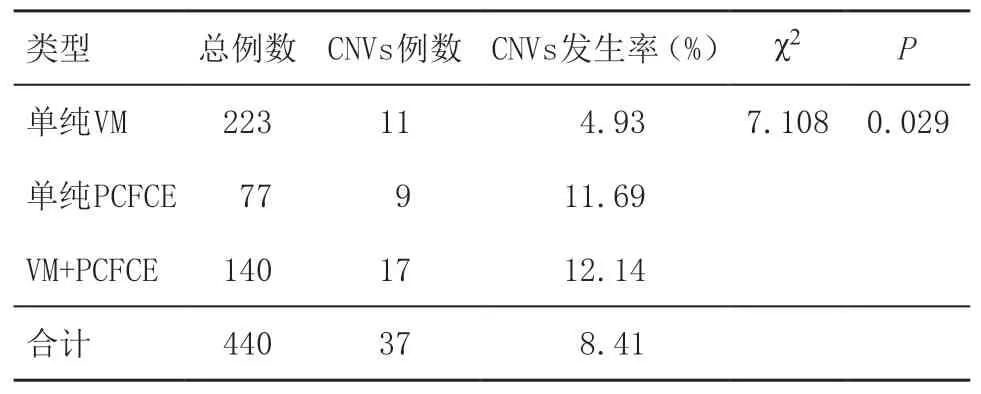
表3 不同類型VM和(或)PCFCE致病性CNVs的比較
2.4 致病性CNVs并發各系統畸形情況 37例致病性CNVs并發各系統畸形情況見表4、圖1、圖2。

圖1 VM和(或)PCFCE中致病性CNVs胎兒頭顱和腎臟MRI圖

圖2 VM和(或)PCFCE中致病性CNVs胎兒頭顱MRI和心臟超聲圖

表4 37例致病性CNVs并發各系統畸形情況
2.5 不同程度VM和(或)PCFCE組致病性CNVs并發臟器畸形的比較 輕中度和重度VM和(或)PCFCE組致病性CNVs并發臟器畸形的差異無統計學意義(P=0.700),見表5。
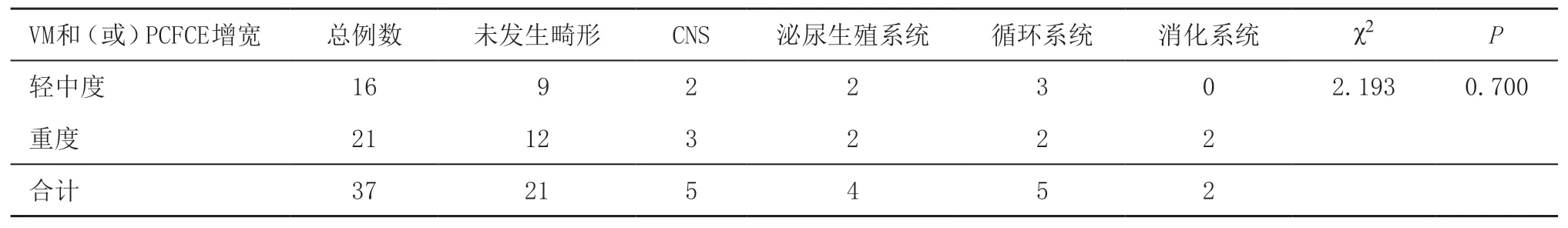
表5 不同程度VM和(或)PCFCE致病性CNVs并發臟器畸形的比較
2.6 不同程度VM和(或)PCFCE組胎兒畸形發生率的比較 16例臟器畸形中,輕中度組7例(2.2%),重度組9例(7.3%)差異有統計學意義(χ2=6.463,P=0.020)。
2.7 不同程度VM和(或)PCFCE組致病性CNVs轉歸比較 37例致病性CNVs胎兒中,輕中度組引產10例,分娩6例,重度組引產13例,分娩8例,差異無統計學意義(χ2=0.001,P=1.000)。
3 討論
產前超聲是評估胎兒結構異常必不可少的檢查方法,也是產科醫師的第三只眼睛,但因其難以穿越胎兒顱骨,視野偏小,對一些畸形尤其是CNS異常的篩查并沒有良好的特異性,且超聲檢查嚴重依賴于臨床醫師自身的技能水平,使其在輕中度VM和(或)PCFCE中無法取得較理想的診斷結果[5]。近年來隨著MR-3D成像及容積測量技術發展,電磁波吸收比值和噪聲降低,成像速度加快,圖像更加清晰準確,并已成為產前診斷的重要補充檢查[6]。
在妊娠15~40周,正常胎兒側腦室及后顱窩池寬度<10 mm,根據VM和(或)PCFCE程度分輕中度(10~15 mm)和重度(>15 mm),發現胎兒存在VM和(或)PCFCE時,首要任務是確定具體病因。若生理性所致,可能為一種正常變異,即孤立性VM和(或)PCFCE;若疾病所致,如先天性腦結構發育畸形、自發性顱內出血、病毒感染等,則稱之為非孤立性VM和(或)PCFCE。前者一般預后較好,而后者常合并多種疾病,常引起小兒智力和體格異常,預后差。針對后者,建議產婦終止妊娠,以降低先天性疾病患兒出生率,減輕家庭及社會的經濟負擔。
加拿大婦產科醫師協會(SOGC)推薦:輕中度VM和(或)PCFCE胎兒(無論是否合并其他異常)均應行羊膜穿刺術,進行核型分析和先天性感染評估。重度孤立性VM和(或)PCFCE胎兒的不良神經發育結局發生率高達38%~90%。盡管大多數輕度孤立性VM和(或)PCFCE預后較好,但也有神經發育異常風險。BAR-YOSEF等[2]研究133例孤立性VM和(或)PCFCE(僅1例重度側腦室增寬),發現3.8%(5/133)有發育遲緩癥狀。本研究468例胎兒中,28例染色體核型異常,發生率為5.98%,其中數目異常11例,結構異常10例,數目+結構異常7例,28例均引產;輕中度及重度VM和(或)PCFCE組間染色體核型異常發生率差異無統計學意義。
致病性CNVs是胎兒VM和(或)PCFCE的重要原因之一,重度VM和(或)PCFCE除了與染色體異常相關之外,還與基因突變密切相關[7]。HU等[8]研究154例輕至中度孤立性VM和(或)PCFCE胎兒致病性CNVs發生率,并評估了所有胎兒的神經發育結局,結果發現除3例隨訪時年齡小于12個月病例外,其余所有攜帶致病性CNVs的VM和(或)PCFCE胎兒出生后都表現出神經發育障礙。相反,沒有攜帶致病性CNVs的VM和(或)PCFCE病例出生后隨訪均未發現異常。因此,其認為致病性CNVs與胎兒VM和(或)PCFCE密切相關,并且可能參與胎兒VM和(或)PCFCE病理過程以及出生后神經發育障礙。本研究440例染色體核型正常胎兒中,輕中度與重度組VM和(或)PCFCE致病性CNVs發生率分別為6.33%、13.71%,CNVs發生率與VM和(或)PCFCE程度差異具有統計學意義;單純VM、單純PCFC、VM+PCFC致病性CNVs發生率分別為4.93%、11.69%、12.14%,差異有統計學意義,說明CNVs在胎兒VM和(或)PCFCE的遺傳學病因中起重要作用,因此所有VM和(或)PCFCE的胎兒均應進行CMA檢測,無論VM和(或)PCFCE嚴重程度或是否合并其他結構異常。
PAGANI等[5]對1 213例輕到中度VM和(或)PCFCE病例進行了系統評價和薈萃分析,發現孤立性VM和(或)PCFCE、VM和(或)PCFCE合并其他結構異常胎兒染色體異常的發生率分別為3.0%、8.3%。本研究37例致病性CNVs胎兒中,并發CNS畸形5例,其中胼胝體發育不良2例;泌尿生殖系統4例,其中腎積水2例;心臟大血管畸形5例;消化系統畸形2例;輕中度與重度VM和(或)PCFCE胎兒臟器畸形發生率分別為2.22%、7.26%,差異具有統計學意義。VM和(或)PCFCE僅為一個表象,在其背后可能有諸多復雜的原因,與預后密切相關。研究表明[9-10],重度VM和(或)PCFCE伴有結構異常、染色體異常和先天性感染的比率高于輕中度VM和(或)PCFCE組。本研究37例致病性CNVs胎兒中,引產23例,分娩14例;輕中度與重度VM和(或)PCFC引產例數分別為10例和13例,差異無統計學意義。
在妊娠早期,超聲即可提示VM和(或)PCFCE,但對側腦室增寬程度及腦室周圍組織發育、全身各器官系統有無異常診斷的準確度不高;隨著MR成像及容積測量技術發展,MRI憑借軟組織分辨率高、視野大等獨特優勢,圖像更加清晰準確,提高了胎兒異常檢出率。精準的影像學評估及病因診斷有助于VM和(或)PCFCE胎兒的宮內轉歸、預后評估和遺傳咨詢。

