異甘草素抗腹瀉活性及其分子機制研究
邢曉旭,張宗山,趙瑩瑩,張馨慧,曾丹丹,趙玉珠,張 旭
(黑龍江八一農墾大學動物科技學院,黑龍江 大慶 163319)
腹瀉是臨床常見疾病,嚴重危害公共衛(wèi)生安全并造成嚴重經濟損失,也是制約畜牧業(yè)發(fā)展因素[1],引起腹瀉原因包括細菌性腹瀉、病毒性腹瀉、寄生蟲性腹瀉及非傳染性腹瀉,預防和治療難度大[2]。因此尋找一種非特異性止瀉藥物成為目前亟待解決的問題之一。
中草藥在腹瀉病防控方面具有一定潛力,多種傳統(tǒng)單味中藥及方劑已被證明具有澀腸止瀉作用[3]。同時,中藥在治療豬腹瀉病上具有副作用小、耐藥性低、藥物無殘留等優(yōu)點[4]。甘草為豆科植物甘草(Glycyrrhiza uralensisFisch.)、脹果甘草(Glycyrrhiza inflataBat.)或光果甘草(Glycyrrhiza glabraL.)干燥根和根莖,味甘性平,具有補脾益氣,清熱解毒,祛痰止咳等功效,可與其他藥物連用止瀉[5]。異甘草素作為甘草提取物,已證明具有抗菌、抗病毒和增強免疫、減輕炎癥作用[6-7]。因此,異甘草素作為一種非特異性抗腹瀉藥物應用前景良好。
中藥治療疾病是“多成分、多途徑、多靶標”協(xié)同作用,無法從單一方面闡明其治療疾病的具體機制[8]。網絡藥理學是一門新興學科,通過整合多種組學、高通量篩選、分子交互驗證、網絡可視化分析等相關技術揭示“藥物-基因-靶標-疾病”之間復雜的網絡關系,闡明藥物作用機理,已成為研究創(chuàng)新藥物重要途徑。網絡藥理學可通過整理歸納現有數據庫中信息,分析中藥與疾病之間相互關系[9]。
本研究利用蓖麻油誘導小鼠腹瀉模型評價異甘草素抗腹瀉活性,再利用網絡藥理研究方法探討異甘草素治療腹瀉關鍵靶標,基于分子對接技術驗證異甘草素與靶標結合作用,揭示異甘草素治療腹瀉潛在分子機制,為臨床應用奠定理論基礎。
1 材料與方法
1.1 實驗動物
本試驗所用昆明白鼠購自哈爾濱醫(yī)科大學,雌雄各半。
1.2 試驗藥品
異甘草素標準品(PHLC≥98%)購自上海源葉生物科技有限公司;蓖麻油(貨號:C6770)購自北京索萊寶科技有限公司;二甲基亞砜(DMSO)購自北京索萊寶科技有限公司。
1.3 方法
1.3.1 蓖麻油誘導小鼠腹瀉
取昆明白鼠50只,體重為18~22 g,雌雄各半,隨機分成5組,每組10只,灌胃給藥,試驗分為空白對照組、腹瀉對照組、異甘草素(50mg.kg-1)低劑量組、異甘草素(100 mg.kg-1)中劑量組和異甘草素(200 mg.kg-1)高劑量組。試驗前24 h禁食,異甘草素低、中、高劑量組分別口服灌胃異甘草素0.2 mL,空白對照組和腹瀉對照組口服灌胃含0.1%DMSO生理鹽水0.2 mL。0.5 h后,分別灌胃0.2 mL蓖麻油,空白對照組灌胃0.2 mL生理鹽水,試驗觀察6 h,記錄各組小鼠精神和生理狀態(tài)及各組小鼠初次腹瀉時間和次數。
另取50只昆明白鼠,體重為18~22 g,雌雄各半,隨機分成5組,試驗分組與處理方式同上,用適量碳粉代替蓖麻油灌胃,1.5 h后處死小鼠,記錄并計算各組小鼠腸道內碳粉推進比。
腸道碳粉推進比計算公式為:推進比=碳粉推進長度/腸管總長度×100%。
1.3.2 網絡藥理學分析
1.3.2.1 異甘草素及腹瀉疾病靶標的檢索
在中藥系統(tǒng)藥理學數據庫和分析平臺(TCMSP數據庫,https://www.tcmspw.com/tcmsp.php)中檢索與異甘草素相關靶標。將“Diarrhea”作為檢索詞,在GeneCards在線數據庫(https://www.genecards.org/)中檢索腹瀉已知相關疾病靶點,得到腹瀉疾病靶點。將異甘草素相關蛋白與腹瀉相關靶標作對比,尋找兩者交集靶標,確定異甘草素治療腹瀉潛在靶點。
1.3.2.2 PPI靶蛋白互作網絡構建
利用STRING平臺(https://string-db.org/)構建交集靶點蛋白質-蛋白質互作網絡(PPI),分析異甘草素治療腹瀉靶標相互關系。將所有交集蛋白導入至STRING平臺,選擇“多重蛋白”分析,物種選擇為“mus”,根據結果選擇編碼相應蛋白基因名稱,生成蛋白互作網絡,分析網絡關聯(lián)度及蛋白富集系數,確定異甘草素治療腹瀉中調控關鍵蛋白。
1.3.2.3 基因本體論(Geneontology,GO)分析
將篩選出的交集靶點基因導入WebGestalt在線工具,對交集靶點作GO富集分析,將物種與背景設定為“mus”,根據P<0.05描述蛋白質顯著程度,分析交集靶標所集中的生物學過程,探討異甘草素治療腹瀉所影響的分子通路。
1.3.2.4 KEGG通路富集分析
與GO分析原理相同,將篩選出的靶點導入WebGestalt在線工具,對交集靶點作KEGG富集分析,將物種與背景設定為“mus”,根據P<0.05描述顯著程度,得到異甘草素治療腹瀉疾病主要作用通路,分析顯著通路。
1.3.3 分子對接
在PDB數據庫(https://www1.rcsb.org/)檢索關鍵蛋白晶體結構,利用NCBI(https://www.ncbi.nlm.nih.gov/)檢索異甘草素3D結構。利用Discovery situido 2016作分子對接,采用C-CDOCK半柔性對接,計算異甘草素與關鍵靶標相互作用潛在結合構想和結合能,確定潛在異甘草素與關鍵靶標相互作用模式。
1.3.4 熒光定量PCR
取昆明白鼠10只,體重為18~22 g,雌雄各半,隨機分成兩組,每組5只,分別為健康對照組、異甘草素組。異甘草素組口服灌胃0.2 mL 200 mg.kg-1異甘草素溶液,對照組灌胃等量生理鹽水。6 h后,處死小鼠,取各小鼠腸段組織研磨,利用RNA提取試劑盒提取組織中RNA,再利用反轉錄試劑盒將RNA反轉錄為cDNA,通過NovoStart?SYBRqPCR SuperMix Plus法實時熒光定量檢測系統(tǒng)作qPCR。所用引物見表1。將上述體系加于0.1 mL八聯(lián)管內,混勻后瞬離上機。反應體系為:水(RNase-Free ddH2O)5μL,上、下游引物(10μmol.L-1)各0.5μL,預混染料(NovoStart?SYBR qPCR SuperMix Plus)10μL,模板(cDNA)4μL,共計20μL。反應程序為:95℃30 s;95℃30 s,60℃30 s,72℃30 s,40個循環(huán);92℃5 s,60℃1 min,95℃continues;50℃30 s。反應結束后,讀取Ct值,運用ΔΔCt法分析數據。確定異甘草素對MAPK14、NCOA2、PPARG和ESR1基因表達的影響。

表1 熒光定量PCR引物Table1 Primersfor quantitative PCR reactions
1.3.5 統(tǒng)計分析
所有試驗均開展3次獨立重復試驗,使用Excel 2016和SPSS 19.0軟件對數據作統(tǒng)計學分析,P>0.05表示無顯著性差異,不標記;0.01<P<0.05表示顯著性差異,以*標記;P<0.01表示極顯著性差異,以**標記。
2 結果與分析
2.1 異甘草素對蓖麻油小鼠腹瀉的治療作用
本研究通過蓖麻油誘導小鼠腹瀉模型評價異甘草素抗腹瀉作用,腹瀉對照組小鼠試驗開始后6 h精神沉郁,不喜運動,四肢蜷縮,小鼠被毛粗亂;用藥組小鼠精神狀態(tài)良好,生理狀態(tài)正常,與空白對照組相比無明顯差異。如圖1所示,與腹瀉對照組相比,異甘草素顯著降低小鼠腹瀉次數(P<0.05),延緩小鼠初次腹瀉時間(P<0.05),且呈一定劑量依賴。同時,與腹瀉對照組相比,異甘草素還可顯著抑制腸道蠕動(P<0.05),延緩碳粉推進距離,減少腹瀉發(fā)生。試驗結果表明異甘草素對蓖麻油誘導小鼠腹瀉具有良好治療作用。
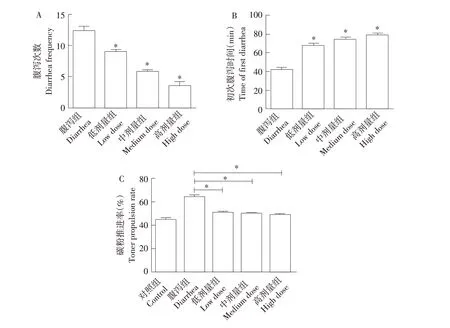
圖1 異甘草素對蓖麻油誘導的小鼠腹瀉治療作用Fig.1 Effect of isoliquiritigenin on castor oil induced diarrhea in mice
2.2 網絡藥理學分析
基于數據檢索,在TCMSP數據庫中共找到與異甘草素相關蛋白靶標34個,在GeneCards在線數據庫共找到與腹瀉相關靶標蛋白5 686個,其中交集靶標共計14個,蛋白名稱如表2所示。這些交集靶標與腹瀉的發(fā)生和異甘草素均具有一定相關性,可能是異甘草素治療腹瀉的靶標。

表2 交集靶標信息Table 2 Intersection target information
將上述交集蛋白名稱導入至STRING平臺,通過STRING平臺構建蛋白互作網絡,種屬選擇為“mus”。試驗結果見圖2,共有4個蛋白與其他蛋白無關聯(lián),其余蛋白與網絡中其他蛋白均產生緊密相關性,網絡中蛋白節(jié)點數為13,網絡預期邊數為5,共產生17條邊,平均節(jié)點度為2.62,PPI富集P值為1.11×10-5,表明網絡中蛋白與蛋白高度關聯(lián),其中有絲分裂活化蛋白激酶14(MAPK14)、核受體輔活化因子2(NCOA2)、過氧化物酶體增殖物激活受體(PPARG)及雌激素受體1(ESR1)在PPI中節(jié)點數最高,為關鍵蛋白。異甘草素可能通過影響上述4個關鍵蛋白活性或調節(jié)關鍵蛋白表達,進而影響整個網絡,達到治療腹瀉目的。
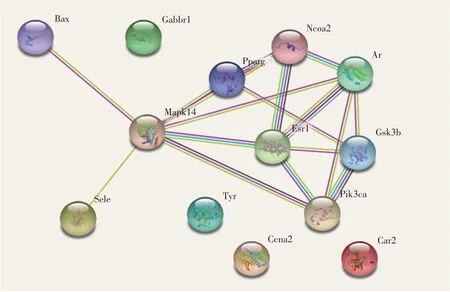
圖2 交集靶標蛋白互作圖Fig.2 PPI of intersection target
2.3 KEGG分析
對上述靶標基因作富集分析,KEGG分析結果見圖3,這些蛋白主要參與成纖維細胞增值通路調節(jié)、平滑肌細胞凋亡過程調節(jié)及應激反應等相關生物學過程,表明異甘草素可能通過上述基因通路和生物學過程,達到治療腹瀉目的。
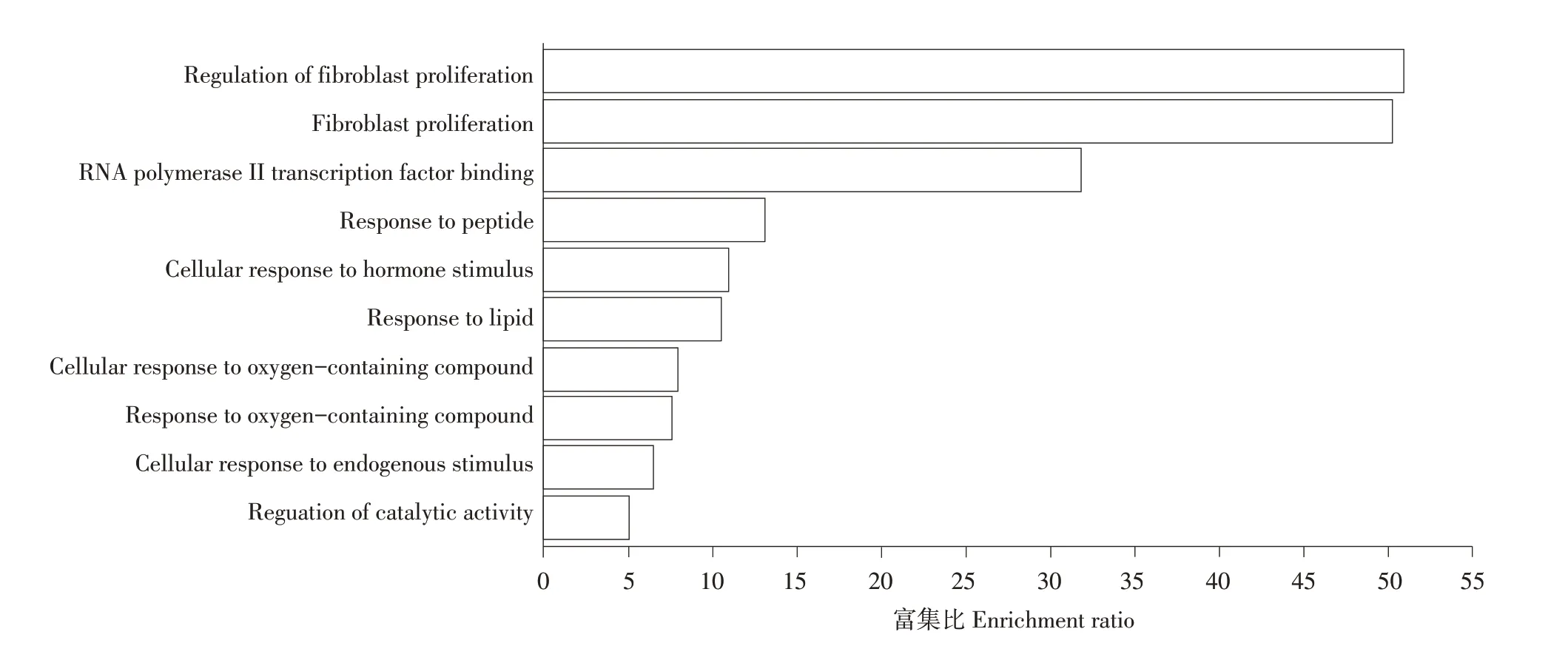
圖3 KEGG分析Fig.3 KEGG analysis
2.4 GO分析
對異甘草素治療腹瀉的相關靶標作GO基因富集分析,試驗結果如圖4所示,不同顏色分別代表不同富集類別,紅色代表生物學過程、藍色代表細胞成分、綠色代表分子功能。
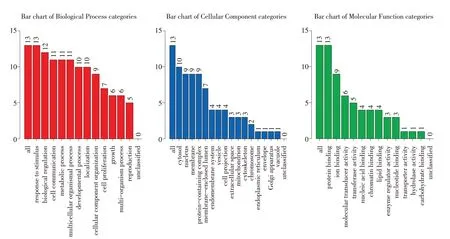
圖4 GO分析Fig.4 GO analysis
結果表明這些靶標基因與應激反應、生物學運動及細胞信息傳遞等生物學過程緊密聯(lián)系。同時,這些靶標基因參與細胞質和細胞核物質調控,與蛋白互作及細胞信息傳遞高度相關。
2.5 分子對接
基于網絡藥理學分析,找到異甘草素治療腹瀉的4個關鍵靶標,分別為MAPK14、NCOA2、PPARG以及ESR1。通過分子對接分析異甘草素與4個關鍵靶標結合作用。如圖5所示,異甘草素分別有效占據4個蛋白活性腔內,異甘草素在該結構域內與底物存在競爭關系,抑制蛋白功能。異甘草素與4個蛋白結合能分別為-30.25、-42.65、-37.64和-46.56 KJ.mol-1。表明異甘草素可自發(fā)與4種蛋白產生結合,是靶標潛在競爭性抑制劑。
2.6 異甘草素對靶標基因表達的影響
為進一步驗證異甘草素與關鍵靶標關系,利用熒光定量PCR檢測異甘草素對關鍵靶標基因表達的影響。異甘草素顯著下調MAPK14、NCOA2、PPARG及ESR1基因表達,結果見圖6。表明異甘草素通過影響關鍵靶標基因表達調控腹瀉相關通路,達到治療腹瀉的作用。
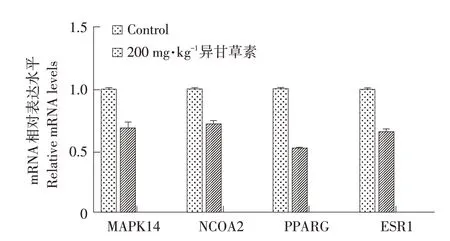
圖6 異甘草素對關鍵靶標基因表達的影響Fig.6 Effect of isoglycyrrhizin on the expression of key target genes
3 討論
異甘草素具有良好抗腹瀉效果,可顯著降低腹瀉次數,延緩初次腹瀉時間,作為一種非特異性抗腹瀉藥物具有一定開發(fā)前景[10-11]。為更好探究異甘草素抗腹瀉作用機制,本文通過網絡藥理學和分子對接方法尋找異甘草素治療腹瀉關鍵蛋白。網絡藥理學是借助網絡研究藥物-靶標-疾病之間關系,基于現有數據信息再次整合,挖掘藥物治療疾病藥理作用的研究方法[12]。本研究探討異甘草素治療腹瀉的關鍵靶標和關鍵通路,結果表明MAPK14、NCOA2、PPARG和ESR1可能是異甘草素治療腹瀉關鍵蛋白。同時,本研究利用熒光定量技術確定異甘草素對上述關鍵靶標基因的影響。白東東等利用網絡藥理學方法分析白頭翁治療腹瀉分子機制,確定雌激素受體1(Estrogen receptor,ESR1)、CREB結合蛋白(CREB binding protein,CREBBP)等gned45個關鍵靶標[13],與本研究結果相似。在異甘草素治療腹瀉關鍵靶標中,MAPK14在結腸炎中具有重要調節(jié)作用,研究表明蓖麻油可對腸黏膜產生強烈刺激,引起腸道炎癥導致動物腹瀉[14]。此外,研究表明NCOA2參與腸道膽汁酸相關通路調節(jié),與結腸炎發(fā)生和發(fā)展相關[15]。PPARG主要存在3個亞型,多在脂肪組織內表達,參與膽固醇和脂質代謝等生物學過程,對腸道內微環(huán)境有一定調節(jié)作用,與腹瀉發(fā)生相關[16]。分子對接技術是目前篩選和設計靶向性藥物的有效手段,為藥物研發(fā)提供重要數據支撐和試驗依據。通過計算機模擬技術進行分子對接已成為藥物研發(fā)主要途徑[17]。在本研究中利用Discovery Stiudio 2016進行半柔性對接,小分子可根據鍵轉角合理改變構象,使結果更加準確。分子對接結果顯示異甘草素能夠有效與MAPK14、NCOA2、PPARG以及ESR1產生結合,結合能均為負值,說明異甘草素可通過抑制上述關鍵靶標活性影響腹瀉相關生物學通路,治療腹瀉。
KEGG和GO基因富集分析是分析“藥物-靶標-通路”有效手段,KEGG分析結果表明交集蛋白與成纖維細胞增值的信號通路調節(jié)高度相關,成纖維細胞是疏松結締組織的重要細胞成分,對維持黏膜固有層和黏膜下層結構具有重要生理作用[18]。表明異甘草素可通過調控成纖維細胞增殖維持腸道管壁結構的穩(wěn)定,防止腹瀉發(fā)生。GO分析結果顯示交集靶標與應激反應相關,而造成腹瀉原因之一是機體對環(huán)境改變而產生應激反應[19],表明異甘草素可通過控制應激反應發(fā)生降低機體發(fā)生腹瀉情況。GO分析結果顯示異甘草素與離子之間相互作用有關,造成腹瀉發(fā)生最直接原因是腸道內無機鹽離子失衡,異甘草素可通過抑制關鍵蛋白,引起相關基因表達,輻射至整個信號通路,影響胃腸道內環(huán)境,延緩腹瀉發(fā)生。基于網絡藥理學和分子對接研究,表明異甘草素可能通過維持腸道內環(huán)境,降低炎癥反應,起抗腹瀉作用。
綜上所述,異甘草素作為抗腹瀉藥物具有良好開發(fā)前景。本研究基于網絡藥理學和分子對接,分析異甘草素治療腹瀉的潛在靶標及可能影響的生物學過程,初步探討其抗腹瀉分子機制,為后續(xù)異甘草素抗腹瀉研究奠定理論基礎。

