腹膜透析患者AAC與鈣磷代謝相關(guān)性及預(yù)測CVD價(jià)值研究
陳珊珊,劉東海,岳英麗
(河北省廊坊市人民醫(yī)院腎內(nèi)科 065000)
腹膜透析是慢性腎臟病(CKD)5期重要的治療方法。有研究顯示,CKD 5期患者通過腹膜透析治療生存率可得到明顯改善[1],但因CKD誘發(fā)的心血管疾病(CVD)逐漸增多,這可能成為今后CKD患者的主要死因[2]。鈣磷代謝與CKD患者CVD密切相關(guān),有研究認(rèn)為,鈣磷代謝可能參與頸動(dòng)脈鈣化[3]。另外,腹主動(dòng)脈鈣化(AAC)評分(AACS)屬半定量評分法。張蕊等[4]研究顯示,AACS有助于預(yù)測血液透析患者CVD風(fēng)險(xiǎn),推測AACS對判斷腹膜透析患者CVD風(fēng)險(xiǎn)有積極作用。因此,本研究回顧性分析2018年8月至2020年3月該院80例腹膜透析患者臨床資料,探討AACS與鈣磷代謝的關(guān)系,分析其在預(yù)測CVD中的應(yīng)用價(jià)值,現(xiàn)報(bào)道如下。
1 資料與方法
1.1 一般資料
選擇2018年8月至2020年3月本院腎內(nèi)科收治的腹膜透析患者80例。納入標(biāo)準(zhǔn):(1)患者均在本院接受規(guī)范腹膜透析治療;(2)年齡大于或等于18歲;(3)均使用axter Dianeal透析液與1.5 mmol/L濃度鈣離子透析;(4)臨床資料完整。排除標(biāo)準(zhǔn):(1)正在接受激素治療或既往有冠狀動(dòng)脈搭橋手術(shù)治療者;(2)合并有嚴(yán)重心肺疾病者;(3)合并有惡性腫瘤者;(4)妊娠哺乳期患者;(5)原發(fā)性甲狀腺功能亢進(jìn)癥(以下簡稱甲亢)患者;(6)其他原因?qū)е卵}磷代謝異常的疾病。80例患者中男48例,女32例;年齡(57.16±13.32)歲;體重指數(shù)(BMI)為(20.81±1.64)kg/m2;透析時(shí)間(26.72±8.09)個(gè)月;透析年齡為(55.41±8.16)歲。原發(fā)病:糖尿病腎病31例,慢性腎小球腎炎20例,腎病綜合征15例,高血壓腎損害5例,多囊腎4例,狼瘡性腎炎4例,馬兜鈴酸腎病1例。
1.2 方法
采用AACS對鈣化程度進(jìn)行評估。行腹部側(cè)位X線檢查,根據(jù)檢查結(jié)果對L1~4對應(yīng)腹主動(dòng)脈前壁和后壁鈣化斑塊進(jìn)行評分[5],AACS為0~15分,其中無鈣化為0分;鈣化斑塊小于1/3動(dòng)脈壁長度為1分;鈣化斑塊大于或等于1/3~≤2/3動(dòng)脈壁長度為2分;鈣化斑塊大于2/3動(dòng)脈壁長度為3分。根據(jù)AACS將80例患者分為無鈣化組(AACS=0分,n=36)、輕度鈣化組(AACS>0~<5分,n=18)、中度鈣化組(AACS 5~≤15分,n=12)及重度鈣化組(AACS>15分,n=14)。取患者入院時(shí)的肘靜脈血5 mL,離心后送檢。采用比色法測定血磷、分光光度法測定血鈣,放射免疫法檢測全段甲狀旁腺激素(iPTH),計(jì)算鈣磷乘積(CPP)。采用西門子Siemens全自動(dòng)生化分析儀檢測低密度脂蛋白膽固醇(LDL-C)、高密度脂蛋白膽固醇(HDL-C)、血肌酐(SCr)及C反應(yīng)蛋白(CRP)。治療結(jié)束后對患者均行12個(gè)月隨訪,記錄CVD發(fā)生率,將發(fā)生心肌梗死、心力衰竭、心絞痛、心源性猝死定義為CVD[6]。
1.3 統(tǒng)計(jì)學(xué)處理
2 結(jié) 果
2.1 各組患者鈣磷代謝指標(biāo)比較
80例患者中出現(xiàn)AAC 44例(55.00%)。各組患者血磷、iPTH及CPP水平比較,差異有統(tǒng)計(jì)學(xué)意義(P<0.05),見表1。
2.2 AACS與鈣磷代謝指標(biāo)Pearson線性相關(guān)分析
Pearson線性相關(guān)分析顯示,AACS與血鈣無明顯正相關(guān)(r=0.124,P=0.587);而與血磷、iPTH、CPP均呈正相關(guān)(r=0.318、0.387、0.506,P<0.001)。
2.3 腹膜透析患者CVD風(fēng)險(xiǎn)因素分析
80例腹膜透析患者中位隨訪時(shí)間為(10.24±1.77)個(gè)月,失訪3例,77例患者發(fā)生CVD者14例(18.18%)。采用Cox風(fēng)險(xiǎn)回歸分析顯示,高血壓腎損害、iPTH、CPP及AACS是腹膜透析患者發(fā)生CVD的獨(dú)立影響因素(P<0.05),見表2、3。
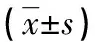
表1 各組患者鈣磷代謝指標(biāo)水平比較

表2 腹膜透析患者CVD風(fēng)險(xiǎn)單因素分析
2.4 AACS及iPTH等指標(biāo)預(yù)測CVD的ROC曲線
ROC曲線分析顯示,AACS、高血壓腎損害、CPP及iPTH對判斷CVD均有一定價(jià)值(P<0.05),見圖1、表4。AACS判斷CVD的曲線下面積(AUC)明顯高于高血壓腎損害(Z=2.776,P=0.017)、CPP(Z=3.097,P<0.001)及iPTH(Z=2.362,P=0.029)。

表3 腹膜透析患者CVD風(fēng)險(xiǎn)多因素分析

圖1 AACS及iPTH等指標(biāo)預(yù)測CVD的ROC曲線

表4 腹膜透析患者AACS及iPTH等指標(biāo)預(yù)測CVD發(fā)生的ROC曲線分析
3 討 論
近年來有關(guān)鈣磷代謝與CVD的關(guān)系已有較多報(bào)道,曾鵬廷[7]研究發(fā)現(xiàn),成纖維細(xì)胞生長因子23(FGF23)在鈣磷代謝致CVD中起到關(guān)鍵作用。在維持性腹膜透析患者中,F(xiàn)GF23升高早于血磷,并可通過調(diào)節(jié)血磷、iPTH水平,參與鈣磷代謝,進(jìn)而造成血管鈣化。劉亞等[8]研究顯示,在鈣磷代謝過程中,F(xiàn)etuin-A水平降低,其抑制鈣磷在軟組織沉積的作用被削弱,從而造成鈣磷的骨外沉積,導(dǎo)致血管鈣化的發(fā)生,最終誘導(dǎo)CVD。另外,也有研究顯示,AAC是CVD的誘因[9]。腹膜透析患者AAC發(fā)生率為33%~80%[10-11],本研究中AAC率為55.00%,與既往報(bào)道相符。因腹主動(dòng)脈在L4節(jié)段下緣分叉,使其局部血流產(chǎn)生湍流效應(yīng),這導(dǎo)致AAC呈現(xiàn)由近端至遠(yuǎn)端逐漸加重特點(diǎn)[12]。李璐瑤等[13]認(rèn)為,AACS與CVD發(fā)生率呈明顯相關(guān)性。本研究結(jié)果證實(shí),AACS是CVD的獨(dú)立影響因子。
另外,本研究發(fā)現(xiàn),AACS與血磷、CPP及iPTH呈明顯正相關(guān),提示AAC與鈣磷代謝有關(guān),這可能是AACS致CVD的原因。腹膜透析患者多合并高磷血癥,其風(fēng)險(xiǎn)與透析時(shí)間正相關(guān),有研究顯示,80%的CKD患者存在高磷血癥[14],當(dāng)腎小球?yàn)V過率(GFR)<60 mL/(min·1.73 m2)時(shí)患者尿磷排泄降低,體內(nèi)血磷水平明顯增高,另受透析等因素影響,最終導(dǎo)致高磷血癥發(fā)生,為保證患者預(yù)后,有必要將血磷控制在合理范圍內(nèi),根據(jù)相關(guān)指南顯示,患者血磷、CPP應(yīng)分別低于1.78 mmol/L、2.94(mmol/L)2,另外,有效控制透析次數(shù)及時(shí)間也可降低血磷水平[15]。對于接受腹膜透析治療的CKD 5期患者,鈣磷代謝紊亂發(fā)生率高[16],這引起甲狀旁腺組織異常增生,使iPTH和CPP水平上升,加快局部血管鈣化,促使AACS異常增加。此外,鳶尾素與骨形態(tài)發(fā)生蛋白7(BMP-7)是具有抑制血管鈣化作用的相關(guān)因子,隨著腹膜透析時(shí)間的延長,鈣磷代謝紊亂日益嚴(yán)重,這導(dǎo)致鳶尾素與BMP-7水平降低[17]。而隨著BMP-7和鳶尾素水平降低,其對血管平滑肌細(xì)胞增殖的抑制作用降低[18],使AACS升高。但有關(guān)AACS與鈣磷代謝相互影響的具體機(jī)制尚不完全清楚[19],這有待今后深入研究。
腹部側(cè)位X線片檢查操作簡便,且價(jià)格低廉,被全球腎臟病預(yù)后組織推薦為可替代CT的影像學(xué)檢查方法[20]。本研究顯示AACS與血磷代謝指標(biāo)相關(guān),且是判斷CVD風(fēng)險(xiǎn)的獨(dú)立因素。因而,AACS在腹膜透析患者中具有廣闊應(yīng)用前景。本研究在Cox分析基礎(chǔ)上采用ROC探討AACS對判斷CVD風(fēng)險(xiǎn)的價(jià)值,結(jié)果顯示AACS判斷CVD的AUC為0.806,明顯高于其他單項(xiàng)指標(biāo),說明AACS臨床應(yīng)用價(jià)值高,尤其是AACS超過10分時(shí),應(yīng)警惕CVD的發(fā)生。但本文為回顧性分析,納入樣本量有限,結(jié)論還有待今后前瞻性研究證實(shí)。
綜上所述,腹膜透析患者AACS與鈣磷代謝相關(guān),監(jiān)測AACS有助于判斷CVD風(fēng)險(xiǎn)。另外,本研究仍存在一定的不足,即受到時(shí)間限制樣本量納入較少、未對發(fā)生CVD患者的預(yù)后及死亡危險(xiǎn)因素進(jìn)行分析。因此,在后續(xù)的研究中仍期待擴(kuò)大樣本量,延長隨訪時(shí)間,繼續(xù)深入探討腹膜透析患者發(fā)生CVD的預(yù)后及其死亡影響因素,以期為此類患者治療工作的開展提供更加詳細(xì)、可靠的依據(jù)。

