上海地區成年人碘營養狀況及其與甲狀腺功能的關系
韓 兵,王寧薦,陳 馳,俞 潔,陳 奕,陳穎超,程 靜,陸穎理
(上海交通大學醫學院附屬第九人民醫院內分泌科 200011)
碘是一種合成甲狀腺激素所必需的重要微量元素。在成年人,每日碘攝入量為150 μg,而在孕婦和哺乳期的婦女,每日推薦碘攝入量為250 μg[1]。碘缺乏和碘過量都會導致甲狀腺疾病。碘缺乏會導致甲狀腺腫、甲狀腺功能減退(簡稱甲減)、甲狀腺功能亢進(簡稱甲亢)和甲狀腺自身免疫性疾病[2]。而碘過量會導致甲亢和甲減[3]。長久以來,碘缺乏已被認為是一種重要的公共衛生問題,因此許多國家采用食鹽加碘來消除碘缺乏[4]。1996年開始我國實行全民食鹽加碘法規。2000年和2011年經歷了兩次食鹽加碘濃度下調,允許各個省份根據不同情況選擇食鹽加碘濃度。2005年我國已經完全消除碘缺乏癥。然而,隨著碘缺乏的逐漸糾正,流行病學調查顯示中國人群總體處于碘超足量狀態,這也導致了甲狀腺疾病發病率的增加[5]。上海市從1996年4月開始全面實施食鹽加碘政策。本研究通過檢測上海郊區及市區成年人尿碘濃度(UIC),甲狀腺功能及自身抗體情況,更好地了解上海市成年人碘營養狀態及其與甲狀腺功能的關系。
1 對象與方法
1.1 對象
2019年3-9月,本課題組采取整群、分層抽樣的方法,在上海市黃浦區(市區)及上海市奉賢區(郊區)共抽取2 166例18歲以上常住成年人,排除甲狀腺手術史患者90例;垂體瘤手術病史患者2例;放射碘治療患者1例;最終納入2 073例。其中市區成年人1 013例,年齡(56.03±13.66)歲;郊區成年人1 060例,年齡(62.04±10.57)歲;男848例,女1 225例。納入標準:年滿18歲以上,漢族;在當地居住半年以上。排除標準:妊娠;終末期疾病;近3個月接受造影劑檢查或者服用胺碘酮。
1.2 方法
1.2.1一般資料收集
由統一培訓的調查人員進行問卷調查。調查內容包括:地區、年齡、性別、籍貫、常住地、甲狀腺病史及用藥情況、甲狀腺疾病家族史、吸煙情況。使用標準化方案測量人體參數,包括身高、體重,采用體重(kg)/身高平方(m2)計算體重指數(BMI)。
1.2.2甲狀腺功能、維生素D及UIC檢測
收集受試者血清,采用化學發光法進行促甲狀腺激素(TSH)、三碘甲狀腺原氨酸(T3)、四碘甲狀腺原氨酸(T4)、甲狀腺過氧化物酶抗體(TPOAb)、甲狀腺球蛋白抗體(TGAb)檢測(SIEMENS immulite 2000,德國)。TSH、T3、T4可反映機體總的甲狀腺激素水平[6],TPOAb和TGAb高于60 IU/mL定為抗體陽性。采用化學發光法(SIEMENS ADVIA Centaur XP,德國)檢測受試者血清維生素D。組內差異6.25%,組間差異8.33%。UIC的測定使用電感耦合等離子體質譜法(ICP-MS,Agilent 7700x,美國)。組內差異10%,組間差異15%。判定標準:根據WHO/UNICEF/ICCIDD建議,UIC中位數小于100 μg/L為碘缺乏,100~<200 μg/L為碘適量,200~300 μg/L為碘超足量,>300 μg/L為碘過量。
1.3 統計學處理
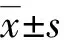
2 結 果
2.1 基線特征
研究對象整體人群年齡(59.33±12.61)歲,UIC為195.50(139.10~287.45)μg/L,碘缺乏、碘足量、碘超足量、碘過量的比例分別為8.32%、43.03%、26.22%、22.43%。男、女性間年齡比較差異無統計學意義(P>0.05);男性UIC明顯高于女性(204.30 μg/Lvs.189.10 μg/L)。男、女性BMI和維生素D水平比較,差異有統計學意義(P<0.01)。女性TSH及TPOAb、TGAb陽性率均高于男性(P<0.01),見表1。
2.2 郊區及市區成年人UIC及甲狀腺功能相關指標等比較
郊區、市區成年人平均年齡分別為(62.04±10.57)、(56.03±13.66)歲。市區成年人UIC明顯高于郊區(P<0.01)。市區和郊區成年人的BMI和維生素D存在明顯差異(P<0.05)。郊區成年人TSH水平高于市區,市區成年人T3、T4水平高于郊區,差異均有統計學意義(P<0.01)。根據上海市統計局2018年黃浦區和奉賢區成年人口比例調整碘營養狀態比例、吸煙比例及TPOAb和TGAb陽性率。黃浦區18~<35、35~60、60歲以上人口比例分別為19.30%、37.20%、43.50%。奉賢區18~<35、35~60、60歲以上人口比例分別為17.20%、46.60%、36.20%。經過不同年齡段人口比例校正后,郊區和市區成年人的TPOAb陽性率比較差異無統計學意義(P>0.05),而TGAb陽性率比較差異有統計學意義(P<0.05)。另外,二者碘營養狀態比較差異有統計學意義(P<0.01),見表2。
2.3 不同碘營養狀態的成年人UIC及甲狀腺功能情況
郊區成年人碘缺乏、碘適量、碘超足量、碘過量成年人的UIC分別為83.55、153.60、242.80、379.05 μg/L。市區碘缺乏、碘適量、碘超足量、碘過量成年人的UIC分別為88.05、145.30、245.10、415.80 μg/L。郊區和市區不同碘營養狀態的成年人TSH和T3水平比較,差異均無統計學意義(P>0.05);T4水平比較差異有統計學意義(P<0.05)。郊區和市區不同碘營養狀態的成年人TPOAb、TGAb陽性率比較,差異均無統計學意義(P>0.05),見表3。

表1 男、女性成年人年齡、UIC及甲狀腺功能相關指標等比較

表2 郊區及市區成年人UIC及甲狀腺功能相關指標比較

表3 郊區及市區不同碘營養狀態的成年人UIC及甲狀腺功能相關指標比較
2.4 回歸分析TPOAb、TGAb陽性及影響TSH、T3、T4水平的危險因素
logistic回歸分析結果顯示,性別是TPOAb和TGAb陽性的主要危險因素(OR=2.483、4.317),見表4。線性回歸分析結果顯示,居住地點和年齡是影響TSH水平的危險因素(P<0.05);居住地點、年齡、BMI和吸煙是影響T3水平的危險因素(P<0.01);居住地點、性別和BMI是影響T4水平的危險因素(P<0.05),見表5。

表4 logistic回歸分析TPOAb,TGAb陽性的危險因素

表5 線性回歸分析TSH、T3、T4的危險因素
3 討 論
近20多年來我國實行了全民加碘政策及食鹽加碘濃度的下調。本研究的開展可以了解上海市成年人碘營養狀態及其與甲狀腺功能的關系。共納入了2 073例上海市區和郊區成年人,研究發現上海成年人UIC為195.50 μg/L,接近碘適量的上限。郊區成年人UIC為碘適量,而市區成年人UIC為碘超足量;女性成年人UIC為碘適量,男性成年人UIC為碘超足量。2009年,上海市的調查研究表明UIC為146.7 μg/L[7]。到2015年上海市開展的流行病學調查結果顯示18歲以上男性和女性UIC中位數分別為215.4 μg/L和186.1 μg/L[8]。與本研究結果比較接近(男:204.30 μg/L 女:189.10 μg/L)。
2009年上海市碘缺乏(UIC<100 μg/L)和碘過量(UIC>300 μg/L)的比例分別為28.6%和10.1%[7]。2016年中國十城市甲狀腺疾病流行病學調查發現,上海人群中碘缺乏的比例為18.8%[5]。本研究結果顯示,上海市碘缺乏和碘過量的比例分別為8.32%和22.43%。可以看出從2009-2019年上海市碘缺乏人群的比例呈逐漸下降趨勢。但是在碘缺乏糾正的同時,碘過量人群的比例逐漸升高。有研究表明,上海各年齡段人群膳食主要來源中,碘鹽的貢獻率均在50.0%左右。其他貢獻比較多的食物包括海帶紫菜(7.6%~16.6%),肉蛋(7.1%~12.7%),魚蝦(4.5%~7.4%),最少的包括谷類(1.7%~4.9%) 蔬菜(1.3%~2.4%)[8]。同時該研究發現,上海成年人消費較多動物性海產品,但是由于動物性水產品中碘含量較低,因此,對UIC的貢獻率較低。飲水中碘含量較低,因此,水對上海成年人碘的貢獻也有限。
碘與甲狀腺疾病密切相關。有研究表明,過量的碘抑制自噬促進甲狀腺濾泡細胞凋亡,因此與橋本甲狀腺炎的發生有關[9]。碘過量增加甲狀腺內Th17細胞浸潤,抑制調節性T細胞發育,誘發甲狀腺細胞內腫瘤壞死因子α(TNF-α)相關凋亡誘導配體,因此導致凋亡和實質性破壞[10]。在既往碘缺乏地區補充碘之后,甲狀腺自身抗體的陽性率會升高[11]。提示體內碘營養狀態的改變會影響甲狀腺自身免疫。本研究發現,在郊區和市區不同碘營養狀態的人群中TPOAb和TGAb的陽性率比較差異無統計學意義(P>0.05),提示可能在整體碘營養狀態適量的情況下,對甲狀腺自身抗體的陽性率無明顯影響。
在既往的研究中,本課題組發現UIC降低與自身免疫性甲狀腺疾病密切相關(OR=1.50,95%CI:1.10~2.05,P=0.01)[12]。TENG等[13]曾經對不同UIC的地區進行前瞻性隨訪研究,結果顯示碘超足量地區和碘過量地區亞臨床甲減的發病率分別升高11.3倍和12.6倍,自身免疫性甲狀腺炎的發病率分別升高4.4倍和5.5倍。2016年發表的中國十城市甲狀腺疾病流行病學調查也證實碘超足量地區的臨床甲減、亞臨床甲減和甲狀腺自身抗體的患病率均明顯高于碘充足地區。其中在上海人群中UIC為170.20 μg/L[5]。但是本研究顯示上海人群UIC為195.50 μg/L,較之前的報道有所升高。由此可以看出,碘攝入量與自身免疫性甲狀腺疾病呈現U型曲線的關系。
過量的碘攝入會引起Wolff-Chaikoff效應,導致甲狀腺激素合成短暫性減少[14]。在易感人群中,如自身免疫性甲狀腺疾病患者,有甲狀腺手術史患者,131I或者抗甲狀腺藥物治療的Graves病患者等,會出現碘誘導的甲減。其具體機制尚不明確,可能與無法適應急性Wolff-Chaikoff效應有關。而在另外一些易感人群中,過量的碘攝入提供了合成甲狀腺激素的豐富原料而導致碘誘導的甲亢。這種碘誘導的甲亢可能是短暫性的,也可能是永久性的。其危險因素包括非毒性或彌漫性結節性甲狀腺腫,潛伏性Graves病和長期碘缺乏[15]。
本研究發現,上海郊區和市區成年人在TGAb陽性率比較差異無統計學意義(P>0.05)。而甲狀腺自身抗體與性別和年齡密切相關[16]。2018年的meta分析研究顯示補充維生素D可以在短期內降低血清TPOAb和TGAb滴度[17]。2019年一項橫斷面研究顯示,吸煙與TPOAb水平的下降有關(β=-0.287)[18]。WU等[19]在2020年TIDE研究中發現,TPOAb/TGAb陽性組的BMI明顯高于TPOAb/TgAb陰性組。因此,在logistic回歸分析中調整了居住地、年齡、性別、BMI、維生素D和吸煙。研究發現相較于碘適量,其他不同的碘營養狀態并不會增加TPOAb和TGAb的陽性率。
碘營養狀態除了與甲狀腺疾病密切相關之外,也會帶來其他危害。有研究表明,碘缺乏與心血管結局呈負相關[20]。UIC降低是血脂紊亂和心臟代謝生物標志物異常的危險因素[21]。并且UIC與高尿酸血癥和痛風呈負相關[22]。美國的一項研究表明,過量碘暴露(UIC≥400 μg/L)的個體全因死亡率較UIC正常(UIC 100~299 μg/L)的個體明顯升高(HR=1.19)。而UIC降低(UIC<100 μg/L)與病死率的增加無明顯相關[23]。
本研究尚存在一些局限性。(1)本研究為橫斷面研究,缺乏長期隨訪數據;(2)本研究為社區整群抽樣,因此選取的人群年齡偏大,本課題組根據2018年上海市黃浦區和奉賢區成年人口的比例將碘營養狀態在人群中的比例進行了校正;(3)本研究未涉及重點人群如兒童及孕婦的碘營養狀態。
綜上所述,上海成年人整體處于碘適量狀態,其中市區成年人處于碘超足量狀態,郊區成年人處于碘適量狀態。不同碘營養狀態的成年人TPOAb及 TGAb陽性率比較無明顯差異。因此,碘攝入狀態與甲狀腺自身抗體之間的關系,需要進一步隨訪。

