小兒肝移植的圍術期管理研究進展
徐艷,張勤,何重香,任艷偉,曾志貴,孫麗瑩,朱志軍,葉啟發,3 (.武漢大學中南醫院,武漢大學肝膽疾病研究院,武漢大學移植醫學中心,國家人體捐獻器官獲取質量控制中心,移植醫學技術湖北省重點實驗室,湖北省天然高分子生物肝臨床醫學研究中心,湖北省天然高分子基醫用材料構建工程技術研究中心,湖北 武漢,43007; .首都醫科大學附屬北京友誼醫院肝臟移植中心,北京,00050; 3.中南大學湘雅三醫院,衛生部移植醫學工程技術研究中心,湖南 長沙,4003)
小兒肝移植是治療兒童膽汁淤積性疾病和遺傳代謝性疾病的有效手段。由于我國兒童逝世后器官捐獻不足,親屬活體肝移植是我國目前小兒肝移植的主要器官來源。隨著免疫抑制劑、移植術后管理及治療方案的不斷改進,小兒肝移植術后存活率、生存質量和移植物存活率在不斷提高。小兒肝移植術不僅需要移植醫師精湛的技術,還需麻醉科、超聲科、影像科、輸血科及護理團隊等多學科的緊密合作與支持。本文對小兒肝移植的圍術期管理,包括鎮靜鎮痛、抗凝劑使用、液體和營養管理、免疫抑制劑管理、感染控制、移植術后并發癥及出院隨訪7 個方面進行綜述,為臨床小兒肝移植圍術期的管理提供參考經驗,以期進一步改善小兒肝移植患者的預后。
1 術前評估與準備
1.1 配型評估:小兒肝移植術前需謹慎進行術前評估,首選親屬活體器官捐獻,如無合適親屬捐獻,方可考慮公民逝世后器官捐獻[1]。相比公民逝世后器官捐獻,親屬活體器官捐獻的器官功能相對較好,且器官配型相容性更高,長期、短期預后也更好[2]。對不滿1 歲的兒童因其發育系統不完善,血型抗體滴度較低,行血型不合的肝移植術不會增加患兒在圍術期并發癥、急慢性排斥反應和長期預后方面的差異,但對血型抗體滴度大于 1 ∶64或超過1 歲的患兒進行血型不合的肝移植術時,需通過血漿置換、抗 CD20 單克隆抗體或脾臟切除(>4 歲),將血漿抗體滴度降至1 ∶8 以下,抑制體液排斥反應的發生,長期預后與血型相合移植患兒無明顯差異[3-4]。
1.2 術前感染防治:肝移植術后感染是肝移植術后的主要并發癥及死亡的重要危險因素。由于患者術前存在潛在感染的可能,而手術應激和術后免疫抑制劑的使用,均可增加術后的感染復發風險、甚至直接導致患者死亡。因此,移植術前感染篩查尤為重要,主要包括病毒、細菌、真菌及寄生蟲、免疫接種4 個方面。相比成人,小兒肝移植術后更容易發生巨細胞病毒(cytomegalovirus,CMV)和EB 病毒感染,在患兒移植術前完善供受者病原學篩查可以進一步降低患者感染風險。在患兒移植前完善免疫抑制方案設計可降低移植術后移植物功能損傷、移植物失功風險,因此在小兒肝移植術前應積極設計免疫抑制治療方案[5]。
1.3 營養狀況評估:營養不良會導致小兒肝移植術后的預后不良,尤其是增加了并發癥的發生率,如腹腔積液、感染、肝腎綜合征以及糖尿病等[6],故而移植術前的營養狀況評定顯得尤為重要。營養評定方法通常分為5 個方面,包括人體測量、實驗室指標、臨床情況、膳食和家庭環境情況,通過這5 個方面的評估對患兒營養風險進行綜合評定[7]。
1.4 重要臟器功能評估
1.4.1 肝功能評估:小兒終末期肝病模型(model for end-stage liver diseas,MELD)評分與Child-Pugh分級對小兒肝移植患者而言更能準確全面地反映終末期肝病嚴重程度。MELD 評分越高,患兒在未來3 個月內的病死率越高。因此可以使用PELD 評估患兒對肝移植需要的緊迫程度,對于PELD 評分高的患兒可以盡早進行肝移植手術[8]。
1.4.2 心功能評估:小兒肝移植術對患兒心功能有一定的影響,因此,在移植術前需完善患兒心功能檢查,如心電圖或超聲心動圖。如考慮在小兒肝移植過程中進行門體分流,應進一步對患者進行直立位血氧飽和度測定[9]。
1.4.3 神經功能評估:兒童肝性腦病是由肝功能異常導致的神經、精神綜合征,預后通常較差。大約80%的3 期、4 期肝性腦病患兒會出現腦水腫,而且病情通常進展迅速,引起大腦缺氧性損傷,甚至可能會造成腦疝等嚴重并發癥[10]。對這類肝性腦病昏迷的患兒需盡快完成術前評估及術前干預,盡量降低顱內壓和血氨濃度,并盡快安排移植手術。
2 圍術期管理
2.1 鎮靜鎮痛:鎮靜鎮痛是術后有機械通氣需求患兒保持舒適與安全的關鍵。肝移植術后患兒在重癥監護病房(intensive care unit,ICU)停留期間應給予鎮痛鎮靜治療,以減少術后軀體不適,降低心理創傷,防止術后意外事件,減輕氧耗,并促進器官功能恢復[11]。臨床常用鎮痛藥物為芬太尼、舒芬太尼及嗎啡;常用鎮靜藥物為咪達唑侖、地西泮、苯巴比妥及水合氯醛[12]。但這類藥物的不良反應通常較多,近年來,由于右美托咪啶的安全性較高,因此在患兒圍術期的應用逐漸增多[13]。右美托咪啶沒有明顯呼吸抑制,且鎮靜效果較好。但是使用右美托咪啶也可能會引起心率、血壓下降,因此,在用藥期間需監測患兒生命體征變化。臨床常用Ramsay 評分量表評估患兒鎮痛鎮靜期間使用效果[9],Ramsay 評分總分為 1 ~ 6 分,1 分表示患兒出現躁動、焦慮狀況;6 分表示患兒處于麻 醉、深睡狀況,評分越高,患兒鎮靜效果越佳[14]。
2.2 抗凝藥物使用管理:肝移植術后血管相關并發癥是一類主要的并發癥,以動脈內血栓形成為主,且通常預后不良。小兒肝移植術后肝動脈血栓形成的發生率高于成人,主要是因為兒童血管管徑纖細,吻合難度高,解剖變異多,并且患兒通常獲得性蛋白 S、蛋白 C 及抗凝血酶缺乏,因此移植術后通常表現為高凝狀態[15]。肝移植術后患兒發生血管并發癥以肝動脈血栓及門靜脈血栓形成為主,因此,患兒肝移植術后需常規行預防性抗凝治療。大部分研究認為,小兒肝移植術后早期抗凝方案首選普通肝素[15-16],術后1 ~2周內持續使用肝素鈉經中心靜脈靜脈泵入,起始劑量為10 U/(kg·h),最大劑量 為20 U/(kg·h)[8],將患者活化部分凝血活酶時間(activated partial thromboplastin,APTT)維持在50 ~ 80 s,凝血酶原國際正常化比值(international normalized radio,INR)維持在1.25 ~ 1.50,凝血酶原時間 (prothrombin,PT)維持在正常值的1.5 倍內[17]。在患兒肝移植術后1 ~ 2 周后逐漸改為口服華法林或阿司匹林抗凝藥。靜脈輸注抗凝劑期間需嚴密監測APTT、INR、PT 及血紅蛋白,必要時增加血栓彈力圖檢測。術后1周內每天行B 超檢查監測移植肝各吻合管道通暢情況,后期定期復查或必要時復查。
2.3 營養支持:營養不良可以導致患兒預后不佳,并增加并發癥發生率[18]。積極治療營養不良能顯著提高患兒的術后總體生存率[19],因此移植術后需及時對患兒進行營養風險評估。小兒肝移植術后早期營養干預包括提升能量需求、減少吸收不良、糾正厭食等[20]。移植術后患兒的營養支持主要包括腸外營養(total parenteral nutrition,TPN)和腸內營養(enteral nutrition,EN)。患兒肝移植術后早期每日輸注5%葡萄糖量5 ~ 6 g/kg 適宜,使用輸液泵24 h勻速輸注,同時使用微量泵泵注胰島素調控血糖。為維持血漿蛋白水平,每天按1 ~ 2 g/kg 補充白蛋白為宜。高鈉和低鉀血癥是小兒肝移植術后電解質控制重點[21]。EN 是一種安全有效、符合生理狀態的營養支持方法。小兒肝移植術后若無臨床禁忌,患兒術后24 ~ 48 h 開始早期EN 不會增加胃腸功能負擔。EN 喂養順序遵循低濃度流質飲食、軟食,少食多餐,循序漸進。
2.4 免疫抑制劑管理:免疫抑制劑是影響移植術后患兒生活質量及移植物存活率的重要因素。免疫抑制劑使用遵循藥物劑量最小化原則和個體化用藥原則,根據患兒原發病及實際健康情況對免疫抑制劑進行調整和選擇,選擇最適合患兒的免疫方案。免疫抑制劑經典方案通常包括:鈣調磷酸酶抑制劑(calcineurin inhibitor,CNI)(他克莫司或環孢素)、細胞增殖抑制劑(MMF 或硫唑嘌呤)和糖皮質激素(潑尼松或甲潑尼龍)[22]。首選以FK506 作為基礎免疫抑制劑,并根據患兒個體情況加用嗎替麥考酚酯(MMF)和糖皮質激素[23]。考慮到 MMF 類藥物有影響兒童生長發育的風險,因此,僅在患兒不能耐受 CNI 相關不良反應(如癲癇及腎臟毒性等)、需停用或減量 CNI時加用[9]。術中無肝期甲潑尼龍的使用劑量為10 mg/kg,術后第一天靜脈注射糖皮質激素劑量為4 mg/(kg·d),每日遞減至術后 1 周更換為口服制劑 ,盡早撤除糖皮質激素[24]。激素的應用會增加患兒的食欲,降低脂肪氧化、增加脂肪堆積,最終導致其體質量過重,所以盡早停用激素是值得推薦的[25]。免疫抑制過度使用易導致兒童圍術期出現感染,為動態平衡免疫抑制和移植感染,兒童移植術后需嚴密監測血藥濃度和感染指標,如出現感染加重時,需減量或停用免疫抑制劑的使用[9]。
2.5 感染防控:免疫抑制劑的使用是移植術后感染的直接危險因素,合理預防、治療小兒肝移植術后感染是改善患兒預后的關鍵。小兒肝移植術后抗感染治療應對每位患兒進行個體化治療,根據患兒癥狀、血培養結果及感染源的控制情況綜合決定[9]。小兒肝移植由于膽腸吻合難度較大存在一定的腸道損傷風險,患兒真菌感染的風險通常較高,因此應預防性使用抗真菌藥物。在未明確有真菌感染的情況下,為減少潛在的肝功能損害及藥物相互作用風險,預防性抗真菌治療1 周后應停用或降階梯使用抗真菌藥物[9]。CMV 和EB 病毒感染是兒童肝移植術后最常見的病毒感染類型,應預防性使用更昔洛韋治療3 ~ 6 個月,并密切監測CMV 血清檢測[26]。患兒EB 病毒感染與移植后淋巴增殖性疾病的發病密切相關,移植術后需密切監測EB 病毒的血清學檢測,警惕 EB 病毒引起移植后淋巴增殖性疾病的發生[27]。
2.6 并發癥管理:肝移植術后常見并發癥包括血管并發癥、膽道并發癥、排斥反應、肺部感染、小肝綜合征、出血及急性腎功能衰竭等。兒童各器官系統發育不完善,肝移植術后并發癥較多,且兒童血管直徑纖細,吻合難度大,因此小兒肝移植術后尤以血管并發癥多見[28]。小兒肝移植術后常見并發癥的監測及處理見表1。

表1 兒童肝移植術后常見并發癥的監測及處理
2.6.1 血管并發癥:包括動脈血栓、門靜脈脈狹窄或血栓和靜脈流出道梗阻,其中動脈血栓最常見且最嚴重,多發生于移植術后1 周左右,與移植物的失功和患兒的病死率密切相關;與之相反,靜脈并發癥往往發生在移植術后晚期,且與移植物的失功或患者病死率關系并不密切[6]。超聲檢查對肝動脈血栓檢測的靈敏度較高,是首選的影像學檢查手段,必要時可行肝血管造影等有創性檢查或手術探查[29]。如超聲檢查懷疑患兒門靜脈狹窄時建議行CT血管成像,門靜脈造影是目前診斷門靜脈狹窄的金標準[9]。
2.6.2 膽道并發癥:主要包括膽道狹窄和膽瘺,多發生于移植術后1 周左右。肝動脈狹窄或血栓、冷缺血時間過長及排斥反應是發生膽道狹窄的重要因素,膽道造影是診斷膽道狹窄的金標準。小兒肝移植術后膽瘺多見于肝切面和膽腸吻合口處,以吻合口瘺較常見。影像學檢查對于膽漏的早期診斷和治療很重要,少量膽瘺患兒可予暫觀或留置引流管,嚴密觀察患兒腹痛及引流液情況,膽瘺嚴重者應積極行手術探查[9]。
2.6.3 排斥反應:根據排斥反應發生的時間、病理檢驗及臨床表現,排斥反應分為超急性排斥反應、急性排斥反應和慢性排斥反應。兒童肝移植登記系統顯示,排斥反應的發生率隨著兒童月齡的增長逐漸增加,如<1 歲和≥1 歲患兒的排斥反應發生率分別為43.8%和57.9%[30]。
2.6.4 肺部感染:小兒肝移植術后感染多見于肺部感染、腹腔感染和血流感染,其中以肺部感染最為常見。肝移植術后肺部感染癥狀體征有:① 患兒出現咳嗽、咳痰、肺部啰音等肺部癥狀體征,同時伴有發熱或白細胞計數升高;② 肺部影像學提示肺部炎性浸潤性病變[31]。小兒肝移植術后在常規預防性使用廣譜抗菌藥物的同時,給予拍背咳痰、霧化吸入等護理措施能促進痰液排出,改善肺部感染癥狀。
2.6.5 小肝綜合征:是導致原發性移植肝無功能的主要原因之一,影響活體肝移植效果的主要因素是移植物體積絕對或相對過小,易發生小肝綜合征(small-for-size syndrome,SFSS)。小兒受者供肝質量與受者體重比正常值為2%~4%[32-33],過小的移植肝不能滿足患兒的功能需要 ,引起移植肝功能障礙 ,表現為術后持續性膽汁淤積 、凝血功能紊亂、門靜脈高壓、頑固性腹水和肝性腦病[34]。
2.6.6 出血:包括腹腔出血和消化道出血,血管吻合口縫合不佳、患兒凝血功能差及腹腔感染是腹腔出血主要因素,研究報道其發生率為4.9% ~13.0 %[35],隨著小兒肝移植手術技術日趨完善,腹腔出血發生率逐漸減少。少數患兒因肝炎復發造成肝硬化導致食管胃底曲張靜脈出血;另一方面,由于患兒移植術后長期服用免疫抑制劑和糖皮質激素類藥物,引起消化系統潰瘍,造成消化道出血。
2.6.7 急性腎功能衰竭:急性腎功能衰竭是肝移植手術后的普遍并發癥之一,增加患者的住院時長并增加感染風險,降低了患者遠期存活率,且病死率與殘疾率都極高[36]。因經典原位肝移植手術完全阻斷下腔靜脈,無肝期腎臟血流量減少、灌注壓下降,對腎臟功能影響較大,且患兒下腔靜脈纖細,因此建議小兒肝移植常規進行背駝式肝移植以降低術后急性腎衰竭風險[37-38]。
3 出院隨訪
小兒肝移植是終末期肝病患兒的最佳治療方法,術后的長期生存率與規律的定期隨訪密切相關[39]。制訂隨訪計劃是患兒能夠按時隨訪的前提,完善的管理體系和科學有效的評價指標是完成高質量隨訪的保障[40]。隨訪內容主要包括隨訪項目及頻率、免疫抑制劑服藥依從性、生活指導、生長發育及心理干預等方面。
3.1 隨訪項目及頻率:兒童肝移植受者主要隨訪項目及頻率[41-42]見表2。
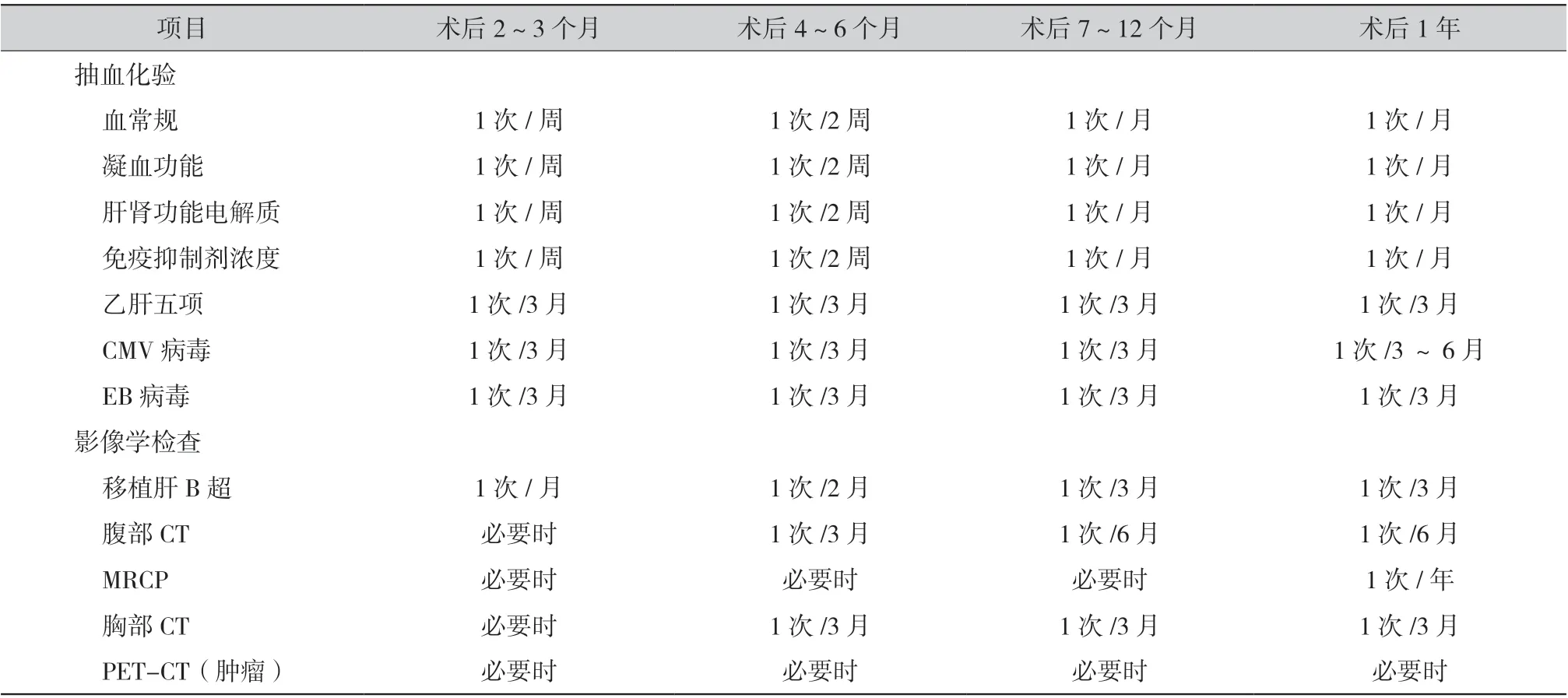
表2 兒童肝移植受者主要隨訪項目及頻率
3.2 免疫抑制劑服藥依從性:服藥依從性差是導致兒童肝移植術后遠期死亡的主要因素之一, 患兒未按時服用免疫抑制劑引起排斥反應的發生, 是導致移植物死亡的主要原因[43]。患兒移植術后出現依從性低,其危險因素有家庭貧困[44]、不愿服藥史、藥物濫用、單親家庭以及接受公眾的幫助等[45]。父母是兒童肝移植家庭的主要健康管理者[46],在移植術后隨訪階段,醫務人員向患兒及照護者做好宣教隨訪,灌輸免疫抑制劑服用及隨訪的重要性。
3.3 生活指導 包括飲食、活動及環境3 個方面。移植術后患兒因服用激素類藥物引起食欲增加,體重增長較快,應少食多餐,避免暴飲暴食等不良生活習慣。長期使用免疫抑制劑和肝功能下降都會引起患兒機體對鈣離子吸收減少,導致骨質疏松, 表現為腰疼、 骨關節痛及手足抽搐[46]。奶制品是鈣的最好來源,補鈣的同時注意補充維生素D,多進行戶外活動。兒童肝移植術后運動應循序漸進,會走路的兒童可從散步開始,后逐漸加大運動量,至體力逐漸恢復。患兒居住環境應保持干凈整潔,不接觸寵物及花草,外出戴口罩。保持良好的生活習慣,遵循有效的飲食指導,能提高患者的生活質量,減少免疫抑制劑引起的并發癥, 保持移植后肝功能的穩定[47]。
3.4 生長發育及心理干預:評估兒童生長發育指標包括身高、體重、頭圍、胸圍及皮下脂肪等。有研究[48]指出,存活期長的肝移植術后患兒會出現以脂肪質量增加為主并伴隨體細胞質量降低的現象,而自身生長發育卻不理想,因此評價生長發育狀況不能單看體質量[49]。肝移植術后患兒術后生長發育情況可以評價肝移植手術對于追趕性生長的貢獻度,有利于及時實施針對性干預[50]。對于年齡較小的幼兒,照護者在其成長過程中逐步告知,使其逐步接受和適應,養成一個良性認知理念;對于大齡兒童,似懂非懂時期,父母應正確引導,以鼓勵性語氣當面溝通交流。部分兒童受者到青春期階段可能產生叛逆心理,妨礙醫療依從性,應循序善誘,加強疏導[41]。

