ISO15189認可準則在免疫組化質量管理中的應用
張曉琴,高艷,王瑩,申寧寧,原偉成,張王亮,王晨
(山西醫科大學第二醫院,山西 太原 030001)
《醫學實驗室質量和能力認可準則(ISO15189)》(以下簡稱ISO15189)是當前全球公認的醫學實驗室質量管理標準。在我國的醫學檢驗領域,較多的檢驗科已建立了完善的質量管理體系并獲得中國合格評定國家認可委員會(CNAS)認可。2009年3月國家衛生計生委關于《病理科建設與管理指南(試行)》相關規定發布,病理科質量安全和質量管理受到越來越多的重視[1]。隨著精準醫學時代的到來,病理診斷作為疾病診斷的金標準,日益受到臨床學科的重視和依賴[2]。免疫組化室作為病理科重要的組成部分,是病理診斷堅實的基石和可靠的技術保障。我院病理科免疫組化實驗室從2017年10月開始,逐步將ISO15189中的相關要素運用到實驗室的管理中,提高了免疫組化制片質量,增強了醫技之間的互信,提升了實驗室的質量管理水平,工作更加科學規范有序。
1 材料與方法
1.1 材料
收集山西醫科大學第二醫院病理科2017年4月—2017年9月的免疫組化數據23 864 例為質量改進前組(Q組),2017年10月—2018年3月的免疫組化數據22 712 例為持續改進動態觀察組(G組),2018年4月—2018年9月的免疫組化數據34 282 例為質量改進后組(H組)。
1.2 方法
2017年10月—2018年3月按照ISO15189的質量管理要素,對免疫組化室進行規范的質量管理。對質量管理持續改進期間(G組)每月的免疫組化質量做動態觀察;對比分析Q組與H組的切片質量和數據。評片工作由一線診斷醫師在日常診斷工作中進行,錄入系統;對于不合格切片,免疫組化室技術員返工復染,并登記復染原因。免疫組化優良率=免疫組化優良切片數量/免疫組化切片總數量×100%;免疫組化復染率=免疫組化復染切片數量/免疫組化切片總數量×100%。
1.3 評價標準
免疫組化切片的評價標準分為優良、合格、不合格三個級別。優良:切片完整,裱貼牢固,無明顯皺褶,免疫組化著色定位準確無背景;合格:切片完整,裱貼較牢固,存在皺褶,免疫組化染色定位準確,或存在一定背景著色,不影響結果判讀;不合格:切片不完整,脫片嚴重,免疫組化染色定位不準或出現異常表達,背景著色嚴重以及各種原因造成醫師判讀產生困惑,導致復染。
1.4 統計學方法
采用SPSS13.0系統軟件進行統計學分析。質量改進前后免疫組化質量(優良率和復染率)比較采用χ2檢驗,G組免疫組化質量動態觀察中切片質量優良率與觀察時間采用Spearman秩相關分析。P<0.05為差異有統計學意義。
2 結 果
2.1 質量改進前后兩組切片優良率和復染率比較
免疫組化切片優良率:H組為91.1%(31 216/34 282),Q組為78.2%(18 656/23 864),兩組比較,χ2=1 912.51,P<0.001,差異有統計學意義。復染率:H組為0.4%(152/34 282),Q組為1.2%(283/23 864),兩組比較,χ2=105.8,P<0.001,差異有統計學意義。
2.2 質量管理改進中G組切片質量動態觀察
G組免疫組化切片優良率隨動態時間不斷改進,優片率大致呈逐月遞增趨勢(r=0.943,P=0.005)(見圖1)。
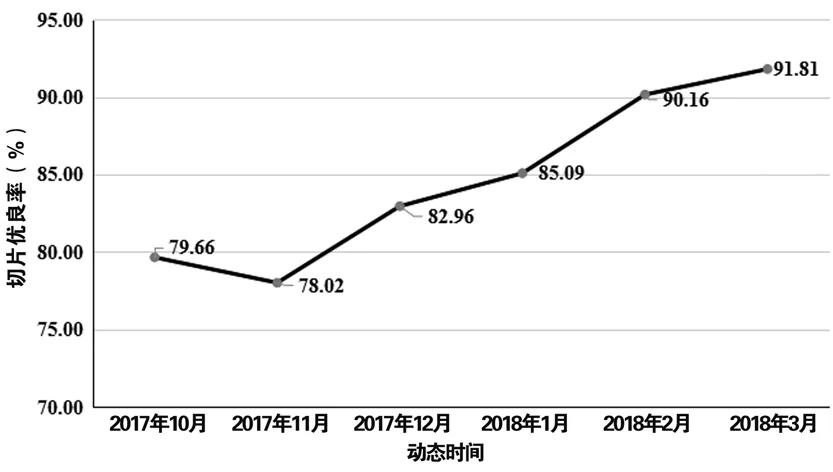
圖1 G組免疫組化切片質量動態觀察
3 討 論
3.1 影響免疫組化染色質量的原因
在質量管理改進前的Q組中,影響切片質量甚至不合格被要求重復染色的因素較多,主要為組織的前期處理不當,影響了部分抗體的表達,甚至造成脫片;各種原因導致的表達異常(組織中內對照未呈現預期陽性、非特異著色、陽性異位表達等);試劑管理混亂,使用了失效或過期試劑,無法溯源;染色結果與病理醫師的診斷思路相左而被要求復染;病理醫師對醫囑的修正未能及時與技師溝通,導致執行出現偏差;對技術員缺乏系統的理論培訓和實操考核,也是影響實驗結果穩定性的重要因素。運用ISO15189中的要素,通過質量管理持續改進后的H組,對免疫組化實驗室進行全方位管理,上述因素得到有效控制,使切片優良率大幅提升,大大減少了實驗前、實驗過程和實驗結果的不確定性,也使免疫組化切片的復染率顯著降低。
3.2 質量持續改進中切片質量動態觀察分析
PDCA循環是美國質量管理專家戴明博士提出的一種全面質量管理應遵循的科學程序,是質量計劃的制訂和組織實現的過程[3]。在持續6 個月的實驗室整改過程中,我們遵循計劃-執行-檢查-處理(PDCA)質量循環,對影響制片質量的多種因素進行多次循環和持續改進。上一個循環中出現和遺留的問題,轉入下一個循環進一步改進,逐步提高了免疫組化片的優良率。
3.3 質量管理改進措施
3.3.1 標準作業程序文件的完善和執行
提高實驗室的質量管理水平,需完善質量體系文件,才能確保質量體系能夠長久有效地運行[4]。按照ISO15189中的管理要素,根據實驗室自身條件,建立和完善免疫組化室的程序性文件和作業指導書,并逐步完善了各種記錄[5]。工作人員嚴格按照標準作業程序(SOP)文件的要求規范操作,是穩定質量的前提。
3.3.2 人員的管理
實驗室質量管理,人員是第一要素。對此,我們依據ISO15189技術要素5.1對人員進行以下幾方面的管理。
3.3.2.1 對技術員的資質要求
技術員必須具備相關專業本科學歷,病理常規技術工作3年以上,具有病理技術專業資質。
3.3.2.2 規范對技術員的培訓
首先進行免疫組化及其相關知識的理論培訓;免疫組化SOP文件的培訓;儀器設備的使用和實驗操作的培訓;參加相關機構組織的免疫組化技術培訓并取得證書;注重個人能力的培養,逐步了解和掌握各種標記物在組織和細胞中的定位和表達,掌握判斷真假陽性的經驗和技能,有利于對實驗過程和結果進行分析和評估。
3.3.2.3 個人技術檔案的管理
對個人信息、繼續教育培訓、能力和表現定期考核評估,歸入個人技術檔案。由實驗室管理人員對技術人員書面授權,設定工作權限。
3.3.3 儀器設備的管理
依據ISO15189技術要素5.3.1對儀器設備做以下幾方面管理。
3.3.3.1 建立儀器設備檔案
每一臺或每一類儀器設備均建立專屬檔案。重點是與廠商建立聯系,完善必要的性能驗證、維修保養、操作使用記錄。目的是實時掌握儀器設備運行狀況,保證儀器設備良好運行。
3.3.3.2 儀器設備操作培訓
技術員必須經過專業人員或帶教老師的培訓,嚴格按照設備管理程序,定期對儀器設備進行清潔維護和保養,及時做好相應記錄。
3.3.4 試劑耗材的管理
依據ISO15189技術要素5.3.2,建立《試劑耗材管理程序》,對試劑耗材進行采購、驗收、庫存和出庫的信息化管理。免疫組化試劑和耗材的特點是:品種繁多,使用頻率差異較大,工作中易疏忽,導致使用過期試劑耗材。使用電子信息管理系統,使試劑耗材的管理變得有序。對試劑耗材的使用可實時追蹤,具有可追溯性。
3.3.5 質量管理
3.3.5.1 內部質量控制
第一,標本的質量控制:離體標本及時充分固定、規范取材和組織處理程序是免疫組化實驗成功的前提。第二,試劑的質量控制:每一個批號的試劑,在購置驗收后,用已知的陽性組織,按照規范的操作流程,做試劑有效性驗證,測定最佳稀釋度和最佳實驗條件,并做詳細記錄。第三,實驗過程的質量控制:在每張載玻片上,待檢組織的遠端,裱貼同一標記物的陽性對照組織,以保證待檢組織與對照組織保持實驗條件的一致性,有利于結果的對比和判斷,尤其是相關精準診斷和靶向治療的標記物。陽性對照組織的設立,采取制作單組織和多組織芯片或多種組織制成的羊膜卷。第四,實驗結束:鏡下觀察對照組織和待檢組織染色效果,如果發現表達異常,及時追溯,或與病理醫師及時溝通,做好不良事件或異常表達記錄,便于今后分析。
3.3.5.2 外部室間質評
制訂程序化文件,每年至少2次參加國家病理質量控制中心(PQCC)或中國醫療器械行業協會病理專業委員會(CCPI)組織的免疫組化室間質評,驗證能力,體現水平,保證質量,循序漸進,完善質量管理體系。2017年10月以前,我們的免疫組化染色除少數涉及臨床治療的關鍵性指標設立陽性對照外,大部分用于常規輔助病理診斷的指標僅僅依靠被檢組織內或許存在的陽性物質作參照。這種質控方式一度在免疫組化發展進程中被推崇和默許。當組織中缺少內對照時,難以判斷抗體是否應該表達、試劑是否有效、實驗程序是否有誤,出現問題時難以查找原因。特別是免疫組化結果與病理醫師診斷方向相左時,病理醫師更是心存疑慮,下診斷如履薄冰。因此,重復實驗時常發生。針對上述問題,我們數次派人員外出參加ISO15189的內審員培訓和實踐運用培訓,并持續改進;通過PDCA質量循環,規范組織的前期處理[6],持續提高免疫組化切片染色質量;建立醫技之間有效的溝通機制,增強醫技互信,對購進的每一批次試劑,進行有效性驗證試驗;確立每種指標的最佳實驗條件;借鑒外部的實踐經驗,逐步建立實驗室內部的陽性組織對照庫;在每張免疫組化片上標貼陽性對照組織,確保對照組織和待檢組織在實驗條件上的一致性。經過半年的努力,降低了復染率,免疫組化實驗室管理得到整體提升。

