經皮腎鏡球囊擴張術與開放手術治療移植腎術后輸尿管梗阻臨床效果比較
高紀元,范連慧
1.錦州醫科大學 研究生學院,遼寧 錦州 121001;2.北部戰區總醫院 泌尿外科,遼寧 沈陽 110016
移植腎輸尿管梗阻是腎移植術后的常見并發癥之一,嚴重影響移植腎功能,其一般發生在術后幾周或1年內[1],以術后3個月最多[2]。本研究旨在比較經皮腎鏡球囊擴張術與開放手術治療移植腎術后輸尿管梗阻的臨床效果。現報道如下。
1 對象與方法
1.1 研究對象 選取北部戰區總醫院自2010年1月至2020年12月收治的38例移植腎術后輸尿管梗阻患者為研究對象。納入標準:患者以不同程度移植腎區脹痛、尿量減少為主訴就診;經超聲、靜脈尿路造影、腰腹部CT、逆行輸尿管鏡檢查等明確診斷移植腎輸尿管狹窄。排除標準:炎癥積液及腫物壓迫移植腎輸尿管;有嚴重基礎疾病而不能耐受手術;術后失訪。將接受經皮腎鏡球囊擴張術的22例患者納入球囊組,將接受開放手術的16例患者納入開放組。球囊組中,男性14例,女性8例;平均年齡(45.27±10.72)歲;平均體質量指數(24.00±3.10)kg/m2;狹窄部位上段1例,中段7例,下端14例;狹窄原因吻合口狹窄8例,炎癥粘連10例,其他4例。開放組中,男性9例,女性7例;平均年齡(40.69±8.70)歲;平均體質量指數(25.36±2.21)kg/m2;狹窄部位上段1例,中段5例,下端10例;狹窄原因吻合口狹窄10例,炎癥粘連4例,輸尿管過長1例,其他1例。兩組患者一般資料比較,差異無統計學意義(P>0.05),具有可比性。患者及其家屬均簽署知情同意書。本研究經醫院倫理委員會批準。
1.2 治療方法
患者同種異體腎移植術后均接受他克莫司、嗎替麥考、潑尼松方案或環孢素、麥考酚鈉腸溶片、潑尼松方案抗排斥治療。
1.2.1 術前準備 完善血尿常規、凝血、血型、肝腎功離子等檢驗,行胸片、心臟超聲、心電圖檢查。術前有泌尿系感染者,待感染控制后手術;術前梗阻嚴重、肌酐較高者,行一期移植腎造瘺術改善梗阻癥狀,穩定后二期手術治療。
1.2.2 經皮腎鏡球囊擴張術 全身麻醉后,患者取截石位,腰部墊高,常規消毒鋪巾。將超聲定位穿刺針穿刺于移植腎中或上盞,拔出針芯,可觀察到流出尿液,置入導絲,用擴張器擴大穿刺通道至F24鞘管。將輸尿管軟鏡沿導絲置入,直至狹窄部位,斑馬導絲經軟鏡操作孔置入,并從狹窄部位通過。沿著斑馬導絲將輸尿管擴張球囊導管置入,在狹窄部位放置球囊,生理鹽水加壓球囊壓力至25 kPa,持續5 min,抽出球囊內生理鹽水,并繼續前移擴張,直到從狹窄部位通過,順著導絲,留置D-J管和導尿管,結束整個手術操作過程。
1.2.3 開放手術 全身麻醉后,患者取仰臥位,腰部墊高,常規消毒鋪巾。取下腹部正中切口,逐層切開皮膚、皮下組織、腹直肌,上推腹膜,顯露膀胱,探尋移植腎輸尿管口。觀察移植腎輸尿管情況,輸尿管支架管逆行入移植腎輸尿管,觀察梗阻部位。根據不同情況操作:(1)移植腎輸尿管外壁炎性粘連,周圍瘢痕組織壓迫,將狹窄部位游離松解;(2)膀胱輸尿管吻合口狹窄、輸尿管中下段狹窄,狹窄部位切除,移植腎輸尿管-膀胱重新吻合;(3)移植腎輸尿管過長扭轉,切除輸尿管至適當長度,移植腎輸尿管-膀胱吻合;(4)移植腎輸尿管狹窄中上段狹窄或移植腎輸尿管壞死,移植腎輸尿管留置過短,游離同側無腎功能的自體輸尿管,移植腎輸尿管-自體輸尿管吻合。留置D-J管、引流管、導尿管,逐層關閉腹壁。
1.2.4 術后處理 術后監測患者生命體征,給予補液、止血及抗生素預防感染等治療。球囊組術后2~3 d能自行下床后拔出尿管,開放組術后5~7 d拔出引流管、7~14 d拔出尿管。術后3~4個月門診復查,根據患者病情選擇拔出或更換D-J管。
1.3 觀察指標 比較兩組患者的圍術期指標、白細胞計數和血肌酐水平、術后并發癥發生率及復發率。復發率為無效例數占總例數的百分比。有效為臨床癥狀消失,肌酐值正常,影像學檢查未出現移植腎積水;無效為臨床癥狀復發或加重,肌酐值再次升高,影像學檢查再次出現積水。
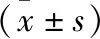
2 結果
2.1 兩組患者圍術期指標比較 球囊組手術時間、留置尿管時間、住院時間分別為(98.64±29.52)min、(4.09±1.19)d、(7.59±2.42)d,均短于開放組的(178.75±44.55)min、(14.31±3.11)d、(15.31±3.32)d,差異有統計學意義(P<0.05)。球囊組留置D-J管時間為(18.05±5.57)周,長于開放組的(13.25±3.25)周,差異有統計學意義(P<0.05)。球囊組術中出血量為(61.82±28.05)ml,少于開放組的(203.75±75.08)ml,差異有統計學意義(P<0.05)。
2.2 兩組白細胞計數和血肌酐比較 兩組術前、術后白細胞計數比較,差異均無統計學意義(P>0.05);兩組術前、術后血肌酐比較,差異均無統計學意義(P>0.05),但兩組術后血肌酐均低于術前,差異有統計學意義(P<0.05)。見表1。
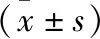
表1 兩組白細胞計數和血肌酐比較
2.3 兩組術后并發癥發生率比較 球囊組尿路感染1例、腎功能損傷1例,術后并發癥發生率為9.09%(2/22);開放組尿路感染2例、腎周積液1例、尿漏1例、腎功能損傷1例,術后并發癥發生率為31.25%(5/16)。兩組術后并發癥發生率比較,差異有統計學意義(P<0.05)。
2.4 兩組復發率比較 球囊組、開放組術后6個月復發率分別為4.55%(1/22)、0(0),差異無統計學意義(P>0.05);術后12個月復發率分別為36.36%(8/22)、6.25%(1/16),差異有統計學意義(P<0.05)。
3 討論
移植腎輸尿管梗阻的病因多為移植腎修補及手術中的不當操作。修補過程中,過多損傷腎周血管及脂肪組織可引發輸尿管缺血壞死,從而導致狹窄,Rodríguez等[3]認為,應當盡量保留腎下極副動脈和輸尿管周圍脂肪組織來保護輸尿管血供。在輸尿管與膀胱吻合時,縫合過緊、損傷輸尿管黏膜等不當操作也可促使輸尿管狹窄。此外,術后輸尿管與周圍組織粘連也可導致梗阻。
目前,治療移植腎輸尿管梗阻的方式主要有兩種—微創手術和開放手術。微創手術以順行經皮腎鏡球囊擴張術和逆行輸尿管、膀胱軟鏡等為主,鏡下找到輸尿管狹窄部位,通過放置球囊擴張、D-J管或冷刀、鈥激光電切等方式解除狹窄。但在臨床工作中,由于移植腎輸尿管與膀胱吻合的位置較高,在出現炎癥、排斥、狹窄等情況時,不易分辨移植腎輸尿管開口,導致逆行軟鏡操作難度大[4]。相對而言,經皮腎鏡順行操作較明確,成功率較高[5]。因此,本研究以順行經皮腎鏡球囊擴張術為主。在開放手術時,由于患者病因復雜,術中會因移植腎輸尿管具體情況不同而決定手術方式,主要為移植腎輸尿管狹窄段松解、狹窄段或過長段輸尿管切除—斷端吻合等。
本研究結果顯示:與開放手術比較,經皮腎鏡球囊擴張術具有術中出血量小、手術時間短及術后并發癥少等優勢,近期效果較好,但在手術12個月隨訪中的復發率較高,有患者需進行多次擴張手術,甚至開放手術解決癥狀;開放手術雖有出血量大、手術時間長及術后并發癥多等不足,但遠期復發率較低,患者生活質量較高,與既往研究[6]結果一致。因此,臨床醫師應精準把控患者病情,選擇恰當的手術方式。手術方式的選擇主要取決于輸尿管損傷和狹窄的部位、長度、嚴重程度等[7-8]。Reus等[9]認為,狹窄時間在3~6個月內或狹窄段在2 cm以內的球囊擴張效果較為理想,而狹窄持續時間>6個月或狹窄段>2 cm的治療效果較差。趙亞偉等[10]認為,狹窄時間越長,術前腎積水程度越重,球囊擴張治療效果越差。袁彪等[11]認為,球囊擴張主要適用于狹窄程度輕、良性、患腎功能良好的輸尿管梗阻患者。開放手術通常被認為是治療輸尿管狹窄的“金標準”[12]。因為開放手術術野開闊,可以明確梗阻病因,對于病因復雜的患者,可精準解除梗阻部位,遠期效果較好。
綜上所述,經皮腎鏡球囊擴張術安全、損傷小,近期效果好,可作為狹窄輕癥患者的首選方式;開放手術遠期效果好,對于病情復雜、狹窄嚴重的患者,開放手術為更優選擇。

