OCTA評價康柏西普對濕性年齡相關(guān)性黃斑變性的治療效果*
楊主敏, 黃星, 劉淑卿, 李娟娟, 王鮮**
(1.貴州醫(yī)科大學(xué)附屬醫(yī)院 眼科, 貴州 貴陽 550004; 2.云南省第二人民醫(yī)院 眼科, 云南 昆明 650021)
年齡相關(guān)性黃斑變性(age-related macular degeneration,AMD)是指由多種因素導(dǎo)致的黃斑區(qū)結(jié)構(gòu)衰老性改變[1]。根據(jù)臨床癥狀不同AMD可分為萎縮性(干性)與滲出性(濕性)2種類型,雖然臨床上常以萎縮性為主[2],濕性僅占AMD的10%左右,但濕性患者的視力喪失率卻處于極高水平[3]。濕性AMD以脈絡(luò)膜新生血管形成為主要特點,新生血管可通過破裂的Bruch膜進(jìn)入視網(wǎng)膜色素上皮下或視網(wǎng)膜神經(jīng)上皮下組織而出現(xiàn)滲出、出血及晚期瘢痕的形成,這也是濕性患者視力喪失的主要原因[4]。對于濕性AMD臨床尚無特效治療藥物,多以雷珠單抗、康柏西普等抗新生血管內(nèi)皮生長因子(VEGF)類藥物進(jìn)行治療[5]。光學(xué)相干斷層掃描血管成像(optical coherence tomography angiography,OCTA)是一種分辨率高、無需使用造影劑即可觀察視網(wǎng)膜和脈絡(luò)膜循環(huán)的新技術(shù)[6]。目前,采用OCTA評價藥物治療AMD的報道尚不多見。因此,本研究對60例(68眼)濕性AMD患者采用抗VEGF藥物康柏西普玻璃體腔注射治療,然后采用OCTA法檢測治療前后患眼的脈絡(luò)膜新生血管面積、黃斑區(qū)血流密度改變,以更直接評價玻璃體腔注射康柏西普的臨床效果,報告如下。
1 資料與方法
1.1 一般資料
選取2018年5月—2019年5月收治的60例(68眼)濕性AMD患者為受試對象,其中男33例(36眼)、女27例(32眼),左眼24只、右眼44只,年齡50~85歲、平均(65.28±8.54)歲。研究符合醫(yī)院倫理委員會制定的倫理要求,所有患者均簽署知情同意書。納入標(biāo)準(zhǔn):(1)年齡≥50歲;(2)散瞳后經(jīng)裂隙燈、眼底照相、眼底熒光血管造影等檢查診斷為濕性AMD;(3)可完成研究、并接受隨訪。排除標(biāo)準(zhǔn):(1)對造影劑過敏者;(2)既往接受過光動力療法治療、玻璃體腔注射或其他抗VEGF藥物治療;(3)既往接受過玻璃體腔注射曲安奈德、內(nèi)眼手術(shù)治療者;(4)既往有外傷史、或行眼底激光光凝治療者;(5)存在黃斑裂孔、糖尿病視網(wǎng)膜病變等其他眼底疾病者;(6)屈光介質(zhì)渾濁、對眼底成像造成嚴(yán)重影響者。
1.2 治療方法
所有患者均接受玻璃體腔注射康柏西普治療。鹽酸奧布卡因表面麻醉后,于顳下方角膜緣外3.5 mm處、與鞏膜面呈90°刺入眼內(nèi),向玻璃體腔緩慢注入康柏西普;注射完畢后,拔出并按壓30 s;測眼壓正常,以妥布霉素地塞米松眼膏涂眼包扎。術(shù)后給予妥布霉素滴眼液滴眼,1月隨訪1次,病情無好轉(zhuǎn)則重復(fù)經(jīng)玻璃體腔注射康柏西普治療。
1.3 觀察指標(biāo)
1.3.1視力改善情況 分別于治療前及治療后1個月時,采用WHO的視力分級標(biāo)準(zhǔn)對患者的最佳矯正視力(BCVA)進(jìn)行檢測,以0.5%復(fù)方托吡卡胺滴眼液散瞳,驗光確定視力。
1.3.2OCTA指標(biāo)檢測 分別于治療前及治療后1個月時,采用OCTA檢測患眼的脈絡(luò)膜新生血管面積(CNV)、中心凹淺層的黃斑厚度及血管血流密度、中心凹旁淺層的黃斑厚度及血管血流密度。
1.3.3血清學(xué)指標(biāo) 分別于治療前及治療后1個月時,取患者空腹靜脈血5 mL,分離血清,以免疫速率散射比濁法檢測血清中C反應(yīng)蛋白(CRP)水平,以ELISA法檢測血清中VEGF含量。
1.3.4不良反應(yīng)發(fā)生情況 觀察治療過程中有無視網(wǎng)膜脫離、玻璃體積血、醫(yī)源性白內(nèi)障等并發(fā)癥發(fā)生。
1.3.5治療后1個月時阿姆斯勒方格表(Amsler表)檢查結(jié)果 綜合其他文獻(xiàn)描述自擬Amsler表,檢查方格線條曲直性、粗細(xì)均勻、清晰度變化。臨床治愈為完全恢復(fù)正常,顯效為大部分癥狀改善,有效為部分癥狀好轉(zhuǎn),無效為上述癥狀無改善甚至加重。
1.4 統(tǒng)計學(xué)分析
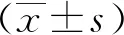
2 結(jié)果
2.1 視力、眼壓改善情況
治療后1個月時,有60只患眼的視力提高、2只患眼的視力下降、6只患眼的視力穩(wěn)定,有效率為88.24%。如表1所示,與治療前比較,治療后1個月BCVA視力明顯提高,眼壓較治療前明顯降低,差異有統(tǒng)計學(xué)意義(P<0.05)。
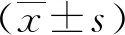
表1 治療前及治療后1個月時68只患眼的視力和眼壓比較
2.2 OCTA檢查指標(biāo)
術(shù)后1個月時,患眼的CNV較治療前縮小,中心凹黃斑厚度、中心凹旁黃斑厚度、中心凹淺層血管血流密度也較治療前減少,差異有統(tǒng)計學(xué)意義(P<0.05);但術(shù)后1個月時的中心凹旁淺層血管血流密度與術(shù)前比較,差異無統(tǒng)計學(xué)意義(P>0.05)。見表2。
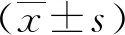
表2 治療前及治療后1個月時68只患眼的OCTA檢查結(jié)果
2.3 血清CRP、VEGF水平
結(jié)果顯示,治療后1個月時60例患者血清CRP、VEGF水平均較治療前下降,差異有統(tǒng)計學(xué)意義(P<0.05)。見表3。
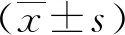
表3 治療前及治療后1個月時60例患者血清CRP、VEGF水平
2.4 并發(fā)癥發(fā)生情況
治療過程中,60例(68眼)接受玻璃體腔康柏西普注射后,有3眼出現(xiàn)結(jié)膜下出血,未給予特殊處理,1周后恢復(fù)正常,所有患眼無視網(wǎng)膜脫離、玻璃體積血、醫(yī)源性白內(nèi)障等嚴(yán)重并發(fā)癥發(fā)生。
2.5 Amsler表檢查結(jié)果
治療后1個月時,68只患眼的Amsler表方格線條曲直性、粗細(xì)均勻性、清晰度變化臨床治愈36眼、顯效26眼、有效3眼、無效3眼,總有效率為95.59%。
3 討論
AMD為導(dǎo)致老年人視力損傷的常見原因之一,根據(jù)眼底表現(xiàn)差異可分為干性AMD與濕性AMD[7]。發(fā)病初期,患者可無任何臨床癥狀,僅有視物變形、視物暗點等出現(xiàn)[8],不易與其他眼部疾病鑒別,導(dǎo)致病情遷延、延誤治療。濕性AMD的臨床治療以抗VEGF藥物為主,其中康柏西普為我國自主研發(fā)的新型人源化抗VEGF藥物,可使VEGF及其降解產(chǎn)物的活性下降,藥效可滲透視網(wǎng)膜全層。通過玻璃體腔注射給藥方式,可使藥物結(jié)合VEGF受體,抑制脈絡(luò)膜新生血管生長,從而減少、控制視網(wǎng)膜水腫及滲出[9-10]。康柏西普還可降低脈絡(luò)膜血管通透性,減輕脈絡(luò)膜血管擴張,使治療后黃斑中心凹下脈絡(luò)膜厚度下降,改善脈絡(luò)膜血管通透性、血管阻力及血流量[11],促進(jìn)疾病恢復(fù)。
既往AMD診斷依賴于熒光素鈉眼底血管造影(FFA)、吲哚青綠眼底血管造影(ICGA)等有創(chuàng)檢查,且檢查過程中需采用吲哚菁綠、熒光素等造影劑,患者可有惡心、嘔吐、過敏等造影劑反應(yīng)出現(xiàn)[11]。此外,F(xiàn)FA、ICGA提供的圖像為二維圖像,易受液體、出血、色素、纖維化等因素影響,而無法清晰顯示深層的血管異常[12]。光學(xué)相干斷層掃描(OCT)為目前AMD診斷、治療的常用成像方式,可監(jiān)測視網(wǎng)膜、淺層脈絡(luò)膜結(jié)構(gòu)變化,與FFA等傳統(tǒng)檢查相比,該技術(shù)更簡便、快捷,對患者創(chuàng)傷小,利于給醫(yī)師提供視網(wǎng)膜、脈絡(luò)膜特征性橫斷面及Enface影像[13],從而使及時作出診斷及判斷治療效果。但OCT檢查無法顯示CNV的血流狀態(tài),也無法鑒別視網(wǎng)膜下纖維化、出血、鄰近視網(wǎng)膜組織等[14-15]。OCTA為在OCT基礎(chǔ)上發(fā)展而來的新型影像技術(shù),除可提供OCT圖像外,還可顯示全層視網(wǎng)膜、淺層脈絡(luò)膜血管系統(tǒng)的血流信息。此外,OCTA具備三維重建功能,可將視網(wǎng)膜淺層、深層、淺層脈絡(luò)膜的血流信號分層顯示,從而更準(zhǔn)確反應(yīng)病灶血流情況及病灶形態(tài)[16]。
有研究表明,OCTA在監(jiān)測抗VEGF治療AMD中具有重要的意義[17-18]。通過OCTA的成像方法,可發(fā)現(xiàn)既往無法發(fā)現(xiàn)的抗VEGF治療后對視網(wǎng)膜、脈絡(luò)膜表層血流密度、CNV、中央視網(wǎng)膜厚度等變化。本研究中,OCTA觀察明確濕性AMD患者在接受融合蛋白類藥物治療后1個月時的CNV明顯較治療前減少,黃斑中心凹厚度、黃斑中心凹旁厚度均較治療前減少。中心凹淺層血流密度較治療前減少。這與Ga等[19]的研究結(jié)論一致。患者經(jīng)抗VEGF治療后視力好轉(zhuǎn),視網(wǎng)膜黃斑中心凹厚度(CRT)降低,CNV血流面積縮小。無血流信號的部位可能為無血液流動或血流速度下降致相應(yīng)部位的一部分CNV不能檢出,作者認(rèn)為該結(jié)果可提示CNV的病灶面積縮小或活動性下降,其變化對判斷CNV病灶大小或活動性的變化有一定臨床意義。說明OCTA可評估抗VEGF治療過程中的新生血管叢的動態(tài)變化,從而為臨床醫(yī)師診斷、評估治療效果提供參考。AMD發(fā)生、發(fā)展過程中,伴隨明顯的炎癥反應(yīng)及血管生成[20-21],故本研究觀察了治療后CRP、VEGF含量,結(jié)果表明康柏西普治療可抑制VEGF分泌,抑制病理性新生血管形成的發(fā)生。CRP為炎癥反應(yīng)的重要蛋白,可識別異體抗原,激活補體系統(tǒng),在受到創(chuàng)傷/刺激時含量升高。經(jīng)治療后CRP水平明顯下降,說明康柏西普可抑制AMD患者炎癥反應(yīng)。治療后視力、眼壓均有明顯的改善,且治療過程中無明顯不良反應(yīng)發(fā)生。說明融合蛋白類藥物治療濕性AMD安全可靠。
綜上所述,康柏西普治療濕性AMD,可有效改善視力、眼壓,OCTA顯示術(shù)后黃斑厚度、中心凹淺層血管血流密度較治療前減少,炎癥程度減輕,無明顯不良反應(yīng),適于在臨床推廣應(yīng)用。

