US-CT/MRI融合成像在超聲引導射頻消融顯影困難的肝癌患者中的應用價值
白云路 徐 杰 丁 遠 買豪嘉
超聲引導下的射頻消融術是治療肝惡性腫瘤的主要術式之一[1-3],具有可實時引導、無輻射、微創、療效顯著等優點,但是超聲引導時超聲影像學下肝臟組織容易受到背景組織及病灶位置等因素的影響,使得部分患者病灶不容易顯影或顯影困難,給射頻消融治療帶來難度。近年來為了解決病灶顯影困難患者的治療問題,臨床上嘗試采取超聲造影與MRI等技術進行圖像融合可提高病灶顯影清晰度,同時還能實時監測治療效果[4-6],具有更精確的特點。為此,本研究對超聲-CT/磁共振成像(US-CT/MRI)融合成像在超聲引導射頻消融顯影困難的肝癌患者中的應用價值進行了進一步研究,為肝癌患者的臨床治療提供參考,現將相關研究結果報告如下。
1 資料與方法
1.1 一般資料
選取2019年1月至12月期間在我院行超聲引導下射頻消融治療的肝癌患者84例(104個病灶)為研究對象,納入標準:①均通過活檢病理證實為原發性肝癌。②患者病情符合行射頻消融治療適應證[7]。③單發病灶直徑≤5 cm,如為多發病灶則直徑≤3 cm且數目≤3個。④病灶距離大血管距離≥0.5 cm,且距離周圍組織重要結構≥1.0 cm。排除標準:①患者有超聲造影禁忌證。②術后3個月內無法進行隨訪。③肝功能Child-Pugh分級為C級,合并遠處轉移或已經侵犯血管者。④在行超聲引導下射頻消融治療同時進行其他治療措施者。將患者根據常規超聲下顯影難度分為顯影困難組與顯影清晰組。顯影困難組共31例(37個病灶),其中男性19例、女性12例,年齡 42~75歲,平均(55.18±12.73)歲,26例為單發病灶、4例為2個病灶、1例為3個病灶,單發病灶直徑0.6~4.7 cm,平均直徑(2.74±0.52)cm,多發病灶直徑0.5~3 cm,平均直徑(1.84±0.42)cm,Child-Pugh分級A級11例、B級20例,25例合并有肝硬化;顯影清晰組共53例(67個病灶),其中男性30例、女性23例,年齡 41~72歲,平均(55.24±12.35)歲,42例為單發病灶、8例為2個病灶、3例為3個病灶,單發病灶直徑0.5~4.8 cm,平均直徑(2.76±0.50)cm,多發病灶直徑0.5~3 cm,平均直徑(1.86±0.44)cm,Child-Pugh分級A級22例、B級31例,32例合并有肝硬化。2組患者性別、年齡、病灶數量及大小、Child-Pugh分級等方面差異無統計學意義(P>0.05)。
1.2 儀器及方法
1.2.1 儀器 超聲診斷儀為GE LOGIQ E9超聲診斷儀,探頭為C1-6VN、凸陣,頻率1~6 MHZ,同時具有磁定位器及圖像融合軟件;超聲造影使用的造影劑為Bracco公司生產的聲諾維(規格:59 mg/瓶),在使用時用0.9%氯化鈉5 ml稀釋后進行造影;GE lightspecd VDT64D多排螺旋CT;MRI為Siemens3.0T TIM TRioMR成像儀。
1.2.2 方法 行肝癌射頻消融治療的醫師要求具有5年及以上肝癌消融工作經驗,超聲介入醫師要求有3年及以上融合成像工作經驗。患者術前均制定手術計劃,對常規超聲顯影清晰的患者在常規超聲引導下行射頻消融手術,術后即刻進行超聲造影檢查,觀察病灶區域消融情況,如病灶未完全覆蓋可進行補充消融。對常規超聲顯影困難的病灶,選擇行US-CT/MRI融合成像進一步對病灶的部位和范圍明確,具體為:選取能將病灶和肝內血管清晰顯影的CT/MRI序列,將DICOM格式的圖像導入超聲診斷儀內,采取內定標法中一點一面法對導入的圖像與超聲圖像進行對位融合,融合完成后超聲下參考CT/MRI圖像對圖像病灶的位置、范圍、大小等進行標記,圖像融合成功后進行射頻消融治療,同一患者具有多個病灶時,對病灶分別進行圖像對位融合,實時超聲下操作避開大血管,按照術前計劃對目標病灶進行逐針穿刺及消融,消融后即刻進行超聲造影檢查并對病灶消融情況進行評價,如病灶未完全覆蓋可進行補充消融。
1.3 觀察指標
實時觀察術中及術后有無發生出血等并發癥,在術后1個月時行UC-CT/MRI檢查,判斷肝癌腫瘤的消融情況,分為消融完全和消融不完全,如增強US-CT/MRI檢查肝癌腫瘤組織有局部殘留為消融不完全,無殘留病灶為消融完全。
1.4 統計學方法
2 結果
2.1 2組患者實施射頻消融治療情況
顯影清晰組患者均行超聲引導下射頻消融,術中有5個病灶超聲造影發現未完全覆蓋行補充消融,術后1個月時復查2個病灶未完全消融。顯影困難組有2例單個病灶患者由于病灶小、肺氣及肋骨影響出現盲區未能圖像融合成功,實際35個病灶US-CT/MIR圖像融合成功,圖像對位時間為 3.7~17 min,平均(6.19±1.98)min,最終均行射頻消融治療,術中有8個病灶超聲造影發現未完全覆蓋行補充消融,術后1個月時復查無未完全消融病灶。顯影清晰組實際完成的射頻消融率、術后完全消融率分別為100.00%(67/67)、97.01%(65/67),顯影困難組分別為94.59%(35/37)、100.00%(35/35),比較差異無統計學意義(P>0.05),顯影清晰組術中補充消融率為7.46%(5/67),顯影困難組為23.53%(8/35),比較差異有統計學意義(P<0.05),見表1。
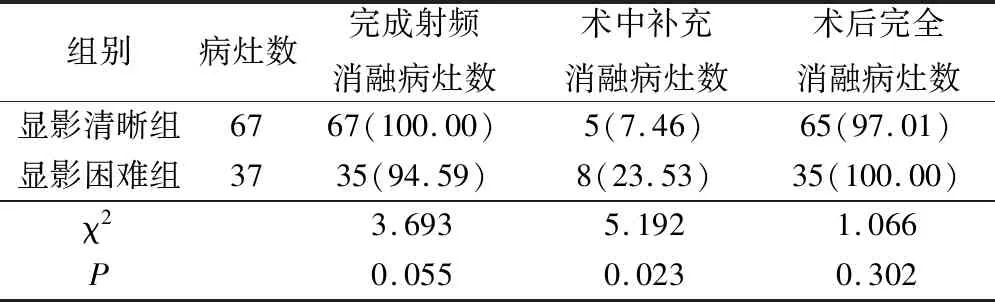
表1 2組患者實施射頻消融治療情況(例,%)
2.2 2組患者并發癥發生情況
2組患者實施射頻消融治療時均未發生大出血等并發癥。
3 討論
射頻消融是通過電極發射的高頻交變電流讓病灶內細胞電離子發生摩擦,產生熱能后細胞蛋白發生不可逆的變性壞死,從而達到治療目的,射頻消融術治療時一般并發癥少、創傷性小、恢復快,對良惡性腫瘤均有良好的治療效果[8-10],但是治療時需要對病灶進行定位,一般臨床上會選擇超聲引導下定位。超聲引導下的射頻消融治療是肝癌治療的主要方法之一,可在超聲實時引導下對病灶進行定位,實施射頻消融治療,然而部分患者超聲下對肝癌病灶并不能進行顯影或者定位,其常見的原因包括病灶被肺氣或者肋骨遮擋、患者有肝硬化背景的回聲雜亂、病灶回聲為等回聲與周圍組織界限不清影響判斷、病灶太小等[11-12],因此這部分患者往往無法實施超聲引導下射頻消融治療。
臨床上目前常用的影像學技術包括形態學成像和功能成像,形態學成像包括CT、超聲、MRI、X線等,功能成像主要包括MRI功能成像、CT灌注成像等。形態學成像技術能對病灶進行定位,解剖關系顯示好,功能成像側重于反應代謝、血流等功能信息。超聲、CT、MRI對肝癌病灶均能進行定位,各有優缺點,部分超聲無法顯影的患者CT或MRI下也能顯影,因此以上影像學技術在臨床上可互為補充。在進行射頻消融治療時CT和MRI實時引導時難度較大,因此常選擇超聲引導,而超聲引導顯影困難的患者,如果能通過CT和MRI圖像定位進行射頻消融治療,不失為治療肝癌的另一個方法。US-CT/MRI融合成像技術應運而生,成為近年來備受關注的新技術,此技術將增強CT/MRI圖像與超聲圖像進行融合,讓三種影像學技術優點融為一體,對單純超聲下無法顯影的病灶能被準確定位,因此讓無法行射頻消融治療的病灶也具備了射頻消融治療的條件,同時醫生也能避免了放射性暴露。臨床報道顯示[13-15],對較小的病灶和不典型的病灶,通過US-CT/MRI融合成像也能提高檢出率和定位率。在本研究中常規超聲顯影困難的患者病灶,通過US-CT/MRI融合成像顯影定位率達到了94.59%,另外2個病灶由于病灶小、肺氣及肋骨等多個因素的共同影響出現盲區,最終經過多次圖像融合仍然未能未融合成功,最終放棄行射頻消融治療。射頻消融技術治療的療效評價指標主要為病灶的完全消融率,如果無法做到完全消融,惡性腫瘤會復發,影響到治療效果[16-18],從目前報道的結果看[13-15],大多數肝癌病灶均能在US-CT/MRI融合成像下完全射頻消融,而且完全消融率接近100.00%。本研究中實際實施US-CT/MRI融合成像射頻消融治療的35個病灶均最終復查時病灶完全消融,成功率高。由于射頻消融需要對病灶完全覆蓋,因此需要實時觀察消融效果,從大多數報道來看[13-15],US-CT/MRI融合成像射頻消融術中補充消融率相對于常規超聲引導下射頻消融治療的術中補充消融率高,這主要是由于實時常規超聲引導下射頻消融治療的病灶顯影清晰,因此邊界等均能準確定位,而實施US-CT/MRI融合成像射頻消融治療的患者主要是常規超聲下定位困難的患者,因此及時US-CT/MRI下定位,也對邊界把握準確性存在影響,增了術中補充消融的幾率,但經過補充消融,最終均達到完全消融,因此,提示我們在進行US-CT/MRI融合成像射頻消融治療時術中即時評價消融效果是非常必要的。
綜上所述,常規超聲引導射頻消融顯影困難的肝癌患者病灶通過US-CT/MRI融合成像能清晰顯影,對位好,完全消融率和安全性高,具有較高的臨床應用價值,但其仍存在一些不足:①技術依賴于獲得 CT/MRI 的 DICOM 圖像,目前在大多數醫院尚不能普及。②圖像融合對影像學工作人員技術和經驗要求高,掌握此技術所需學習周期較長。③體內解剖結果的改變會對定位形成影響,實時精確定位效果會受到一定影響。

