基于Logistic回歸分析的丹參酮ⅡA磺酸鈉注射液致藥品不良反應影響因素分析*
徐美玲,韓寶俠,劉 玲,向光芳,茍小軍,丁春梅
(1.重慶市第四人民醫院·重慶市急救醫療中心·重慶大學附屬中心醫院,重慶400014;2.蘇州大學附屬第二醫院,江蘇 蘇州215004;3.上海市寶山區中西醫結合醫院,上海201999;4.上海市浦東新區迎博社區衛生服務中心,上海200125)
丹參制劑是丹參中二萜醌類化合物丹參酮ⅡA經磺化而得的水溶性物質[1-2],能增加冠狀動脈流量,提高心肌耐缺氧能力,改善缺氧心肌代謝紊亂,抗血栓和抑制血小板聚集[3],在抗菌、減輕腦缺血組織炎癥等方面具有一定藥理作用[4]。臨床主要用于冠心病[5]、心絞痛[6-7]、心肌梗死[8-9]、缺血性腦卒中[10-11]等的輔助治療。隨著臨床的廣泛應用,其藥品不良反應(ADR)報道也越來越多。本研究中綜合分析了236例丹參酮ⅡA磺酸鈉注射液ADR的規律和特點,為臨床合理用藥提供參考。現報道如下。
1 資料與方法
1.1 資料來源
從重慶、蘇州、上海多家醫院ADR監測管理系統中調取2014年1月至2019年12月丹參酮ⅡA磺酸鈉注射液所致ADR報告,納入給藥劑量、給藥途徑、ADR發生時間及具體表現描述均完整,排除聯合用藥情況不能明確為丹參酮ⅡA磺酸鈉注射液所致ADR的報告。
1.2 方法
采用回顧性分析法,應用Excel軟件建立丹參酮ⅡA磺酸鈉注射液ADR數據庫。對ADR發生原因進行單因素、多因素Logistic回歸分析。根據Logistic回歸分析規定,分為自變量和因變量,自變量包括患者性別、年齡、用藥過敏史、用藥時段、單次給藥劑量、溶劑量是否符合藥品說明書要求、是否聯合用藥、原患疾病共8個變量;因變量包括全身性損害、消化系統反應、皮膚及其附件反應、循環系統反應、精神神經系統共5個變量。對不同類型的變量進行標準化處理。
1.3 統計學處理
采用SPSS 23.0統計學軟件分析。計數資料以率(%)表示,ADR發生原因采用單因素、多因素Logistic回歸分析。P<0.05為差異有統計學意義。
2 結果
2.1 描述性分析
共報告ADR 236例。其中,一般ADR 114例(48.31%),新的一般ADR 117例(49.58%),嚴重ADR 1例(0.42%),新的嚴重ADR 4例(1.69%);ADR累及系 統/器 官 以 循 環 系 統(34.46%)、皮 膚 及 其 附 件(31.09%)為主。詳見表1。

表1 ADR累及主要系統/器官和臨床表現Tab.1 Main systems/organs involved in ADR and their clinical manifestations
2.2 單因素Logistic分析
ADR的發生主要集中在60歲及以上老年患者,發生概率為75.00%(177/236);發生時間集中在用藥30 min內(44.49%);溶劑量不符合藥品說明書要求的占36.86%。詳見表2。
2.3 多因素Logistic分析
Logistic回歸分析結果顯示,全身性損害ADR的發生與年齡段在50歲及以下、60~69歲、溶劑量不符合藥品說明書要求及原患疾病為冠狀動脈粥樣硬化性心臟病(簡稱冠心病)、腦梗死有關(P<0.05);消化系統ADR的發生與用藥時段在31~60 min、大于規定劑量、溶劑量不符合藥品說明書要求、聯合用藥及原患疾病為冠心病、腦梗死、腦動脈供血不足有關(P<0.05);皮膚及其附件ADR的發生與年齡段在50歲及以下、用藥時段在31~60 min及原患疾病為冠心病、腦動脈供血不足有關(P<0.05);循環系統ADR的發生與用藥時段在1~3 h、大于規定劑量、溶劑量不符合藥品說明書要求、聯合用藥及原患疾病為冠心病、腦梗死、腦動脈供血不足有關(P<0.05);精神神經系統ADR的發生與男性、大于規定劑量、溶劑量不符合藥品說明書要求及聯合用藥有關(P<0.05)。詳見表3。
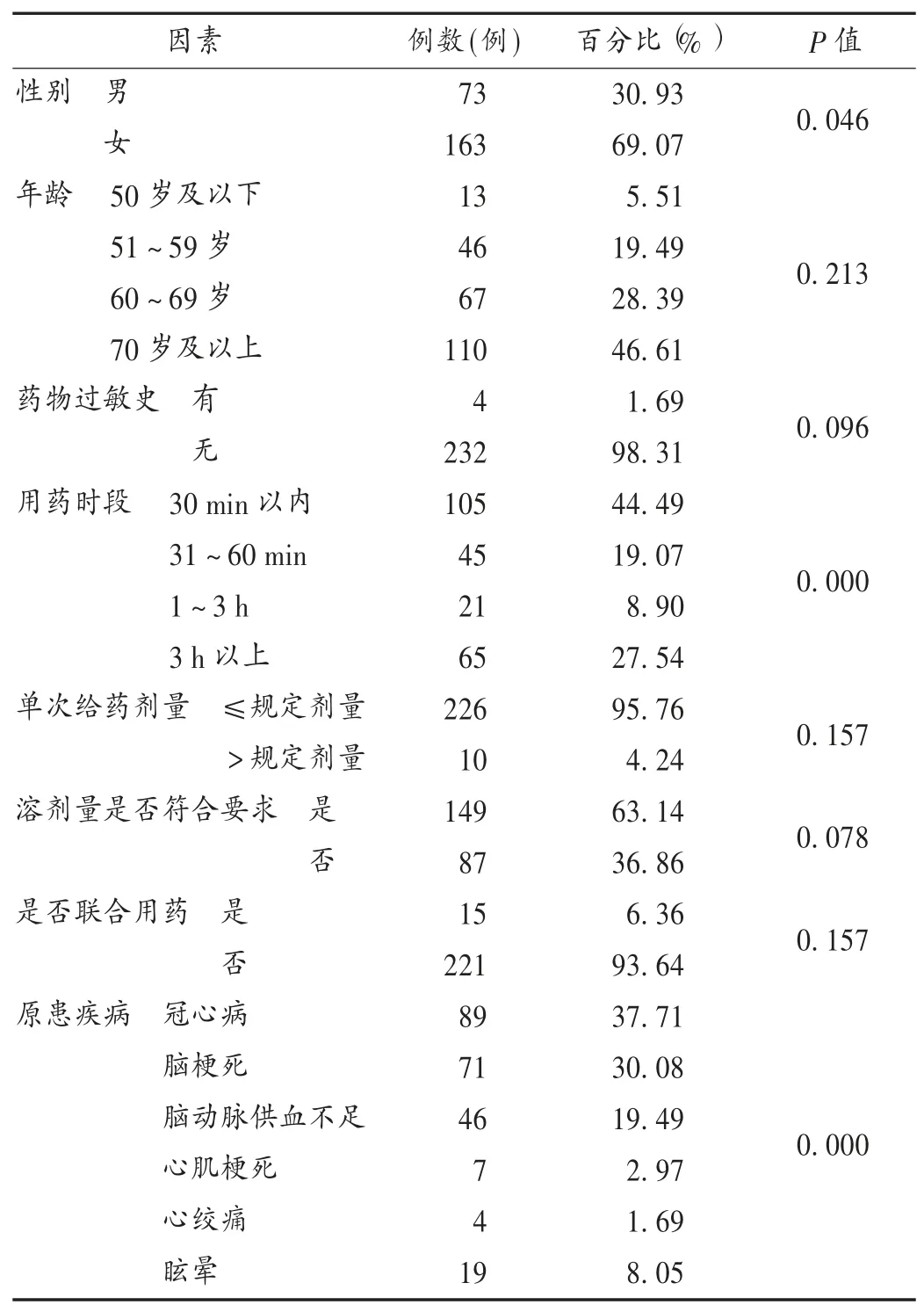
表2 丹參酮ⅡA磺酸鈉注射液ADR影響因素單因素Logistic分析(n=236)Tab.2 The Logistic regression analysis results of single factor for ADR caused by Sulfotanshinone Sodium Injection
3 討論
3.1 與性別關聯性評價
236例患者中,女性占69.07%,性別間比較有統計學差異(P<0.05)。女性患者各項生理機能較男性弱,臨床用藥時要重視其ADR的監測[12]。本研究結果顯示,性別是精神神經系統ADR的影響因素,男性是發生精神神經系統ADR的危險因素;而其他系統ADR的發生與性別均無關。
3.2 與年齡關聯性評價
丹參酮ⅡA磺酸鈉注射液ADR的發生主要集中在50歲及以上,尤其是60歲以上患者,占75.00%,這與孔飛飛等[13]的報道結果相符。根據2015年《丹參酮ⅡA磺酸鈉注射液臨床應用專家建議》(以下簡稱《專家建議》)推薦,一級推薦為心肌梗死、心絞痛、冠心病;二級推薦為缺血性腦卒中[14]。分析該藥的適應證為中老年人,且該年齡段患者易患各種心腦血管系統疾病,故用藥頻率高于其他年齡段人群,出現ADR的概率相應增加。由表3可知,年齡是全身性損害、皮膚及其附件ADR的影響因素。50歲及以下是發生全身性損害、皮膚及其附件ADR的危險因素。雖然未見高齡與丹參酮ⅡA磺酸鈉注射液安全性相關,但在臨床應用中仍不能忽視年齡因素。由于老年人機體組成成分、生物轉化、排泄及對藥物的反應均呈增齡性變化[15],該藥主要經腸道排泄,少量經腎臟排泄,對中老年患者來說一般不會造成大的影響,但對腎功能嚴重受損的高齡老年人應注意調整臨床用量[16]。同時,老年患者多合并其他基礎疾病,聯合用藥多,均可能影響用藥安全,提示該藥用于高齡患者時更應把握適應證和劑量,需密切觀察癥狀,避免ADR發生。

表3 丹參酮ⅡA磺酸鈉注射液ADR影響因素多因素Logistic分析Tab.3 The Logistic regression analysis results of multiple factors for ADR caused by Sulfotanshinone Sodium Injection
3.3 與用藥時段關聯性評價
丹參酮ⅡA磺酸鈉注射液ADR的發生時間主要在用藥30 min及以內(44.49%),與王洪銳等[17]的報道結果一致。因此,用藥后30 min應注意患者情況,出現問題應立即解決。3 h及以上發生ADR的概率占27.54%,提示臨床不應忽視患者用藥后監測,應做到及時發現,正確處理。由表3可見,用藥時段在31~60 min發生皮膚及其附件ADR的危險增加,可能是藥物中添加的助溶劑、穩定劑等成分激活了皮膚組織的H1受體,從而引起組胺釋放,使皮膚反應性增高[17];用藥時段在1~3 h發生循環系統ADR的危險增加。
3.4 與溶劑量、單次給藥劑量是否符合藥品說明書要求關聯性評價
溶劑量選擇:丹參酮ⅡA磺酸鈉注射液藥品說明書用法中支持靜脈滴注使用40~80 mg,用250~500 mL 5%葡萄糖注射液或0.9%氯化鈉注射液稀釋,36.86%的患者使用的溶劑量未達到藥品說明書要求,后續研究可關注ADR的發生是否與藥物濃度過高相關。由表3可見,溶劑量不符合藥品說明書要求使發生全身性損害ADR的危險增加,提示臨床應嚴格按藥品說明書用法用量使用。
單次給藥劑量選擇:丹參酮ⅡA磺酸鈉注射液說明書用法用量中支持靜脈滴注使用藥物劑量為40~80 mg,95.76%的患者使用劑量未超過規定劑量,但有4.24%的患者單次使用劑量超過80 mg,即這部分患者使用的藥物濃度仍高于正常濃度。由表3可見,單次給藥大于規定劑量使消化系統發生ADR的危險增加,提示應嚴格按說明書推薦的用法用量使用。
3.5 與是否聯合用藥關聯性評價
236例ADR中,僅6.36%患者的病歷記錄了聯合用藥情況,考慮老年患者聯合用藥使用率高,不能排除部分報告未描述聯合用藥。聯合使用的藥物主要包括吡拉西坦氯化鈉注射液、天麻素注射液、長春西汀注射液及奧扎格雷鈉氯化鈉注射液。由表3可見,聯合用藥使循環系統發生ADR的危險增加。《專家建議》指出,需特別注意安全性問題:由于丹參酮ⅡA磺酸鈉能競爭性抑制人肝微粒體中的CYP1A2,與CYP1A2底物藥物(如咖啡因、對乙酰氨基酚、非那西丁等)聯用會導致代謝減慢,血藥濃度升高,藥理作用或毒副作用增加。如必須合用時,需密切觀察患者病情,必要時可適當減少或用其他藥物替代[14]。
3.6 與原患疾病關聯性評價
該藥藥品說明書適應證為冠心病、心絞痛、心肌梗死的輔助治療,也是《專家建議》的一級推薦適應證,二級推薦缺血性腦卒中[14]。236例ADR中,原患疾病主要為冠心病、腦梗死、腦動脈供血不足、心肌梗死、心絞痛、眩暈,無超適應證使用情況。由表3可見,原患疾病為冠心病是發生全身性損害、消化系統、皮膚及其附件、循環系統ADR的危險因素,腦梗死也是發生全身性損害、消化系統、循環系統ADR的危險因素,而精神神經系統的ADR與原患疾病無明顯關系。
3.7 小結
針對丹參酮ⅡA磺酸鈉注射液所致ADR,為保證臨床合理用藥,應加強ADR的預防[18]。在臨床使用過程中,應嚴格掌握適應證,嚴格按說明書推薦的用法用量使用,按藥品說明書推薦使用的溶劑和溶劑量使用,避免聯合用藥。另外,丹參酮ⅡA作為天然抗氧化劑[14],極易發生氧化還原反應。因此,還需特別注意溶劑選擇、配伍情況及儲存環境溫度。

