慢性腎臟病患者骨密度與骨代謝生化指標的相關性分析
何舒寧 郝麗 張森
安徽醫科大學第二附屬醫院,安徽 合肥 230601
慢性腎臟病(chronic kidney disease,CKD)是全球性的健康問題。CKD患者早期常并發慢性腎臟病-礦物質和骨代謝紊亂(chronic kidney disease-mineral and bone disorder,CKD-MBD),不僅可引起腎性骨營養不良(renal osteodystrophy,ROD),表現出骨痛、骨折等癥狀[1],同時也會出現血管及軟組織鈣化。ROD患者會出現骨密度(bone mineral density,BMD)降低,導致骨折風險顯著升高[2]。骨折不僅影響患者的生活質量,而且導致死亡風險的增加[3]。因此,早期評估CKD患者的骨骼健康非常重要。
對于ROD患者,臨床上常規檢測的骨代謝生化指標包括鈣、磷及甲狀旁腺素(parathyroid hormone,PTH)等。骨特異性堿性磷酸酶(bone-specific alkaline phosphatase,BALP)是堿性磷酸酶同工酶的一個亞型,近年來,作為骨形成的標志物,對判斷骨代謝的狀態有重要的意義。在2017年更新的KDIGO指南[4]中,亦建議對其進行檢測以評估CKD-MBD中的骨病。
目前,國內外對于BMD與骨代謝生化指標之間的相關性以及BMD對CKD-MBD早期評估的價值的臨床研究仍較少。因此,本研究通過分析BMD在CKD患者中的變化規律,分析BMD與各骨代謝生化指標的相關性以及影響BMD的危險因素,來探討BMD和骨代謝生化指標聯合檢測在早期評估和管理CKD-MBD中的價值,以期盡早干預并發癥,提高患者生活質量,延長患者的生存壽命。
1 材料和方法
1.1 一般資料
選取2018年1月1日-2019年9月30日于安徽醫科大學第二附屬醫院腎臟內科就診的CKD3~5D期患者128例,年齡27~79歲,其中男性88例(68.75 %),女性40例(31.25 %)。原發病中,慢性腎小球腎炎67例(52.34 %),高血壓腎損害21例(16.41 %),糖尿病腎病13例(10.16 %),梗阻性腎病10例(7.81 %),多囊腎8例(6.25 %),其他9例(7.03 %)。納入標準:年齡≥18歲;CKD病史至少超過1年;血液透析(hemodialysis,HD)組透析時間大于等于3個月。排除標準:急性腎損傷;甲狀旁腺手術史或骨折病史;合并惡性腫瘤;嚴重肝病史;嚴重免疫系統疾病史;長期應用激素者等。另選取15例健康人員作為對照組,年齡25~66歲,其中男性6例(40 %),女性9例(60 %)。CKD組與對照組的性別和年齡差異均無統計學意義(P均>0.05),具有可比性。
1.2 方法
1.2.1觀察對象:收集所有入組人員的年齡、性別、身高、體重等,CKD組原發病、并發癥及合并癥情況,近期使用藥物情況(如近期有無長期使用激素),HD患者的透析齡、透析方式等情況,利用公式計算得出體質量指數(body mass index,BMI)。
1.2.2實驗室指標檢測:所有入組人員均于清晨空腹時抽取靜脈血,利用全自動血細胞分析儀及全自動生化分析儀檢測血肌酐(serum creatinine,SCr)、血紅蛋白(hemoglobin,Hb)、白蛋白(albumin,ALB)、鈣(calcium,Ca)、磷(phosphorus,P)等指標,利用化學免疫發光法檢測PTH。同時所有入組人員均留取0.5 mL的血清標本,置于- 80 ℃冰箱中保存待測。
1.2.3BALP檢測:所有入組人員的血清標本收集完畢后,統一采用ELISA法檢測血清BALP水平。
1.2.4BMD檢測:利用雙能X線吸收法(dual energy x-ray absorptiometry,DXA)檢測所有入組人員的腰椎(L1~4)以及左髖關節BMD,單位以g/cm2表示。由同一技師、同一臺儀器完成BMD的檢測。
1.2.5分組方法:利用腎臟病飲食改良(modification of diet in renal disease,MDRD)簡化公式計算得出估算腎小球濾過率(estimated glomerular filtration rate,eGFR),根據eGFR將CKD組分為CKD3期組、CKD4期組和CKD5期組,再根據是否透析分為CKD5期非透析(non dialysis,ND)組(CKD5ND組)和CKD5期HD組(CKD5HD組)。
1.3 統計學處理
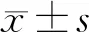
2 結果
2.1 各組間各指標情況
2.1.1BMD狀況:CKD3期組、CKD4期組、CKD5ND期組和CKD5HD期組的髖關節BMD均低于對照組,隨著分期的進展,髖關節BMD不斷降低,差異具有統計學意義(P<0.05)。各組間腰椎BMD比較差異均不具有統計學意義(P均>0.05)。
2.1.2BALP、Ca、P和LogPTH水平:CKD3期組、CKD4期組、CKD5ND期組和CKD5HD期組BALP水平均高于對照組(P均<0.05)。CKD5ND期組Ca明顯低于其他各組(P均<0.05),CKD5ND期組和CKD5HD期組P明顯高于對照組、CKD3期組和CKD4期組,差異均具有統計學意義(P均<0.05)。CKD5HD組logPTH水平明顯高于對照組、CKD3期組、CKD4期組和CKD5ND組,差異具有統計學意義(P均<0.05)。詳見表1。

表1 各組各項指標情況Table 1 The status of indexes between groups
2.2 BMD與各指標間的Pearson相關分析
結果顯示,髖關節BMD與ALB呈正相關(P<0.05),與年齡、SCr、P、LogPTH、BALP呈負相關(P<0.05),與BMI、Hb和Ca無相關性(P均>0.05)。腰椎BMD與各項指標之間均無相關性(P均>0.05)。詳見表2。

表2 BMD與各指標的Pearson相關分析
2.3 BMD的影響因素分析
分別以腰椎BMD和髖關節BMD為因變量,以年齡、BMI、SCr、Hb、ALB、Ca、P、LogPTH和BALP為自變量進行多元線性回歸分析。結果顯示,年齡、BMI和PTH是影響髖關節BMD的危險因素;PTH是影響腰椎BMD的危險因素。詳見表3。

表3 BMD影響因素的多元線性回歸分析
3 討論
CKD是慢性進展性疾病,終末期腎臟病患者的腎臟功能會完全喪失,腎臟替代治療是目前唯一可以延長患者壽命的方法。CKD-MBD是CKD患者的早期常見并發癥,不僅影響患者的生活質量,而且導致死亡率的增加。因此,早期評估和管理CKD-MBD非常重要。
3.1 BMD在評估CKD-MBD中的價值
CKD-MBD中的ROD是一種復雜的骨骼疾病。骨活檢是診斷ROD的金標準,但由于其為侵入性方法,且需要高昂的檢測費用等,限制了其作為日常臨床工具的實用性,目前臨床上常使用非侵入性方法來評估CKD患者的骨質量。ROD患者可表現為BMD下降,最終可發生骨折事件。DXA是目前臨床檢測BMD以評估骨質量有效且常用的工具。據報道,CKD患者的骨折發生率是非CKD患者的2~100倍[5]。重要的是,CKD患者骨折后的死亡率較非CKD患者高出3倍[3]。有研究[6]顯示,CKD患者腎功能下降與髖關節BMD下降存在直接相關性。也有研究[7]發現,透析前和透析患者的低BMD與骨折的高風險有關。本研究發現,與腰椎BMD相比,CKD患者髖關節BMD與腎功能關系更為密切,提示髖關節BMD為早期骨代謝紊亂的敏感指標。這可能與髖關節為主要的承重關節,其骨皮質含量明顯高于腰椎,而CKD患者的骨骼變化主要影響骨皮質,對骨小梁影響較小有關。因此本研究中各組間腰椎BMD無顯著差異,而髖關節BMD存在顯著差異。本研究發現,SCr水平與BMD呈負相關,隨著CKD進展,髖關節BMD不斷降低,多元線性回歸分析結果提示腎功能減退是髖關節BMD降低的危險因素,這一結果與Bezerra等[8]研究結果一致。因此,建議臨床需重視CKD3~5D期患者檢測BMD來預測骨折風險,以早期進行干預。
3.2 CKD患者BMD與骨代謝生化指標的相關性
3.2.1鈣、磷:鈣能刺激成骨細胞形成,抑制破骨細胞生成。磷能直接刺激破骨細胞凋亡,抑制破骨細胞分化。一項針對腎移植后合并低鈣血癥的患者行甲狀旁腺切除術后隨訪的研究[9]發現,隨著血鈣恢復到正常水平,患者股骨頸BMD顯著升高。另外一項研究[10]發現給予CKD大鼠高磷飲食可導致BMD下降。這提示BMD與鈣、磷水平具有相關性。本研究發現,隨著CKD患者血磷水平的升高,髖關節BMD下降,而血鈣水平與BMD無明顯相關性,這可能與目前臨床上CKD患者會定期檢測鈣磷水平,而患者常服用含鈣的磷結合劑,從而導致血鈣水平趨于正常有關。
3.2.2PTH:PTH仍然是目前臨床評估ROD最常用的生物標志物。在一項針對CKD患者的研究[11]中,高PTH水平與低骨皮質和骨小梁BMD相關。但應該注意的是,高和低水平血清PTH都與高骨折風險具有相關性[12]。有研究[13]是對CKD5D期患者髖部骨折危險因素的研究發現,低PTH水平是髖關節骨折高風險的獨立危險因素。本研究結果顯示,CKD患者髖關節BMD與PTH具有相關性,隨著PTH升高,髖關節BMD下降,且高PTH水平是髖關節BMD降低的危險因素,與上述研究結果相對一致。
3.2.3BALP:BALP是骨形成的生物標志物。當CKD患者體內血清鈣水平降低時,刺激甲狀旁腺分泌PTH,血清PTH濃度升高,促進腎臟合成維生素D,它可激活靜止的成骨細胞,從而合成BALP釋放至血液中。BALP與CKD患者骨折的發生密切相關。一項針對HD患者的研究[14]發現,BALP水平升高與骨皮質BMD下降相關。本研究發現,CKD患者髖關節BMD與血清BALP水平呈負相關,隨著BALP水平的升高,CKD患者髖關節BMD下降,提示血清BALP水平在預測CKD患者骨折風險方面具有一定的價值。
以上數據表明,CKD患者BMD與P、PTH和BALP等骨代謝生化指標具有相關性,盡管這些生化指標在改善患者骨折等相關結局的效用尚未得到證實,但可以利用這些指標在一定程度上代替骨活檢來制定相應的治療方案。
4 結論
綜上所述,與腰椎BMD相比,髖關節BMD是CKD患者早期骨代謝異常的敏感指標。隨著CKD進展,髖關節BMD逐漸降低,髖關節BMD與P、PTH和BALP呈負相關,PTH水平是影響髖關節BMD的危險因素。早期聯合檢測髖關節BMD和骨代謝生化指標對早期評估和管理CKD-MBD具有重要的價值。
5 局限性和前景
本研究納入的樣本量共143例,仍舊偏少,且未將研究對象近期使用的所有藥物納入影響因素分析,可能會造成部分數據偏倚。在接下來的研究中,將進一步擴大樣本量,將藥物納入影響因素分析,并對評估CKD-MBD的其他檢測方法和指標進行進一步的探討。

