不同部位起搏對永久心臟起搏器植入患者血清心肌酶及氮末端腦鈉肽前體水平的影響*
秦淑娟,蔡 林,汪 漢
成都市第三人民醫院 心血管內科(成都 610074)
心臟起搏器植入治療是采用特定頻率脈沖電流,以導線和電極對心臟進行刺激,繼而代替心臟起搏點促進心臟搏動的療法,是目前治療緩慢性心律失常患者的有效手段[1]。心臟起搏器植入的起搏部位存在一定爭議,其中心尖部起搏(right ventricular apex,RVA)為傳統起搏方式,具有電極易固定、起搏參數穩定等優點,但其可能改變生理性心室激動順序,引起異常電激動,致心功能障礙,甚至引起心肌損傷標志物-氮末端腦鈉肽前體(NT-proBNP)變化[2]。右心室間隔部起搏(right ventricular septum,RVS)起搏位點與正常傳導系統更接近,理論上RVS起搏時室內和室間隔同步性、患者血流動力學同生理狀態更接近,但心功能惡化仍是RVS起搏的遠期并發癥之一[3]。希氏-浦肯野系統作為心臟特殊組織,傳導速度快,可起到協同心室肌的電機械舒縮作用,因而學者探索以永久性希氏束起搏作為理想生理性起搏位點,但其操作較難,有房室交叉感知、起搏閾值高等不足,會縮短起搏器壽命[4]。左束支區域起搏(left bundle branch pacing,LBBP)操作更便捷,且術者學習曲線不長,較好解決了希氏束起搏的不足,但其有效性和安全性有待進一步觀察[5]。本研究主要分析RVA、RVS、LBBP 3種起搏部位對永久心臟起搏器植入患者血清心肌酶、NT-proBNP的影響與臨床意義,現報道如下。
1 資料與方法
1.1 臨床資料
選取2017年1月至2019年4月成都市第三人民醫院心血管內科收治的120例永久心臟起搏器植入患者為研究對象。納入標準:1)心電圖、影像學檢查等確診為房室傳導阻滯或病態竇房結綜合征,需進行永久性起搏器植入;2)術前紐約心臟病協會(NYHA)心功能分級Ⅰ~Ⅱ級,左室射血分數(LVEF)<55%,且符合美國心臟病學會(ACC)起搏器Ⅰ或Ⅱa標準,意識清晰。排除標準:1)合并嚴重肝腎功能障礙;2)因持續性房顫并長間歇而植入起搏器;3)合并先心病、冠心病、完全性左右束支傳導阻滯、房性心律失常、精神障礙者。采用隨機數字表法將研究對象分為RVA組、RVS組、LBBP組,每組40例。3組一般資料比較,差異無統計學意義(P>0.05),具有可比性(表1)。

表1 3組一般資料比較
1.2 方法
1.2.1 RVA組 經鎖骨下靜脈通道植入右室螺旋電極與心房電極,放置螺旋電極在心尖部位,對起搏閾值和感知功能進行檢測,調整好起搏頻率,將心房電極放置在右心耳,起搏電極與脈沖發生器進行連接,并埋在胸前皮下囊袋中。以X線與心電圖確定電極導線頭端在心尖部位。心尖部電極與間隔部電極均為螺旋電極。
1.2.2 RVS組 采用與RVA相同步驟,于鎖骨下靜脈通道以“J”型鋼絲將右室螺旋電極和心房電極導絲送至右室流出道,后更換近“L”型鋼絲,放置螺旋電極在右心室間隔部位,檢測起搏閾值、感知功能,對起搏頻率進行調整,心房電極放置在右心耳,起搏電極和脈沖發生器連接,埋在胸前皮下囊袋中。X線、心電圖確定電極導線頭端在右心室間隔部位。
1.2.3 LBBP組 依據起搏器的一般操作方法,對部分完全性房室傳導阻滯者實施臨時起搏保護,術中穿刺左腋靜脈或鎖骨下靜脈,后送入3830-65 cm電極達右室流出道中低位間隔部左室面,予以左束支區域起搏。植入位置準確判斷標準:V1導聯出現右束支阻滯,窄QRS波形,下壁導聯rS波,起搏參數(起搏閾值<1.0 V,感知>5.0 mV,阻抗在400~1 200 Ω)滿意,結合X線圖像進行判定。后將脈沖發生器埋植在左胸前皮下囊袋。
1.3 觀察指標
1)采用美國Acuson Sequoia512心臟多普勒超聲(頻率2.25~4.25 MHz)檢測3組術前、術后1個月[左室收縮末期內徑(LVESD)、左室舒張末期內徑(LVEDD)、左室內徑(LAD)、左室射血分數(LVEF)]; 2)比較3組術中、隨訪期間(取隨訪6個月的資料分析)、起搏導線參數(起搏閾值、感知、阻抗); 3)取3組術前、術后1個月靜脈血,離心分離血清,采用速率法及電泳法測定肌酸激酶同工酶(CK-MB)、天冬氨酸轉氨酶(AST)、乳酸脫氫酶(LDH)水平,應用膠體金免疫層析法(南京基蛋生物科技公司FIA8000系列免疫定量分析儀)測定NT-proBNP水平;4)記錄3組術后6個月內并發癥(包括心力衰竭、新發房顫、室間隔穿孔等)發生率及全因死亡率。
1.4 統計學方法
采用SPSS 20.0統計軟件對數據進行處理,并發癥發生率等定性資料以百分比(%)表示,采取2檢驗;心功能指標、起搏參數、血清心肌酶、NT-proBNP水平等定量資料以表示,行單因素方差分析、重復測量數據的方差分析及LSD-t檢驗,檢驗水準α除特別說明外均設定為0.05。
2 結果
2.1 3組心功能指標比較
RVS組、LBBP組術后LVESD、LVEDD低于RVA組;RVS組、LBBP組LVEF較RVA組高(P<0.05);RVS組、LBBP組上述各指標及3組LAD比較,差異均無統計學意義(P>0.05)(表2)。
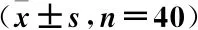
表2 3組心功能指標比較
注:與術前比較,*P<0.05;與RVA組比較,#P<0.05
2.2 3組起搏參數比較
RVS組、LBBP組隨訪起搏閾值、阻抗低于RVA組,差異有統計學意義(P<0.05);RVS組、LBBP組隨訪起搏閾值、阻抗比較,差異無統計學意義(P>0.05);3組感知比較,差異無統計學意義(P>0.05)(表3)。
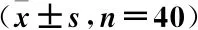
表3 3組起搏參數比較
注:與術中比較,*P<0.05;與RVA組比較,#P<0.05
2.3 3組血清心肌酶、NT-proBNP水平比較
術后RVS組、LBBP組血清NT-proBNP水平低于RVA組,3組CK-MB、AST、LDH水平比較,差異無統計學意義(P>0.05)(表4)。

表4 3組血清心肌酶、NT-proBNP水平比較
注:與術前比較,*P<0.05;與RVA組比較,#P<0.05
2.4 3組并發癥發生率比較
3組術后心力衰竭、新發房顫、全因死亡率比較,差異無統計學意義(P>0.05);3組均無室間隔穿孔發生(表5)。

表5 3組并發癥發生率比較 [n(%),n=40]
3 討論
永久性心臟起搏器植入可延長心律失常患者生命,改善其生活質量[6]。長期以來,RVA為起搏器植入術中最常用的起搏部位,其肌小梁豐富而發達,較少受血流沖擊,因此電極容易固定,但長期RVA可能影響左室內激動-收縮順序,使組織病理學、血流動力學異常,影響患者心功能[7]。隨主動螺旋固定導線發明,右室選擇性部位起搏成為可能,其中RVS及LBBP為主流選擇部位,RVS起搏與右室流出道或希氏束系統接近,能保證電信號經正常希氏束-浦肯野纖維系統而減少不同步性[8]。研究[9]顯示RVS治療緩慢性心律失常安全、有效;Huang等[10]2017年報道了1例擴張型心肌病伴完全性左右束支傳導阻滯患者采用3830導線行LBBP,糾正左束支阻滯,效果良好,但其在電學參數、臨床效果上是否優于RVA與RVS尚缺乏臨床數據。起搏器植入可改善緩慢性心律失常患者生存及生活質量,但無論選擇何種部位起搏,均無法完全做到正常的心室激動順序,可能會對心臟組織結構、心室收縮功能產生不同程度影響,出現心功能下降。本研究中,RVS組、LBBP組術后LVESD、LVEDD低于RVA組;RVS組、LBBP組LVEF較RVA組高,RVS組、LBBP組上述各指標及3組的LAD比較,差異無統計學意義,與賈鳳英等[11]研究結果相近,表明RVS、LBBP相比于RVA對永久性起搏器植入患者心功能影響更小,可能是因為RVS的起搏點位于室間隔間斷,起搏期間自身節律可經正常途徑傳導,保證心室間激動-機械運動一致性[12],而LBBP起搏電極與希氏束接近,輸出電壓可穿過纖維鞘而激動希氏束,較好避免右室心尖起搏的不良影響,且LBBP也實現了心臟電和機械同步行,能較好保留左心室功能,因此是較理想的起搏方式[13]。RVS組、LBBP組隨訪起搏閾值、阻抗低于RVA組,3組感知比較差異無統計學意義,與曾春苗等[14]研究結果一致,表明與RVA相比,RVS或LBBP仍然具有較好的感知功能,RVS、LBBP雖然起搏閾值與阻抗較低,但仍在理想參數范圍內,3個起搏部位導線傳導性能均安全、穩定。
心肌細胞的酶含量豐富,其中CK-MB、AST、LDH在心肌細胞壞死時,均可在24~72 h內出現高峰,安裝起搏器患者,其體內心肌酶也會發生變化[15];NT-proBNP也是心肌損傷標志物[16]。本研究術后RVS組、LBBP組血清NT-proBNP水平低于RVA組,3組CK-MB、AST、LDH比較差異無統計學意義,表明3種部位起搏方式均會導致永久性起搏器植入患者心肌損傷,但RVS、LBBP的損傷較小,可能是因為RVS、LBBP起搏部位較RVA起搏部位更接近生理起搏部位,更能減少對患者心功能的影響,改善其預后。長期RVA可引起心肌細胞排列紊亂、營養不良性鈣化等病理改變,形成肉芽組織與結締組織增生,因此RVA引起心功能損傷和組織學損傷有一定關聯,是起搏導致心肌病的病理基礎[17]。RVS導絲植入希氏束遠端的間隔部心肌,不直接接觸心臟特殊傳導系統,不記錄傳導系統定位,理論上不會損傷傳導系統,直接起搏室間隔左右側心肌而間接獲得心臟傳導組織[18]。但研究[19]報道RVS與RVA對心功能損傷程度比較,差異無統計學意義,本研究結果與之不符,可能與研究樣本量等因素有關。而LBBP中導絲傳入室間隔左側面,直接接觸左心室內膜下的左束支或左前與左后分支,記錄左束支或前后分支電位,在低頻高通濾波時出現局部損傷電流,而選擇性起搏左束支或左前后支,提高了治療成功率。
本研究3組術后心力衰竭、新發房顫、全因死亡率比較,差異無統計學意義,3組全因死亡率均低于5%,表明3種起搏部位用于永久性起搏器植入患者中均可獲得良好的長期預后,當然RVA起搏時心臟激動順序異常,可能降低患者心室收縮與舒張功能,加重心臟負荷,增加心力衰竭等發生風險[20],本研究尚未發現這種差異,可能與隨訪時間短、起搏器植入對心房生理性傳導影響較小等因素有關。此外研究[21]報道,LBBP1例術中向間隔左側旋扭導線時導線阻抗突然降低,起搏失奪獲,表明穿透左心室內膜,回轉及回撤導線,起搏重新奪獲,短期隨訪雖未發生血栓栓塞事件,但存在這種可能性,因此后期可擴大樣本量,進一步分析LBBP與RVS在起搏植入中的優越性,并提高起搏植入術者手術操作水平。
綜上所述,RVA、RVS、LBBP用于永久心臟起搏器植入中均可獲得良好預后,且后二者對心功能、血清心肌酶、NT-proBNP的影響均小于前者,臨床可進一步開展大樣本量實踐證實。

